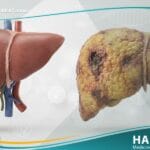
يعد الفيروس المضخم للخلايا (Cytomegalovirus)، والمعروف اختصاراً بـ (CMV)، واحداً من أكثر الفيروسات انتشاراً وغموضاً في عالم الطب البشري، حيث ينتمي إلى عائلة فيروسات الهربس (Herpesviridae). تشير التقارير العلمية الصادرة عن مدونة حياة الطبية إلى أن هذا الفيروس يمتلك قدرة استثنائية على البقاء كامناً داخل أنسجة الجسم مدى الحياة بعد الإصابة الأولية، مما يجعله تحدياً مناعياً مستمراً. على الرغم من أن غالبية الإصابات تمر دون ملاحظة لدى الأفراد الأصحاء، إلا أن الفيروس المضخم للخلايا يمثل تهديداً حقيقياً للأشخاص الذين يعانون من ضعف المناعة والأجنة أثناء فترة التطور الرحمي.
ما هو الفيروس المضخم للخلايا؟
يُعرف الفيروس المضخم للخلايا بأنه كائن مجهري من فصيلة فيروسات الهربس بيتا، ويتميز بقدرته على إصابة الخلايا البشرية وإحداث تضخم ملحوظ في حجمها مع تكوين أجسام احتواء نووية. (Snippet Bait): الفيروس المضخم للخلايا هو عدوى فيروسية شائعة تستوطن الجسم بشكل دائم بعد الإصابة؛ وتظهر خطورته عند تنشيطه لدى مرضى نقص المناعة أو انتقاله للجنين، مسبباً تشوهات خلقية أو تلفاً في الأعضاء الحيوية. بيولوجياً، يستهدف هذا الفيروس الخلايا الطلائية والبطانية، ويقوم بدمج مادته الوراثية (DNA) داخل نواة الخلية المضيفة، مما يؤدي إلى ظهور مظهر مجهري فريد يُشبه “عين البومة”. وتشير التقديرات الوبائية العالمية إلى أن ما يقرب من 60% إلى 90% من البالغين حول العالم يحملون هذا الفيروس، مما يجعله جزءاً لا يتجزأ من الخريطة الفيروسية البشرية.
أعراض الفيروس المضخم للخلايا
تتنوع المظاهر السريرية المرتبطة بـ الفيروس المضخم للخلايا بناءً على كفاءة الجهاز المناعي للمصاب، حيث تنقسم الأعراض إلى فئات تخصصية دقيقة تعكس شدة الغزو الفيروسي. وفقاً لدراسات الأكاديمية الأمريكية لأطباء الأطفال، فإن الأعراض تختلف جذرياً بين البالغين الأصحاء وبين المواليد الذين تعرضوا للعدوى داخل الرحم، وتتمثل في الآتي:
- الأعراض لدى البالغين الأصحاء (العدوى الأولية):
- ارتفاع طفيف في درجة حرارة الجسم يشبه الحمى مجهولة المصدر.
- شعور بالوهن العام والإجهاد العضلي الذي قد يستمر لأسابيع متواصلة.
- تضخم العقد اللمفاوية في الرقبة والإبط، مع احتمالية وجود آلام في الحلق.
- فقدان الشهية المصحوب بأوجاع خفيفة في المفاصل.
- أعراض الإصابة لدى مرضى ضعف المناعة (تنشيط الفيروس):
- التهاب الشبكية: فقدان تدريجي للرؤية أو ظهور “عوامات” في العين، وهو عرض شائع لدى مرضى نقص المناعة المكتسبة.
- التهاب القولون: إسهال حاد ومزمن يترافق أحياناً مع خروج دم وآلام تشنجية في البطن.
- التهاب الكبد: اصفرار الجلد واليرقان وارتفاع إنزيمات الكبد بشكل حاد.
- التهاب الدماغ: نوبات من التشوش الذهني، الصداع الحاد، أو ضعف التنسيق الحركي.
- أعراض العدوى الخلقية عند حديثي الولادة:
- صغر حجم الرأس بشكل ملحوظ (Microcephaly) نتيجة تأثر نمو الدماغ.
- تضخم الطحال والكبد مع ظهور بقع أرجوانية تحت الجلد (طفح فطيرة التوت).
- فقدان السمع الحسي العصبي، والذي قد لا يظهر بوضوح إلا بعد أشهر من الولادة.
- تأخر النمو البدني واختلال في المهارات الحركية الدقيقة.
أسباب الفيروس المضخم للخلايا
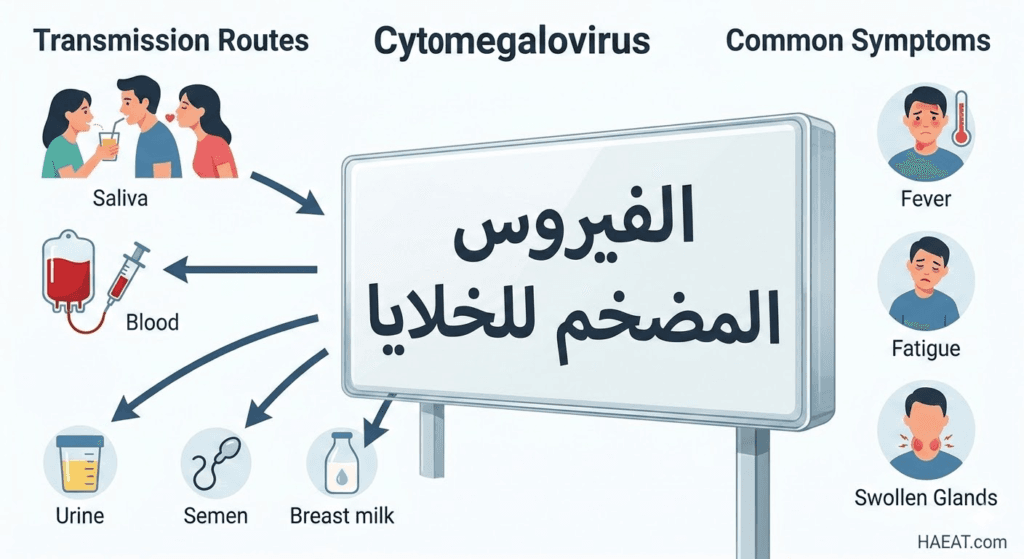
تحدث الإصابة بـ الفيروس المضخم للخلايا نتيجة التعرض المباشر لسوائل الجسم التي تحتوي على الجزيئات الفيروسية النشطة، حيث ينتقل الفيروس عبر التلامس الوثيق. توضح مراكز السيطرة على الأمراض والوقاية منها (CDC) أن الفيروس يمكن أن يظل نشطاً على الأسطح لفترة قصيرة، لكن الانتقال يتطلب عادةً اتصالاً مباشراً بالسوائل الحيوية:
- سوائل الجسم الحاملة للعدوى:
- اللعاب والبول، وهما المصدران الرئيسيان لانتقال العدوى بين الأطفال في بيئات الحضانة والمدارس.
- الدم، حيث يمكن أن ينتقل الفيروس عبر عمليات نقل الدم الملوث أو مشاركة الإبر الوريدية.
- السوائل التناسلية (المني والإفرازات المهبلية)، مما يجعل الاتصال الجنسي أحد طرق الانتقال البارزة للبالغين.
- حليب الأم، حيث يمكن للأم المصابة نقل الفيروس المضخم للخلايا لرضيعها، وإن كان ذلك نادراً ما يسبب أعراضاً خطيرة للأطفال المكتملين.
- آلية الانتقال الرأسي (من الأم للجنين):
- عبر المشيمة أثناء فترة الحمل، خاصة إذا أصيبت الأم بالعدوى الأولية لأول مرة خلال الثلثين الأول أو الثاني.
- أثناء عملية الولادة نتيجة الاحتكاك بإفرازات عنق الرحم الملوثة بالفيروس.
- عمليات زراعة الأعضاء:
- يعتبر الفيروس أحد أهم أسباب فشل زراعة الأعضاء، حيث ينتقل من العضو المزروع (إذا كان المتبرع مصاباً) إلى المتلقي الذي يتناول أدوية مثبطة للمناعة.
متى تزور الطبيب؟
تتطلب الإصابة بـ الفيروس المضخم للخلايا استشارة طبية فورية عند ظهور علامات تشير إلى انتشار الفيروس في الأعضاء الحيوية، خاصة لدى الفئات الهشة مناعياً. يشير موقع حياة الطبي إلى أن الكشف المبكر عن نشاط الفيروس يساهم في تقليل الأضرار الدائمة التي قد تلحق بالجهاز العصبي أو البصري.
للبالغين والأصحاء
يجب التوجه لطلب الرعاية الصحية إذا استمرت أعراض تشبه “الأنفلونزا” لأكثر من أسبوعين دون تحسن ملحوظ، أو في حالة ظهور آلام حادة في الجانب الأيمن العلوي من البطن. كذلك، فإن ظهور بقع داكنة في مجال الرؤية أو ضبابية غير مبررة في العين يستدعي فحصاً فورياً لاستبعاد التهاب الشبكية الناتج عن الفيروس المضخم للخلايا.
للأطفال وحديثي الولادة
بالنسبة للوالدين، يجب مراقبة استجابة الرضيع للأصوات؛ فإذا بدا الطفل لا يتفاعل مع الضوضاء، فقد يكون ذلك علامة على فقدان السمع المرتبط بالعدوى الفيروسية. أيضاً، فإن ظهور اليرقان المستمر أو ضعف زيادة الوزن لدى الرضيع يتطلب إجراء تحاليل دم متخصصة للكشف عن الأجسام المضادة للفيروس.
علامات التحذير عند مرضى زراعة الأعضاء
تعتبر هذه الفئة هي الأكثر عرضة لخطر الموت الناتج عن مضاعفات الفيروس المضخم للخلايا؛ لذا يجب مراجعة الطبيب فور حدوث:
- ضيق حاد في التنفس أو سعال جاف مستمر (قد يشير لالتهاب الرئة الفيروسي).
- ارتفاع مفاجئ في درجة الحرارة غير مستجيب للمسكنات التقليدية.
- تدهور مفاجئ في نتائج تحاليل وظائف العضو المزروع (كارتفاع الكرياتينين في زراعة الكلى).
عوامل خطر الإصابة بـ الفيروس المضخم للخلايا
تتفاوت احتمالية التعرض لعدوى الفيروس المضخم للخلايا بناءً على البيئة المحيطة والحالة الصحية العامة، حيث يزداد الخطر في أوساط معينة تتطلب احتكاكاً وثيقاً أو تعاملاً مع سوائل بيولوجية. يستعرض موقع HAEAT الطبي أهم الفئات والظروف التي ترفع من وتيرة خطر الإصابة أو إعادة تنشيط الفيروس الكامن:
- العاملون في دور الحضانة والتعليم المبكر: نظراً لشيوع طرح الفيروس المضخم للخلايا في بول ولعاب الأطفال الصغار، فإن المعلمين ومقدمي الرعاية هم الأكثر عرضة للعدوى الأولية.
- مرضى نقص المناعة البشرية (HIV/AIDS): تضعف القدرة الرقابية للجهاز المناعي، مما يسمح للفيروس بالخروج من حالة الكمون ومهاجمة الأعضاء الحيوية مثل العين والرئتين.
- خاضعو عمليات زراعة الأعضاء والنخاع العظمي: يضطر هؤلاء المرضى لتناول أدوية مثبطة للمناعة لمنع رفض العضو، مما يجعلهم “بيئة خصبة” لنشاط الفيروس المضخم للخلايا.
- النساء الحوامل: تزداد الخطورة إذا كانت الحامل تعمل في مهن تتطلب التعامل مع الأطفال، حيث أن العدوى الأولية أثناء الحمل قد تؤدي لنتائج كارثية على الجنين.
- مرضى السرطان الخاضعون للعلاج الكيميائي: يؤدي تثبيط النخاع العظمي إلى تقليل عدد الخلايا اللمفاوية التائية (T-cells) المسؤولة عن كبح الفيروس.
- العاملون في القطاع الصحي: خاصة أولئك الذين يتعاملون مع وحدات غسيل الكلى أو المختبرات التي تعالج عينات السوائل البشرية الملوثة بـ الفيروس المضخم للخلايا.
مضاعفات الفيروس المضخم للخلايا
يمكن أن يتسبب الفيروس المضخم للخلايا في أضرار هيكلية ووظيفية جسيمة للأعضاء إذا لم يتم التدخل الطبي في الوقت المناسب، خاصة عندما يفشل الجهاز المناعي في السيطرة على تكاثر الفيروس. وفقاً لإحصائيات من “كليفلاند كلينك”، فإن المضاعفات الجهازية للعدوى تشمل ما يلي:
- التهاب الشبكية (CMV Retinitis): يعتبر من أخطر المضاعفات المؤدية للعمى، حيث يهاجم الفيروس المضخم للخلايا خلايا الشبكية الحساسة للضوء مسبباً نزيفاً ونخراً في أنسجة العين.
- التهاب الرئة الخلالي: يسبب صعوبات تنفسية حادة ونقصاً في الأكسجين، وهو سبب رئيسي للوفاة بين مرضى زراعة النخاع العظمي المصابين بالعدوى.
- التهاب الدماغ والجهاز العصبي: قد يؤدي نشاط الفيروس إلى التهاب السحايا أو التهاب الجذور العصبية، مما يسبب شللاً أو تدهوراً إدراكياً حاداً.
- القرحة الهضمية والتهاب القولون: يتسبب الفيروس المضخم للخلايا في تآكل بطانة الأمعاء والمعدة، مما يؤدي إلى نزيف هضمي حاد وثقوب في الجدار المعوي.
- فقدان السمع الحسي العصبي: عند الأطفال المصابين بالعدوى الخلقية، يظل فقدان السمع هو العرض الأكثر شيوعاً وتأثيراً على جودة الحياة على المدى الطويل.
- التهاب عضلة القلب وفشل الأعضاء المتعدد: في حالات نادرة وحادة، يمكن أن يهاجم الفيروس القلب والكليتين بشكل متزامن.
الوقاية من الفيروس المضخم للخلايا
تعتمد استراتيجية الوقاية من الفيروس المضخم للخلايا بشكل أساسي على تعديل السلوكيات الشخصية واتباع بروتوكولات صارمة للنظافة، لاسيما لدى النساء في سن الإنجاب والأفراد ذوي المناعة الضعيفة. تؤكد مدونة HAEAT الطبية أن الالتزام بالقواعد التالية يقلل من احتمالية انتقال العدوى بنسبة تتجاوز 80%:
- غسل اليدين المتكرر: بالماء والصابون لمدة لا تقل عن 20 ثانية، خاصة بعد تغيير الحفاضات للأطفال أو ملامسة ألعابهم الملوثة باللعاب.
- تجنب مشاركة الطعام والأواني: ينصح بشدة بعدم مشاركة أكواب الشرب أو الملاعق مع الأطفال الصغار، حيث يعد اللعاب وسيطاً قوياً لنقل الفيروس المضخم للخلايا.
- الحذر عند التعامل مع اللهايات: يجب تجنب تنظيف لهاية الطفل بوضعها في فم البالغين، وهي ممارسة خاطئة شائعة تنقل العدوى فوراً.
- استخدام وسائل الحماية أثناء الجماع: لتقليل خطر انتقال الفيروس عبر السوائل التناسلية بين الشركاء غير المصابين.
- بروتوكولات المستشفيات: فحص وحدات الدم والأعضاء المتبرع بها للتأكد من خلوها من الفيروس المضخم للخلايا قبل نقلها للمرضى المعرضين للخطر.
- التوعية الصحية للحوامل: ضرورة إجراء فحوصات دورية للأجسام المضادة (IgM و IgG) لمراقبة أي عدوى حديثة قد تحدث خلال أشهر الحمل.
تشخيص الفيروس المضخم للخلايا
يتطلب تشخيص الفيروس المضخم للخلايا دقة عالية واستخدام تقنيات مخبرية متطورة للتمييز بين العدوى النشطة، والعدوى السابقة الكامنة، وإعادة التنشيط. تشمل المسارات التشخيصية المعتمدة طبياً ما يلي:
- اختبارات الأمصال (Serology): البحث عن الأجسام المضادة؛ حيث يشير وجود IgM إلى عدوى حديثة أو نشطة، بينما يشير IgG إلى إصابة قديمة ومناعة سابقة.
- اختبار تفاعل البوليميراز المتسلسل (PCR): تقنية بالغة الحساسية تستخدم للكشف عن الحمض النووي لـ الفيروس المضخم للخلايا في الدم، البول، أو السائل النخاعي، وهي المعيار الذهبي لمراقبة الحمل الفيروسي.
- زراعة الفيروسات (Viral Culture): عزل الفيروس من العينات الحيوية، ورغم أنها دقيقة، إلا أنها قد تستغرق وقتاً طويلاً يصل لعدة أيام أو أسابيع.
- خزعة الأنسجة (Biopsy): فحص عينات من الأمعاء أو الرئة تحت المجهر للبحث عن “أجسام الاحتواء” المميزة التي يتركها الفيروس المضخم للخلايا داخل النواة.
- اختبار غسيل القصبات الهوائية: يستخدم لتشخيص التهاب الرئة الناتج عن الفيروس عبر سحب عينة من الرئتين وفحصها مخبرياً.
علاج الفيروس المضخم للخلايا
لا يتطلب الفيروس المضخم للخلايا علاجاً دوائياً للأشخاص الأصحاء في أغلب الأحيان، حيث يتكفل الجهاز المناعي بالسيطرة عليه، ولكن التدخل الدوائي يصبح حتمياً في الحالات السريرية المعقدة.
نهج الرعاية المنزلية والراحة
بالنسبة للحالات الخفيفة، تتركز الرعاية على شرب السوائل بكثرة لمنع الجفاف، والحصول على فترات راحة كافية لمساعدة الجسم على إنتاج الأجسام المضادة الطبيعية ضد الفيروس المضخم للخلايا. يمكن استخدام مسكنات الألم التقليدية مثل الأسيتامينوفين لخفض الحرارة وتقليل الصداع.
العلاجات الدوائية (الأدوية المضادة للفيروسات)
تستهدف هذه الأدوية تثبيط إنزيم “DNA Polymerase” الفيروسي، مما يمنع تكاثر الفيروس وانتشاره في الخلايا السليمة.
الجرعات للبالغين
يتم استخدام عقار “جانسيكلوفير” (Ganciclovir) وريدياً للحالات الحادة، أو “فالجانسيكلوفير” (Valganciclovir) فموياً للحالات الأقل شدة وللوقاية الطويلة. تعتمد الجرعات على وزن المريض ووظائف الكلى، وغالباً ما تستمر دورة العلاج لـ الفيروس المضخم للخلايا من 14 إلى 21 يوماً في المرحلة الحادة.
البروتوكول العلاجي للأطفال
عند الرضع المصابين بالعدوى الخلقية، أظهرت الدراسات أن العلاج المبكر بـ “فالجانسيكلوفير” لمدة 6 أشهر قد يساعد في تحسين نتائج السمع والنمو العصبي، مع مراقبة صارمة لعدد كريات الدم البيضاء لتجنب الآثار الجانبية.
البروتوكولات الحديثة لـ CMV المقاوم للأدوية
في حالات نادرة، يطور الفيروس المضخم للخلايا طفرات جينية تجعله مقاوماً للعلاجات التقليدية. هنا يلجأ الأطباء لاستخدام أدوية بديلة مثل “فوسكارنيت” (Foscarnet) أو “سيدوفوفير” (Cidofovir)، رغم سميتها العالية على الكلى، أو استخدام العقار الحديث “ليتيرموفير” (Letermovir) المصمم خصيصاً لمرضى زراعة النخاع.
دور الأجسام المضادة الوريدية (IVIG) في الحالات الحرجة
يتم اللجوء أحياناً لاستخدام الجلوبيولين المناعي عالي التمنيع (Cytogam) كعلاج مكمل، حيث يوفر أجساماً مضادة جاهزة للارتباط بـ الفيروس المضخم للخلايا ومعادلته، خاصة في حالات التهاب الرئة الحاد بعد زراعة الأعضاء.

الطب البديل والفيروس المضخم للخلايا
على الرغم من أن العلاج الدوائي هو الركيزة الأساسية للحالات الحادة، إلا أن الطب البديل والتكميلي يلعب دوراً حيوياً في دعم الجهاز المناعي لمقاومة الفيروس المضخم للخلايا ومنع إعادة تنشيطه. تشير مجلة حياة الطبية إلى أن بعض المكونات الطبيعية تمتلك خصائص مضادة للفيروسات ومعززة للخلايا اللمفاوية:
- عنصر الزنك: يعد الزنك معدناً أساسياً لمنع تكاثر الفيروسات؛ حيث يعيق قدرة الفيروس المضخم للخلايا على نسخ مادته الوراثية داخل الخلية.
- فيتامين C بجرعات عالية: يعمل كمضاد أكسدة قوي يحمي الخلايا من التلف الناتج عن الالتهاب الفيروسي ويحفز إنتاج الإنترفيرون الطبيعي.
- عشبة القنفذية (Echinacea): تُستخدم لتعزيز استجابة الجهاز المناعي الأولية، مما يقلل من شدة الأعراض عند التعرض لعدوى الفيروس المضخم للخلايا.
- الثوم (الأليسين): يمتلك خصائص طبيعية مضادة للميكروبات والفيروسات، وقد أظهرت بعض الدراسات المخبرية قدرته على تثبيط نشاط فيروسات الهربس.
- الفطر الريشي: يحتوي على “بيتا جلوكان” التي ترفع من كفاءة الخلايا القاتلة الطبيعية (NK cells) في رصد وتدمير الخلايا المصابة بـ الفيروس المضخم للخلايا.
- الأحماض الأمينية (ليسين): يعتقد البعض أن التوازن بين الليسين والأرجينين يساعد في كبح نشاط فيروسات هذه العائلة.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع الفيروس المضخم للخلايا استعداداً دقيقاً لضمان الحصول على التشخيص الصحيح، خاصة إذا كنت تعاني من أعراض غامضة أو كنتِ في مرحلة التخطيط للحمل.
ما يجب عليك فعله
- تدوين قائمة بكافة الأعراض التي تظهر عليك، حتى تلك التي قد تبدو غير مرتبطة بالعدوى الفيروسية.
- كتابة التاريخ الطبي الكامل، بما في ذلك أي عمليات زراعة أعضاء سابقة أو حالات نقص مناعة معروفة.
- حصر الأدوية والمكملات الغذائية التي تتناولها حالياً، حيث قد تتداخل بعض العلاجات مع مضادات الفيروس المضخم للخلايا.
ما الذي تتوقعه من الطبيب
- سيسأل الطبيب عن طبيعة عملك (مثل العمل في دور الحضانة) لتقييم احتمالية التعرض المستمر للفيروس.
- قد يطلب إجراء فحوصات دم دورية لمراقبة “الحمل الفيروسي” (Viral Load) في حال كنت تتلقى علاجاً مثبطاً للمناعة.
- فحص بدني يشمل فحص العقد اللمفاوية، الطحال، والكبد للبحث عن أي تضخم ناتج عن الفيروس المضخم للخلايا.
قائمة الأسئلة الحاسمة للمصابين بضعف المناعة
- ما هي احتمالية انتقال الفيروس من العضو المزروع إليّ؟
- كيف يمكنني مراقبة نشاط الفيروس المضخم للخلايا بشكل دوري في المنزل؟
- هل الأدوية التي أتناولها حالياً تزيد من خطر إعادة تنشيط الفيروس؟
مراحل الشفاء من الفيروس المضخم للخلايا
لا يعني الشفاء من الفيروس المضخم للخلايا التخلص النهائي منه، بل الوصول إلى حالة من “الكمون المستقر” حيث يسيطر الجهاز المناعي على الفيروس.
- مرحلة الاستجابة الحادة: تستمر من أسبوعين إلى 4 أسابيع، حيث تنخفض الحمى وتبدأ العقد اللمفاوية في العودة لحجمها الطبيعي.
- مرحلة التطهير الفيروسي: قد يستمر الجسم في طرح الفيروس المضخم للخلايا في البول واللعاب لعدة أشهر بعد زوال الأعراض الظاهرة.
- مرحلة الكمون (Latency): يستقر الفيروس في الخلايا الجذعية للنخاع العظمي، ويصبح غير نشط مخبرياً (PCR سلبي في الدم) ولكنه موجود جينياً.
- مرحلة المراقبة طويلة الأمد: خاصة للأطفال المصابين بالعدوى الخلقية، حيث تتطلب هذه المرحلة فحص السمع والنظر بشكل سنوي لضمان عدم حدوث تدهور متأخر.
الأنواع الشائعة للفيروس المضخم للخلايا
ينقسم ظهور الفيروس في الجسم إلى أنماط سريرية تختلف في درجة خطورتها وطريقة التعامل الطبي معها:
- العدوى الأولية (Primary Infection): وهي المرة الأولى التي يلتقي فيها الجسم بـ الفيروس المضخم للخلايا، وتكون الأخطر على الحوامل اللواتي لم يسبق لهن الإصابة.
- العدوى الكامنة (Latent Infection): وهي الحالة “النائمة” للفيروس داخل الخلايا، حيث لا يسبب أي ضرر طالما أن المناعة قوية.
- إعادة التنشيط (Reactivation): تحدث عندما يستغل الفيروس المضخم للخلايا ضعف المناعة المؤقت ليبدأ في التكاثر مرة أخرى، وهي شائعة لدى مرضى السرطان.
- العدوى المتكررة (Reinfection): الإصابة بسلالة جديدة من الفيروس تختلف عن السلالة التي سببت العدوى الأولى.
الفيروس المضخم للخلايا والحمل: دليل شامل لحماية الجنين
تعد العدوى الخلقية بـ الفيروس المضخم للخلايا السبب الفيروسي الأول للإعاقات الذهنية وفقدان السمع غير الوراثي عند الأطفال حول العالم. إذا أصيبت الأم بالعدوى لأول مرة أثناء الحمل، فإن احتمال انتقال الفيروس للجنين يصل إلى حوالي 40%، مما قد يؤدي إلى تلف دائم في الجهاز العصبي المركزي. ينصح الأطباء بضرورة إجراء فحص الأجسام المضادة قبل الحمل؛ فإذا كانت النتائج سلبية، يجب اتباع قواعد نظافة صارمة، لاسيما تجنب ملامسة لعاب الأطفال الصغار، لضمان عدم حدوث إصابة أولية قد تهدد سلامة الجنين وتؤدي إلى تشوهات خلقية خطيرة ناتجة عن الفيروس المضخم للخلايا.
التأثيرات العصبية والإدراكية طويلة الأمد للعدوى الخلقية
قد يولد الطفل المصاب بـ الفيروس المضخم للخلايا دون أعراض واضحة (حالات صامتة)، ولكن الدراسات الطويلة الأمد كشفت عن مضاعفات تظهر لاحقاً:
- صعوبات التعلم: خلل في معالجة المعلومات وضعف في التركيز الأكاديمي.
- فقدان السمع التدريجي: قد يبدأ السمع طبيعياً عند الولادة ثم يتدهور خلال السنوات الخمس الأولى.
- اضطرابات التوازن: نتيجة تأثر القنوات الهلالية في الأذن الداخلية بـ الفيروس المضخم للخلايا.
- التأخر اللغوي: صعوبة في اكتساب المفردات وتكوين الجمل مقارنة بالأقران.
التغذية العلاجية والمكملات الداعمة لمرضى نقص المناعة
تلعب التغذية دور “الدرع الواقي” الذي يمنع الفيروس المضخم للخلايا من إعادة التنشيط. يجب التركيز على نظام غذائي غني بمضادات الأكسدة مثل “السيلينيوم” الموجود في المكسرات البرازيلية، و”فيتامين D3″ الذي يلعب دوراً محورياً في تنشيط الخلايا التائية القاتلة. إن تناول الأطعمة الغنية بالبروبيوتيك (البكتيريا النافعة) يعزز مناعة الجهاز الهضمي، وهو خط الدفاع الأول ضد التهاب القولون الذي قد يسببه الفيروس المضخم للخلايا لدى المرضى ذوي المناعة المنخفضة.
مستقبل اللقاحات والأبحاث الجينية في مواجهة الفيروس
تسابق المختبرات العالمية الزمن لتطوير لقاح فعال ضد الفيروس المضخم للخلايا، وتتركز الأبحاث الحالية على:
- لقاحات mRNA: على غرار تقنية لقاحات كورونا، لتحفيز الجسم على إنتاج أجسام مضادة لبروتينات الفيروس السطحية.
- تعديل الجينات (CRISPR): أبحاث واعدة تهدف لقطع الحمض النووي للفيروس وهو في حالة الكمون لاستئصاله نهائياً من الخلايا.
- الأجسام المضادة أحادية النسيلة: لتوفير حماية فورية للحوامل اللواتي يتعرضن لـ الفيروس المضخم للخلايا.
خرافات شائعة حول الفيروس المضخم للخلايا
- الخرافة: “العدوى بالـ CMV تعني أنك مصاب بالإيدز”.
- الحقيقة: الفيروس يصيب الجميع، ولكن شدته تظهر فقط عند مرضى نقص المناعة.
- الخرافة: “إذا أصيبت الحامل بالفيروس، سيولد الطفل مشوهاً حتماً”.
- الحقيقة: غالبية المواليد من أمهات مصابات يولدون أصحاء، والتدخل الطبي المبكر يقلل المخاطر.
- الخرافة: “الفيروس المضخم للخلايا ينتقل عبر الهواء مثل الأنفلونزا”.
- الحقيقة: ينتقل فقط عبر التلامس المباشر مع سوائل الجسم المصابة.
نصائح ذهبية من “بوابة HAEAT الطبية” 💡
بصفتنا خبراء في الرعاية السريرية، نقدم هذه النصائح الحصرية لمواجهة الفيروس المضخم للخلايا:
- قاعدة الـ 20 ثانية: غسل اليدين بعد تغيير حفاضات الأطفال هو السلاح الأقوى ضد العدوى الأولية.
- الفحص قبل الزرع: إذا كنت مقبلاً على زراعة عضو، أصر على معرفة حالة المتبرع بخصوص الفيروس المضخم للخلايا لمناقشة الخطة الوقائية مع طبيبك.
- فحص السمع الدوري: لأي طفل تعرض للعدوى في الرحم، يجب إجراء فحص سمع كل 6 أشهر حتى سن الخامسة.
- النوم العميق: يساعد النوم في الحفاظ على مستويات “الإنترفيرون” التي تبقي الفيروس في حالة كمون دائمة.
أسئلة شائعة
كم تستمر مدة عدوى الفيروس المضخم للخلايا؟
تستمر العدوى الأولية عادة من أسبوعين إلى 6 أسابيع، ولكن الفيروس يظل موجوداً في الجسم للأبد في حالة كمون.
هل يمكن للمرأة المصابة بـ CMV إرضاع طفلها؟
نعم، بالنسبة للأطفال المكتملين، فإن فوائد الرضاعة تفوق مخاطر العدوى بـ الفيروس المضخم للخلايا، لكن يجب استشارة الطبيب في حالات الخدج.
هل يوجد لقاح متوفر حالياً؟
لا يوجد لقاح مرخص عالمياً حتى عام 2026، ولكن العديد من اللقاحات في مراحل التجارب السريرية الأخيرة.
الخاتمة
في الختام، يظل الفيروس المضخم للخلايا تحدياً طبياً يتطلب توازناً بين الوعي الوقائي والتدخل العلاجي الدقيق. من خلال اتباع توصيات مدونة حياة الطبية والالتزام ببروتوكولات النظافة الشخصية، يمكننا تقليل عبء هذا الفيروس على المجتمع وحماية الفئات الأكثر عرضة للخطر. تذكر دائماً أن المعرفة هي الخطوة الأولى نحو الشفاء التام والاستقرار الصحي.