تعد الثلاسيميا (Thalassemia) من أكثر اضطرابات الدم الوراثية تعقيداً، حيث تؤثر بشكل مباشر على قدرة الجسم على إنتاج الهيموجلوبين السليم اللازم لنقل الأكسجين إلى الأنسجة.
توضح مدونة حياة الطبية أن هذا الاضطراب يتطلب إدارة طبية دقيقة ومستمرة لضمان حياة صحية ومستقرة للمصابين، وتجنب المضاعفات الناتجة عن فقر الدم المزمن أو ترسب الحديد.
يتناول هذا الدليل الشامل من موقع حياة الطبي كل ما تحتاج معرفته حول هذا المرض، بدءاً من الميكانيكا الحيوية للخلل الجيني وصولاً إلى أحدث الابتكارات العلاجية المتاحة عالمياً.
ما هي الثلاسيميا؟
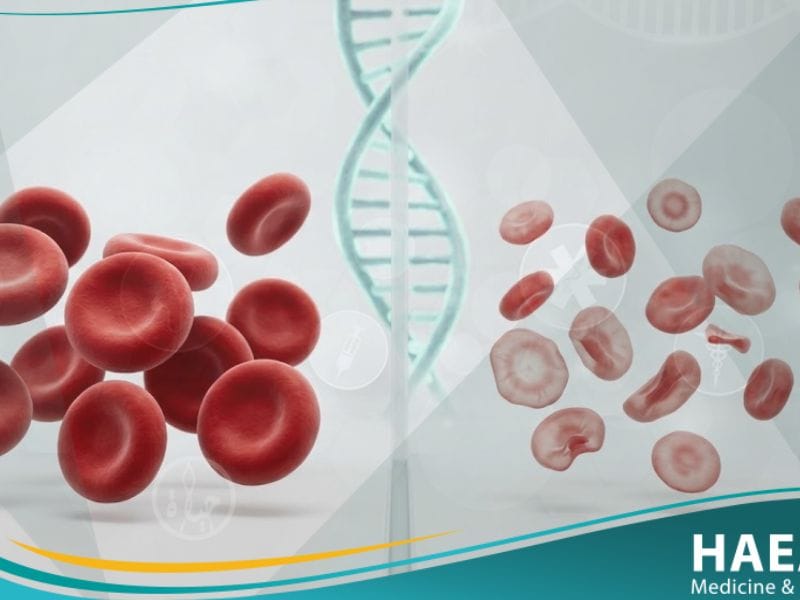
الثلاسيميا هي مجموعة من اضطرابات الدم الوراثية الناتجة عن طفرات جينية تؤدي إلى نقص في إنتاج سلاسل البروتين المكونة للهيموجلوبين في خلايا الدم الحمراء، مما يسبب تكسرها المبكر.
وفقاً لـ المعهد الوطني للصحة (NIH)، فإن هذا الخلل يؤدي إلى تدمير مفرط لخلايا الدم الحمراء، مما يسبب فقر دم مزمن تتراوح حدته بين الطفيف الذي لا يحتاج لعلاج، والمهدد للحياة الذي يستلزم نقل دم دوري.
يتكون الهيموجلوبين من أربع سلاسل بروتينية (اثنتان من ألفا واثنتان من بيتا)، وأي خلل في إنتاج هذه السلاسل يحدد نوع المرض وشدة الأعراض التي تظهر على المريض منذ الصغر.
يعمل نخاع العظم في حالات الإصابة بمرض الثلاسيميا بشكل مفرط لتعويض النقص، مما قد يؤدي إلى تمدد العظام وتشوهها، خاصة في الوجه والجمجمة، إذا لم يتم التحكم في الحالة طبياً بشكل صحيح.
من الناحية الفيزيولوجية، يؤدي نقص الهيموجلوبين إلى حرمان أعضاء الجسم الحيوية من الأكسجين الكافي، مما يسبب حالة من الإجهاد التأكسدي المزمن وتراجعاً في الوظائف الحيوية العامة للجسم.

أعراض الثلاسيميا
تتنوع الأعراض السريرية بناءً على نوع الطفرة وعدد الجينات المتضررة، وتظهر غالباً خلال العامين الأولين من العمر في الحالات الشديدة، بينما قد يتأخر اكتشاف الحالات الخفيفة لسنوات طويلة.
تتلخص العلامات الأكثر شيوعاً في النقاط التالية:
- الإرهاق المزمن والوهن العام: يشعر المريض بتعب مستمر حتى مع الراحة، نتيجة نقص الأكسجين الواصل للعضلات والدماغ.
- شحوب الجلد أو اصفراره (اليرقان): ناتج عن التحلل السريع لكريات الدم الحمراء وارتفاع مادة البيليروبين في الدم.
- تشوهات عظام الوجه: تبرز عظام الخدين والجبهة نتيجة محاولة نخاع العظم التوسع لإنتاج المزيد من الخلايا التعويضية.
- بطء النمو والتطور البدني: غالباً ما يعاني الأطفال المصابون من تأخر في الطول والوزن مقارنة بأقرانهم.
- انتفاخ وبروز البطن: يحدث عادةً بسبب تضخم الطحال والكبد اللذين يعملان كمصانع بديلة لإنتاج الدم أو تصفية الخلايا التالفة.
- البول الداكن: يشير إلى وجود الهيموجلوبين المحطم أو زيادة الحمل على الكلى نتيجة تكسر الخلايا المستمر.
- ضيق التنفس عند الجهد: عدم قدرة القلب على تلبية احتياجات الجسم من الأكسجين أثناء النشاط البدني البسيط.
- اضطرابات ضربات القلب: نتيجة محاولة القلب الضخ بسرعة أكبر لتعويض نقص ناقلات الأكسجين.
وتجدر الإشارة إلى أن مرضى الثلاسيميا الصغرى (الحاملون للمرض) قد لا يعانون من أي أعراض ظاهرة، ويتم اكتشاف حالتهم بالصدفة عند إجراء تحاليل دم روتينية تظهر صغر حجم الكريات الحمراء.

أسباب الثلاسيميا
يعود السبب الرئيسي لهذا الاضطراب إلى خلل في الحمض النووي (DNA) للخلايا المسؤولة عن إنتاج الهيموجلوبين، وهو ما ينتقل وراثياً من الآباء إلى الأبناء عبر الجينات.
تعتمد شدة الإصابة بمرض الثلاسيميا على عدد الجينات المصابة والموروثة من كلا الوالدين، وتنقسم الأسباب الجينية إلى قسمين رئيسيين:
- ثلاسيميا ألفا: تتضمن أربعة جينات (اثنان من كل والد). إذا فُقد جين واحد لا تظهر أعراض، وإذا فُقد اثنان تظهر أعراض طفيفة، أما فقدان أربعة جينات فيؤدي عادةً إلى الوفاة قبل الولادة.
- ثلاسيميا بيتا: تتضمن جينين فقط (واحد من كل والد). إذا أصيب جين واحد يعاني المريض من حالة خفيفة، أما إصابة الجينين معاً فتؤدي إلى الحالة الكبرى (Cooley’s Anemia).
وفقاً لمركز السيطرة على الأمراض والوقاية منها (CDC)، فإن الطفرات الجينية المسببة لهذا المرض تنتشر بشكل أكبر في مناطق معينة مثل حوض البحر الأبيض المتوسط، جنوب شرق آسيا، وأفريقيا.
لا يمكن أن تنتقل الثلاسيميا عبر العدوى أو التلامس، فهي مرض وراثي بحت يتطلب وجود الأبوين كحاملين للجين لكي يظهر المرض بصورته الشديدة في الأجيال القادمة.
تؤدي هذه الطفرات إلى اختلال التوازن بين سلاسل ألفا وبيتا، مما يجعل السلاسل الفائضة تترسب داخل خلايا الدم الحمراء، مما يؤدي إلى تدميرها داخل نخاع العظم أو في الطحال.
متى تزور الطبيب؟
يشير موقع حياة الطبي إلى ضرورة المتابعة الفورية عند ملاحظة علامات فقر الدم المستمر التي لا تستجيب للمكملات الغذائية التقليدية، خاصة في العائلات التي لديها تاريخ مرضي وراثي.
العلامات التحذيرية لدى البالغين
يجب على البالغين استشارة اختصاصي أمراض الدم إذا واجهوا ضيقاً مفاجئاً في التنفس، أو آلاماً في الصدر، أو إرهاقاً يعيق ممارسة الأنشطة اليومية البسيطة. كما أن ملاحظة اصفرار في بياض العين أو شحوب غير مبرر يتطلب إجراء فحص “تفريد الهيموجلوبين” فوراً.
مؤشرات الخطر عند الأطفال والرضع
بالنسبة للرضع، يجب مراقبة نمط الرضاعة والنمو؛ فإذا لاحظت الأم ضعفاً في الشهية، أو تغيراً في ملامح الوجه، أو تضخماً في منطقة البطن، فإن ذلك قد يشير إلى إصابة بمرض الثلاسيميا من النوع الشديد الذي يظهر في الشهور الأولى.
دور الذكاء الاصطناعي في الفرز الأولي
تقترح الأبحاث الحديثة استخدام تقنيات الذكاء الاصطناعي في تحليل صور الدم الكاملة (CBC) للتنبؤ باحتمالية الإصابة قبل إجراء الفحوصات الجينية المكلفة. يمكن لبرمجيات متطورة اكتشاف أنماط دقيقة في حجم وشكل الكريات قد يغفل عنها الفحص البصري التقليدي، مما يسرع من عملية التشخيص الأولي بشكل كبير.
تساعد تطبيقات المتابعة الذكية أيضاً في مراقبة مستويات الطاقة والنشاط لدى المرضى، حيث تعطي تنبيهات عند انخفاض معدلات الأكسجين أو تراجع النشاط البدني، مما يستدعي زيارة الطبيب لتعديل خطة نقل الدم.
يؤكد الخبراء أن التدخل المبكر يمنع حدوث تشوهات العظام الدائمة ويحمي الأعضاء الحيوية من التلف الناتج عن نقص الأكسجين المزمن المرتبط بمرض الثلاسيميا.
عوامل خطر الإصابة بـ الثلاسيميا
تعتمد احتمالية الإصابة بهذا الاضطراب بشكل أساسي على المحددات الجينية والعرقية، حيث تشير مدونة HAEAT الطبية إلى أن التاريخ العائلي هو المؤشر الأقوى لتحديد مستوى الخطر.
تتضمن أبرز عوامل الخطر ما يلي:
- التاريخ العائلي للإصابة: وراثة جينات الهيموجلوبين المتحورة من الأبوين هي الطريق الوحيد للإصابة؛ فإذا كان كلاهما حاملاً للمرض، تزداد احتمالية ولادة طفل مصاب بنسبة 25% في كل حمل.
- الأصول العرقية والجغرافية: ينتشر المرض بكثافة في سكان حوض البحر الأبيض المتوسط، ومنطقة الشرق الأوسط، وجنوب شرق آسيا، ودول أفريقيا جنوب الصحراء.
- زواج الأقارب: في المجتمعات التي يكثر فيها زواج الأقارب، تزداد فرص التقاء الجينات المتنحية المسببة لمرض الثلاسيميا، مما يرفع معدلات المواليد المصابين بالحالات الكبرى.
- الطفرات الجينية العشوائية: رغم ندرتها الشديدة، قد تحدث طفرات جينية جديدة في حالات فردية، إلا أن الغالبية العظمى تظل مرتبطة بالانتقال الوراثي التقليدي.
مضاعفات الثلاسيميا
تنشأ مضاعفات الثلاسيميا إما من المرض نفسه وفشل نخاع العظم، أو كنتيجة ثانوية للعلاجات الضرورية مثل عمليات نقل الدم المتكررة التي تؤدي لتراكم الحديد.
تشمل قائمة المضاعفات الأكثر تأثيراً على جودة الحياة:
- فرط حمل الحديد (Iron Overload): يؤدي نقل الدم المستمر إلى ترسب الحديد في الأعضاء الحيوية مثل القلب والكبد والغدد الصماء، مما قد يسبب فشلاً عضوياً إذا لم يتم استخلاصه.
- تضخم الطحال (Splenomegaly): يعمل الطحال بجهد مضاعف لتصفية خلايا الدم التالفة، مما يؤدي لتضخمه وزيادة فقر الدم سوءاً، وقد يتطلب الأمر استئصاله جراحياً.
- العدوى والالتهابات: تزداد عرضة المرضى للعدوى، خاصة في حالات استئصال الطحال أو نتيجة ضعف المناعة العام المرتبط بالاضطراب المزمن.
- مشاكل القلب: يعد قصور القلب الاحتقاني واضطراب النظم القلبي من الأسباب الرئيسية للوفاة في حالات الثلاسيميا الكبرى نتيجة ترسب الحديد في العضلة القلبية.
- هشاشة العظام وتشوهها: يؤدي توسع نخاع العظم للبحث عن مساحة إنتاجية إلى ترقق قشرة العظام، مما يزيد من احتمالية الكسور والآلام العظمية المزمنة.
- تأخر البلوغ واضطرابات النمو: يؤثر الحديد الزائد على الغدة النخامية، مما يعطل إفراز هرمونات النمو والهرمونات الجنسية.
الوقاية من الثلاسيميا
تعتمد استراتيجيات الوقاية من الثلاسيميا على الحد من ولادة أطفال جدد مصابين بالحالات الشديدة من خلال الفحص المبكر والتوعية المجتمعية المكثفة.
توضح مجلة حياة الطبية أن الخطوات الوقائية الفعالة تشمل:
- الفحص الطبي قبل الزواج: يعد الفحص الإلزامي للزوجين من أهم الأدوات لتحديد احتمالية انتقال المرض للأبناء وتقديم المشورة الوراثية اللازمة.
- الاستشارة الوراثية: الحصول على جلسات مع متخصصين لشرح الاحتمالات الجينية والخيارات المتاحة للزوجين الحاملين للجينات المتحورة.
- التشخيص الوراثي قبل الانغراس (PGD): استخدام تقنيات التلقيح الاصطناعي لفحص الأجنة قبل زرعها في الرحم للتأكد من سلامتها من طفرات الثلاسيميا.
- الفحص أثناء الحمل: إجراء اختبارات السائل الأمنيوسي أو عينة من مشيمة الجنين في المراحل المبكرة لتحديد ما إذا كان الجنين مصاباً بالنوع الشديد.
- حملات التوعية الوطنية: تثقيف المجتمع حول أهمية الكشف المبكر وكيفية التعايش مع الحالات البسيطة لتجنب تفاقم الخطر الجيني.
تشخيص الثلاسيميا
يتطلب التشخيص الدقيق لمرض الثلاسيميا سلسلة من الفحوصات المختبرية المتخصصة التي تفرق بينه وبين أنواع فقر الدم الأخرى مثل فقر الدم بنقص الحديد.
تشمل بروتوكولات التشخيص المعتمدة:
- تعداد الدم الكامل (CBC): يظهر انخفاضاً في مستوى الهيموجلوبين وصغراً ملحوظاً في حجم خلايا الدم الحمراء (Microcytosis).
- تفريد الهيموجلوبين (Hemoglobin Electrophoresis): الاختبار المعياري لتحديد أنواع الهيموجلوبين الموجودة (مثل HbF وHbA2) ونسبتها، مما يؤكد نوع الإصابة.
- فحص مستوى الفيريتين والحديد: للتأكد من أن فقر الدم ليس ناتجاً عن نقص الحديد، ولتقييم مخزون الحديد لدى المصابين فعلياً.
- الاختبارات الجينية (DNA Testing): الفحص الأدق الذي يحدد نوع الطفرة الجينية المحددة وعدد الجينات المصابة، وهو ضروري في حالات التخطيط للإنجاب.
- مسح العظام والأشعة: لتقييم مدى تأثر الهيكل العظمي بتوسع نخاع العظم في الحالات المتقدمة.
علاج الثلاسيميا
يتطلب علاج الثلاسيميا نهجاً متعدد التخصصات يهدف إلى الحفاظ على مستويات كافية من الهيموجلوبين مع منع تلف الأعضاء الناتج عن العلاج ذاته.
يوضح موقع HAEAT الطبي أن الخطة العلاجية تُفصل بناءً على عمر المريض وشدة الأعراض السريرية.
تعديلات نمط الحياة والرعاية المنزلية
يجب على مرضى الثلاسيميا تجنب تناول مكملات الحديد تماماً ما لم يوصِ الطبيب بخلاف ذلك. يُنصح باتباع نظام غذائي متوازن غني بحمض الفوليك (ضروري لإنتاج خلايا الدم) والحفاظ على روتين رياضي معتدل لا يرهق الجهاز التنفسي.
العلاجات الدوائية والطبية
بروتوكولات علاج البالغين (Adults)
- نقل الدم الدوري: يتم عادةً كل 2 إلى 4 أسابيع للحفاظ على مستويات الهيموجلوبين فوق 9.5 جم/ديسيلتر، مما يسمح للبالغين بممارسة حياتهم الطبيعية.
- علاجات استخلاص الحديد (Chelation Therapy): استخدام أدوية مثل (Deferasirox) أو (Deferoxamine) للتخلص من تراكم الحديد السام الناتج عن نقل الدم.
الاعتبارات الخاصة بعلاج الأطفال (Children)
- المتابعة الدقيقة للنمو: يحتاج الأطفال لجرعات مدروسة من حمض الفوليك ومراقبة مستمرة للطول والوزن وتطور العظام.
- زراعة النخاع (BMT): تعد الخيار الوحيد للشفاء التام في سن مبكرة، خاصة إذا توفر متبرع متطابق تماماً (غالباً أخ أو أخت).
التحرير الجيني CRISPR كحل جذري مستقبلي
يمثل التحرير الجيني باستخدام تقنية (CRISPR-Cas9) ثورة في علاج الثلاسيميا. تعتمد هذه التقنية على تعديل الخلايا الجذعية للمريض نفسه لتمكينها من إنتاج الهيموجلوبين الجنيني (HbF) بكميات كافية، مما قد يلغي الحاجة لنقل الدم نهائياً. أظهرت التجارب السريرية نتائج مبشرة جداً تقترب من الشفاء التام.
تقنيات استخلاب الحديد الذكية والمضخات الحديثة
تتوفر الآن مضخات ذكية متصلة بتطبيقات ذكاء اصطناعي تقوم بحساب الجرعة الدقيقة من أدوية الاستخلاص بناءً على قراءات مستمرة لمستوى الحديد ومعدل نقل الدم. هذا يقلل من الآثار الجانبية للأدوية ويضمن كفاءة أعلى في حماية القلب والكبد من التلف التراكمي المرتبط بمرض الثلاسيميا.
الطب البديل لـ الثلاسيميا
على الرغم من أن الثلاسيميا تتطلب علاجاً طبياً متخصصاً، إلا أن بعض الممارسات التكميلية قد تساعد في تخفيف الأعراض وتحسين جودة الحياة، شريطة استشارة الطبيب المختص أولاً.
تتضمن خيارات الدعم التكميلي ما يلي:
- حمض الفوليك (فيتامين B9): يساعد في بناء خلايا الدم الحمراء الجديدة ويقلل من تكسرها السريع؛ وهو مكمل أساسي لمعظم المرضى.
- عشبة القمح (Wheatgrass): تشير بعض الدراسات المحدودة إلى أنها قد تساعد في تقليل الحاجة لنقل الدم لدى بعض المصابين بمرض الثلاسيميا، لكنها لا تغني عن العلاج التقليدي.
- الشاي الأخضر والشاي الأسود: يساعد شرب الشاي مع الوجبات في تقليل امتصاص الحديد غير الهيم من الغذاء، مما يساهم في التحكم في مستويات الحديد.
- فيتامين د والكالسيوم: ضروريان جداً لحماية العظام من الهشاشة والترقق الناتج عن توسع نخاع العظم.
- ممارسات الاسترخاء (اليوجا والتأمل): تساعد في تقليل مستويات الإجهاد النفسي والألم المزمن المرتبط بالمرض.
- تجنب فيتامين ج (بجرعات عالية): قد يزيد من امتصاص الحديد من الغذاء، لذا يجب الحذر عند استخدامه، خاصة في أوقات الوجبات.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع مرض مزمن مثل الثلاسيميا تنظيماً دقيقاً للمعلومات الطبية لضمان الحصول على أفضل رعاية ممكنة خلال الزيارات الدورية.
ما الذي يمكنك فعله قبل الموعد؟
- قم بتدوين قائمة بجميع الأعراض التي شعرت بها مؤخراً، حتى تلك التي قد تبدو غير مرتبطة بفقر الدم.
- أحضر سجلاً دقيقاً لتواريخ عمليات نقل الدم الأخيرة وكمياتها.
- أعد قائمة بجميع الأدوية والمكملات الغذائية التي تتناولها حالياً.
- سجل الأسئلة التي تود طرحها على الطبيب، مثل خيارات العلاج الجديدة أو تعديل جرعات استخلاص الحديد.
ما الذي تتوقعه من الطبيب؟
سيقوم الطبيب بمراجعة نتائج فحوصات الدم الأخيرة، وتقييم حجم الطحال والكبد، ومناقشة أي تغيرات في مستويات الطاقة لديك. كما سيراجع مستويات الفيريتين للتأكد من فكاكة الحديد من الأعضاء الحيوية.
استخدام تطبيقات المتابعة الرقمية لتنظيم سجل نقل الدم
توصي بوابة HAEAT الطبية باستخدام التطبيقات الذكية التي تسمح للمرضى بتسجيل مستويات الهيموجلوبين قبل وبعد النقل، ومراقبة مواعيد أدوية الاستخلاص. تعمل هذه التطبيقات كمنبهات ذكية وتحلل البيانات لتقديم تقرير شامل للطبيب، مما يحسن من دقة التعديلات العلاجية لمرض الثلاسيميا.
مراحل الشفاء من الثلاسيميا
بما أن الثلاسيميا اضطراب وراثي مزمن، فإن مفهوم “الشفاء” يختلف باختلاف نوع التدخل الطبي المتبع.
- مرحلة الإدارة والسيطرة: في الحالات التي تعتمد على نقل الدم، تهدف هذه المرحلة إلى الحفاظ على استقرار مستويات الهيموجلوبين ومنع تراكم الحديد.
- مرحلة ما قبل زراعة النخاع: تتضمن تحضير الجسم وتثبيط المناعة لاستقبال الخلايا الجذعية الجديدة.
- مرحلة التعافي بعد الزراعة: هي المرحلة التي يبدأ فيها الجسم بإنتاج خلايا دم سليمة؛ وتتطلب متابعة دقيقة لعدة أشهر للتأكد من نجاح الانغراس.
- مرحلة المتابعة طويلة الأمد: حتى بعد الشفاء الجذري (عبر الزراعة أو العلاج الجيني)، يحتاج المريض لمتابعة حالة الأعضاء المتأثرة سابقاً بالحديد الزائد.
الأنواع الشائعة لـ الثلاسيميا
تنقسم الثلاسيميا إلى فئات رئيسية بناءً على السلسلة البروتينية المصابة وعدد الجينات المتضررة:
- ثلاسيميا ألفا (Alpha Thalassemia):
- الحامل الصامت: طفرة في جين واحد، لا أعراض.
- سمة ثلاسيميا ألفا: طفرة في جينين، فقر دم خفيف.
- مرض الهيموجلوبين H: طفرة في 3 جينات، فقر دم متوسط إلى شديد.
- موه الجنين (Hydrops Fetalis): طفرة في 4 جينات، حالة حرجة قبل الولادة.
- ثلاسيميا بيتا (Beta Thalassemia):
- الثلاسيميا الصغرى (Minor): حالة خفيفة جداً، المريض “حامل” للمرض.
- الثلاسيميا المتوسطة (Intermedia): فقر دم متوسط قد يحتاج لنقل دم أحياناً.
- الثلاسيميا الكبرى (Major): وتعرف بأنيميا كولي، تتطلب نقل دم دوري مدى الحياة.
إحصائيات الثلاسيميا وانتشارها في المنطقة العربية
تشير التقارير الصادرة عن منظمة الصحة العالمية إلى أن المنطقة العربية تعد من أعلى المناطق في معدلات انتشار جينات الثلاسيميا. ففي دول مثل المملكة العربية السعودية والإمارات العربية المتحدة ومصر، تتراوح نسبة حاملي المرض بين 2% إلى 5% من السكان في بعض المناطق. وتؤكد البيانات أن برامج الفحص الإلزامي قبل الزواج في دول الخليج ساهمت بشكل جذري في خفض معدلات ولادة الحالات الكبرى بنسبة تصل إلى 60% خلال العقد الماضي.
النظام الغذائي والمكملات الممنوعة لمرضى الثلاسيميا
يجب أن يكون النظام الغذائي لمريض الثلاسيميا مصمماً بعناية فائقة لتجنب مخاطر تسمم الحديد.
- الأطعمة الممنوعة (أو الواجب تقليلها): اللحوم الحمراء، الكبد، الحبوب المدعمة بالحديد، والسبانخ بجرعات كبيرة.
- المكملات الممنوعة: يجب تجنب أي فيتامينات تحتوي على عنصر الحديد نهائياً.
- الأطعمة الموصى بها: الخضروات الورقية (باستثناء السبانخ)، الفواكه، ومنتجات الألبان الغنية بالكالسيوم.
- دور الكالسيوم: يعد حيوياً لمنع هشاشة العظام التي يسببها توسع النخاع العظمي نتيجة مرض الثلاسيميا.
التأثير النفسي والاجتماعي للتعايش مع الثلاسيميا
التعايش مع مرض مزمن يتطلب قوة نفسية هائلة. يواجه مرضى الثلاسيميا تحديات تتعلق بصورة الجسد (بسبب تشوهات العظام أو القامة القصيرة) والقلق من المستقبل. تشدد “مجلة حياة الطبية” على أهمية الانضمام لمجموعات الدعم النفسي، حيث يساعد تبادل الخبرات في تقليل الشعور بالعزلة والاكتئاب، ويعزز الالتزام بالبروتوكول العلاجي المجهد.
مستقبل علاج الثلاسيميا: العلاج الجيني والتقنيات الواعدة
يتجه العلم اليوم نحو “العلاج لمرة واحدة”. تهدف أبحاث التحرير الجيني إلى إصلاح الطفرة في الخلايا الجذعية للمريض وإعادتها له، مما يجعله قادراً على إنتاج هيموجلوبين طبيعي. كما يتم تطوير أدوية جديدة تعمل على تحسين جودة خلايا الدم الحمراء وإطالة عمرها داخل الدورة الدموية، مما يقلل من وتيرة الحاجة لعمليات النقل المجهدة المرتبطة بمرض الثلاسيميا.
خرافات شائعة حول الثلاسيميا
- الخرافة:الثلاسيميا مرض معدٍ يمكن أن ينتقل باللمس أو المعيشة المشتركة.
- الحقيقة: هو مرض وراثي بحت ينتقل عبر الجينات من الآباء للأبناء فقط.
- الخرافة: تناول الكبدة واللحوم الحمراء يعالج هذا النوع من الأنيميا.
- الحقيقة: في هذا المرض، الحديد الزائد هو العدو الأول؛ وتناول هذه الأطعمة يزيد الحالة سوءاً.
- الخرافة: مريض الحالات الكبرى لا يمكنه الزواج أو الإنجاب.
- الحقيقة: مع العلاج الحديث والاستشارة الوراثية، يمكن للمرضى الزواج وتكوين أسر وإنجاب أطفال أصحاء (عبر تقنيات الفحص الوراثي).
نصائح ذهبية من “مدونة حياة الطبية” 💡
- الالتزام الصارم: لا تفوت مواعيد نقل الدم أو جرعات أدوية الاستخلاص؛ فالتراكم البسيط للحديد اليوم يسبب أضراراً لا يمكن إصلاحها غداً.
- النشاط البدني الذكي: مارس المشي السريع أو السباحة، وتجنب الرياضات العنيفة التي قد تعرض عظامك الهشة للكسر.
- الترطيب المستمر: شرب الماء بكثرة يساعد الكلى في معالجة نواتج تكسر خلايا الدم بكفاءة.
- الفحوصات الدورية للقلب والكبد: اجعل فحص “الرنين المغناطيسي T2*” روتيناً سنوياً لتقييم ترسب الحديد في القلب.
أسئلة شائعة
هل يمكن للمصاب بالثلاسيميا الصغرى ممارسة الرياضة؟
نعم، يمكنهم ممارسة كافة أنواع الرياضات بشكل طبيعي تماماً، وغالباً ما لا تظهر عليهم أي أعراض تمنعهم من عيش حياة رياضية نشطة.
ما هو متوسط العمر المتوقع لمريض الثلاسيميا الكبرى؟
بفضل بروتوكولات نقل الدم الحديثة وأدوية استخلاص الحديد الفعالة، أصبح المرضى يعيشون لعقود طويلة (حتى الخمسينيات والستينيات وما بعدها) ويمارسون وظائفهم بشكل طبيعي.
هل يغني تناول حمض الفوليك عن نقل الدم؟
لا، حمض الفوليك هو عامل مساعد فقط لإنتاج الخلايا، ولكنه لا يعوض النقص الشديد الناتج عن تكسر سلاسل الهيموجلوبين في حالات مرض الثلاسيميا الشديدة.
الخاتمة
في الختام، يظل الوعي الوراثي والفحص المبكر هما حجر الزاوية في مواجهة الثلاسيميا. إن التطور التكنولوجي الهائل في مجال التحرير الجيني واستخلاص الحديد يمنح أملاً جديداً لملايين المصابين حول العالم. نحن في بوابة HAEAT الطبية نؤمن بأن الإدارة الذكية للمرض والالتزام بالتوصيات الطبية هما المفتاح لحياة مليئة بالصحة والنشاط.