تُعد عملية أكسدة الأحماض الدهنية (Fatty-acid beta-oxidation) المحرك الحيوي الأساسي لإنتاج الطاقة في جسم الإنسان خلال فترات الصيام أو المجهود البدني الشاق. عندما يعجز الجسم عن تفكيك الدهون لتحويلها إلى وقود، تظهر مجموعة من الاضطرابات الأيضية المعقدة التي قد تهدد الحياة إذا لم تُشخص مبكراً.
يشير موقع حياة الطبي إلى أن هذه الاضطرابات الجينية تعيق قدرة الخلايا على استخدام الدهون كمصدر بديل للجلوكوز، مما يؤدي إلى تراكم الأحماض الدهنية السامة في الأعضاء الحيوية مثل القلب والكبد. إن فهم الآلية الكيميائية الحيوية وراء هذا الخلل هو الخطوة الأولى لتجنب الأزمات الاستقلابية الحادة.
ما هي أكسدة الأحماض الدهنية؟
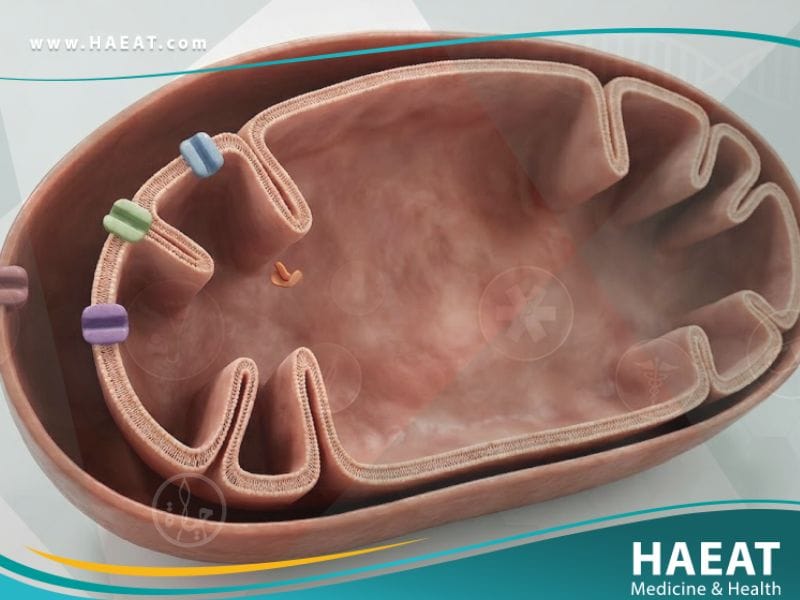
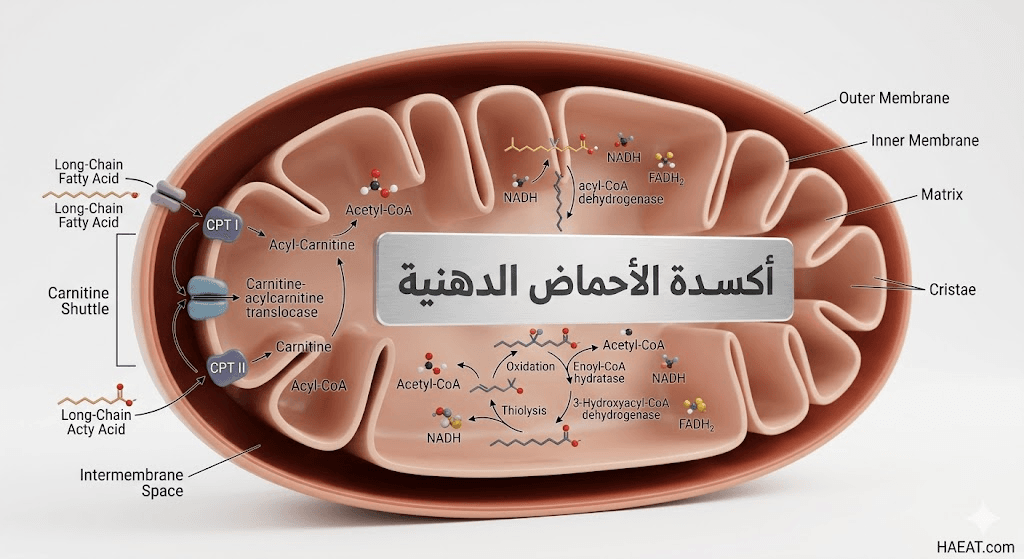
أكسدة الأحماض الدهنية هي مسار استقلابي كيميائي حيوي يحدث داخل الميتوكوندريا، حيث يتم تكسير سلاسل الأحماض الدهنية الطويلة إلى جزيئات أصغر تسمى “أسيتيل كو-أ” (Acetyl-CoA) لإنتاج الطاقة. هذه العملية حيوية جداً لبقاء الأعضاء التي تستهلك طاقة عالية، مثل عضلة القلب والعضلات الهيكلية، في حالة عمل مستمر.
وفقاً لأبحاث منشورة في دورية (The Lancet)، فإن هذه الدورة تتكون من أربع خطوات إنزيمية متتالية تُعرف بـ “بيتا أكسدة”. في الحالات الطبيعية، يفرز الجسم إنزيمات محددة لكل طول من سلاسل الدهون (قصيرة، متوسطة، طويلة، وطويلة جداً). يوضح موقع HAEAT الطبي أن أي نقص في هذه الإنزيمات يؤدي إلى توقف المسار، مما يسبب انخفاضاً حاداً في مستويات السكر في الدم وزيادة مفرطة في حموضة الأنسجة.
أعراض اضطرابات أكسدة الأحماض الدهنية
تتفاوت حدة الأعراض بناءً على نوع النقص الإنزيمي، لكنها تشترك جميعاً في ظهورها المفاجئ عند تعرض الجسم لضغط جسدي أو صيام طويل. تشير مدونة HAEAT الطبية إلى أن العلامات السريرية قد تظهر في غضون الساعات الأولى من الولادة أو تتأخر حتى سن البلوغ.
- نوبات نقص السكر غير الكيتوني: وهي السمة الأبرز، حيث ينخفض سكر الدم دون ظهور الأجسام الكيتونية التي تعوض نقص الطاقة.
- الإرهاق العضلي الشديد: الشعور بوهن وكتل عضلية مؤلمة بعد ممارسة تمارين رياضية بسيطة.
- تضخم الكبد (Hepatomegaly): نتيجة تراكم الدهون غير المؤكسدة داخل خلايا الكبد، مما يغير وظائفه الحيوية.
- اعتلال عضلة القلب: ظهور ضيق في التنفس وتورم الأطراف نتيجة ضعف قدرة القلب على ضخ الدم بفعالية.
- الخمول وفقدان الوعي: نوبات من النعاس الشديد التي قد تتطور إلى غيبوبة استقلابية كاملة.
- آلام البطن والقيء: خاصة بعد الانقطاع عن الطعام لفترة تتجاوز 8 ساعات.
- تغير لون البول: قد يميل إلى اللون الداكن (لون الشاي) نتيجة تحلل العضلات وإفراز الميوجلوبين.

أسباب خلل أكسدة الأحماض الدهنية
يعود السبب الجذري لهذا الخلل إلى طفرات وراثية تنتقل عبر نمط “وراثة جسدية متنحية”، مما يعني أن الطفل يجب أن يرث نسخة من الجين الطافر من كلا الوالدين ليصاب بالمرض. تؤكد مجلة حياة الطبية أن هذه الطفرات تؤدي إلى غياب أو ضعف نشاط الإنزيمات المسؤولة عن تحطيم الدهون.
- نقص إنزيم (MCAD): وهو السبب الأكثر شيوعاً، حيث يعجز الجسم عن تكسير الدهون متوسطة السلسلة، مما يسبب أزمات مفاجئة.
- نقص إنزيم (VLCAD): يؤثر على الأحماض الدهنية طويلة السلسلة جداً، ويرتبط غالباً بمشاكل قلبية حادة.
- خلل ناقل الكارنيتين: الكارنيتين هو “المكوك” الذي ينقل الدهون إلى داخل الميتوكوندريا؛ أي نقص فيه يعطل عملية أكسدة الأحماض الدهنية بالكامل.
- نقص البروتين الثلاثي الوظائف (TFP): حالة نادرة ومعقدة تؤثر على ثلاث خطوات إنزيمية في آن واحد.
- عوامل بيئية محفزة: الصيام، العدوى الفيروسية، الحمى، والإجهاد البدني هي محفزات تؤدي لظهور الأعراض الكامنة.
متى تزور الطبيب؟
إن التوقيت هو العامل الفاصل في إنقاذ حياة المصاب باضطرابات التمثيل الغذائي. توضح بوابة HAEAT الطبية أن تجاهل العلامات البسيطة قد يؤدي إلى تلف دماغي دائم نتيجة نقص الطاقة المزمن في الخلايا العصبية.
الحالات الحرجة لدى البالغين
يجب استشارة الطبيب فوراً إذا لاحظت ضعفاً عضلياً مفاجئاً بعد الصيام أو ممارسة الرياضة، خاصة إذا ترافق ذلك مع بول داكن. البالغون الذين يعانون من نوبات متكررة من الدوار أو “ضبابية الدماغ” عند تأخير الوجبات يحتاجون إلى فحص استقلابي شامل لاستبعاد وجود نقص جزئي في الإنزيمات.
العلامات التحذيرية لدى الأطفال والرضع
تُعد اضطرابات أكسدة الأحماض الدهنية من الأسباب الخفية وراء متلازمة موت الرضع المفاجئ (SIDS). يجب طلب الرعاية الطارئة إذا كان الرضيع:
- يرفض الرضاعة لفترات طويلة ويبدو خاملاً بشكل غير طبيعي.
- يعاني من قيء مستمر يصاحبه برودة في الأطراف.
- يظهر عليه اصفرار في الجلد (يرقان) لا يزول مع الوقت.
متى يكون الفحص الجيني المبكر ضرورة لا غنى عنها؟
توصي المعايير الطبية الحديثة (وفقاً لـ NIH) بإجراء تسلسل جيني مستهدف في الحالات التالية:
- وجود تاريخ عائلي لوفيات رضع غير مفسرة.
- عند التخطيط للزواج في عائلات لديها إصابات معروفة بالتمثيل الغذائي.
- إذا أظهر فحص حديثي الولادة (مسحة الكعب) نتائج غير حاسمة أو “إيجابية كاذبة” متكررة.
- في حالات الحمل التي تعاني فيها الأم من متلازمة (HELLP) أو الكبد الدهني الحاد أثناء الحمل، حيث قد يكون الجنين مصاباً بخلل في أكسدة الأحماض الدهنية.
عوامل خطر الإصابة بـ أكسدة الأحماض الدهنية
تعتبر اضطرابات أكسدة الأحماض الدهنية حالات وراثية بالدرجة الأولى، حيث تلعب الجينات الدور المحوري في تحديد كفاءة التمثيل الغذائي للدهون. تشير التقارير الصادرة عن (Cleveland Clinic) إلى أن عوامل الخطر لا تتعلق بنمط الحياة بقدر ما تتعلق بالتركيبة البيولوجية الموروثة.
- التاريخ العائلي: وجود شقيق أو قريب من الدرجة الأولى مصاب بأحد أنواع خلل الأكسدة يزيد من احتمالية حمل الجين الطافر.
- زواج الأقارب: ترتفع نسب الإصابة في المجتمعات التي يكثر فيها زواج الأقارب، نظراً لأن هذه الأمراض تتبع نمط الوراثة المتنحية.
- الأمراض الفيروسية الحادة: تعمل العدوى (مثل الإنفلونزا أو النزلات المعوية) كمحفز مباشر للأعراض، حيث تضع الجسم في حالة إجهاد تزيد الطلب على الطاقة.
- فترات الصيام الطويلة: الانقطاع عن الطعام لأكثر من 8 إلى 12 ساعة يضع ضغطاً هائلاً على نظام أكسدة الأحماض الدهنية المحدود لدى المصابين.
- العرق والجغرافيا: تلاحظ بعض الدراسات (وفقاً لـ Johns Hopkins) انتشار نقص إنزيم (MCAD) بشكل أكبر لدى المنحدرين من أصول شمال أوروبا.
مضاعفات أكسدة الأحماض الدهنية
إذا لم يتم التحكم في مستويات الطاقة وتجنب المحفزات، يمكن أن تؤدي اضطرابات أكسدة الأحماض الدهنية إلى تدهور سريع في الوظائف الحيوية. تكمن الخطورة في أن الخلايا “تتضور جوعاً” رغم وجود مخزون دهني هائل لا يمكن استغلاله.
- انحلال الربيدات (Rhabdomyolysis): تحلل سريع للأنسجة العضلية يؤدي إلى إطلاق بروتينات سامة في مجرى الدم، مما قد يسبب فشلاً كلوياً حاداً.
- الفشل الكبدي الصاعق: تراكم الدهون داخل الكبد يعطل قدرته على إزالة السموم وتنظيم سكر الدم، مما يؤدي إلى تراكم الأمونيا.
- اعتلال الدماغ الاستقلابي: نقص الوقود عن الدماغ يسبب تورماً في الأنسجة العصبية، مما قد يؤدي إلى نوبات صرع أو غيبوبة.
- الموت المفاجئ: خاصة لدى الرضع، حيث يمكن أن تتوقف عضلة القلب فجأة نتيجة نقص الطاقة الحاد خلال النوم (نقص السكر الليلي).
- تليف الأعصاب الطرفية: في حالات معينة مثل (LCHAD)، قد يعاني المرضى من فقدان تدريجي للإحساس أو الرؤية نتيجة تلف الأنسجة العصبية الحساسة.
الوقاية من أكسدة الأحماض الدهنية
تعتمد الوقاية في هذا السياق على “الإدارة الاستباقية” وليس منع المرض جينياً، حيث تهدف الإستراتيجيات إلى منع حدوث الأزمات الاستقلابية التي تعطل عملية أكسدة الأحماض الدهنية.
- تجنب الصيام التام: القاعدة الذهبية هي عدم البقاء دون طعام لفترات طويلة، خاصة للأطفال (لا تتجاوز 4-6 ساعات حسب العمر).
- النظام الغذائي الغني بالكربوهيدرات: ضمان توفر الجلوكوز كمصدر دائم للطاقة لتقليل الاعتماد على حرق الدهون.
- استخدام زيت (MCT): في بعض الحالات، يمكن استخدام الدهون متوسطة السلسلة التي تتجاوز بعض العقبات الإنزيمية في مسار أكسدة الأحماض الدهنية.
- التخطيط للتمارين الرياضية: تناول وجبة خفيفة غنية بالنشويات قبل وبعد أي مجهود بدني لمنع إجهاد العضلات.
- الفحص الجيني قبل الزواج: يعد وسيلة وقائية فعالة للحد من انتقال الجينات المسؤولة عن هذه الاضطرابات للأجيال القادمة.
تشخيص أكسدة الأحماض الدهنية
تطورت تقنيات التشخيص بشكل مذهل، حيث يتم الاعتماد الآن على “البصمة الكيميائية” للأحماض الدهنية في الدم. توضح مدونة حياة الطبية أن التشخيص المبكر خلال الأيام الأولى من الولادة ينقذ آلاف الرضع سنوياً من الإعاقات الدائمة.
- فحص حديثي الولادة (Newborn Screening): استخدام تقنية (Tandem Mass Spectrometry) لتحليل قطرة دم من كعب الرضيع للكشف عن مستويات “الأسيل كارنيتين”.
- تحليل ملف الأسيل كارنيتين: يعطي خريطة دقيقة لنوع الإنزيم المفقود بناءً على طول سلاسل الدهون المتراكمة في الدم.
- اختبار الأحماض العضوية في البول: يساعد في الكشف عن الكيتونات غير الطبيعية أو نواتج التمثيل الغذائي غير المكتملة.
- الفحص الجيني الجزئي: تحديد الطفرة المحددة في الجينات (مثل جين ACADM) لتأكيد التشخيص وتحديد البروتوكول العلاجي.
- اختبار تحفيز الصيام (تحت إشراف طبي): في حالات نادرة جداً ومراقبة، لتقييم استجابة الجسم لنقص الوقود (يتم تجنبه غالباً لخطورته).
علاج أكسدة الأحماض الدهنية
لا يوجد “شفاء” جيني نهائي حتى الآن، لكن العلاج يركز على الالتفاف حول العقدة الإنزيمية وتوفير مصادر طاقة بديلة. الهدف هو الحفاظ على حالة الاستقرار الأيضي ومنع تفعيل مسار أكسدة الأحماض الدهنية المعطل.
الإدارة الغذائية ونمط الحياة
يُشكل النظام الغذائي حجر الزاوية في العلاج؛ حيث يتم تقليل الدهون الكلية وزيادة الكربوهيدرات المعقدة. يُنصح بتناول وجبات صغيرة متفرقة، مع استخدام “نشا الذرة غير المطهو” (Uncooked Cornstarch) قبل النوم لتوفير إطلاق بطيء ومستمر للجلوكوز طوال الليل.
المكملات والأدوية (بروتوكولات دقيقة)
- L-Carnitine: يعمل كمنظف للميتوكوندريا، حيث يرتبط بالأحماض الدهنية السامة ويساعد الجسم على طرحها في البول.
- مكملات الريبوفلافين (فيتامين B2): تعمل كعامل مساعد لبعض الإنزيمات في عملية أكسدة الأحماض الدهنية، مما يحسن من كفاءتها المحدودة.
إدارة البالغين
التركيز على تجنب “الكيتو دايت” تماماً، والحفاظ على مستويات السكر مستقرة أثناء ممارسة العمل أو الرياضة، مع حمل سوائل سكرية دائماً للطوارئ.
الرعاية الخاصة بالأطفال والرضع
يتطلب الأمر تغذية عبر الأنبوب الأنفي المعدي في بعض الحالات لضمان عدم انقطاع الطاقة ليلاً، مع مراقبة صارمة أثناء الإصابة بأي حمى بسيطة.
دور الـ Triheptanoin (UX007) كعلاج ثوري حديث
يُعد عقار (Triheptanoin) ثورة في علاج اضطرابات أكسدة الأحماض الدهنية طويلة السلسلة (LC-FAOD). يعمل هذا الزيت الاصطناعي على توفير جزيئات كربونية تدخل مباشرة في دورة “كريبس” (Krebs Cycle)، متجاوزةً تماماً الإنزيمات المفقودة، مما يقلل بشكل كبير من نوبات دخول المستشفى واعتلال عضلة القلب.
بروتوكول الطوارئ المنزلي أثناء العدوى البسيطة
عند إصابة المريض ببرد أو قيء، يجب تفعيل خطة الطوارئ فوراً:
- إعطاء سوائل غنية بالجلوكوز (مثل محلول الجفاف بتركيز سكري عالٍ).
- إذا لم يستطع المريض الاحتفاظ بالسوائل لمدة تزيد عن ساعتين، يجب التوجه فوراً للمستشفى للحصول على الجلوكوز الوريدي بتركيز 10% (D10).
- تجنب استخدام الأدوية التي تعتمد على التمثيل الغذائي الدهني (مثل بعض أنواع الإيبوبروفين في جرعات عالية دون استشارة).

الطب البديل لأكسدة الأحماض الدهنية
في سياق اضطرابات التمثيل الغذائي، يجب التعامل مع الطب البديل بحذر شديد؛ حيث أن أي مادة تتدخل في عمل الكبد أو الميتوكوندريا قد تعطل مسار أكسدة الأحماض الدهنية الضعيف أصلاً. ومع ذلك، هناك مكملات داعمة أثبتت فعاليتها سريرياً كعوامل مساعدة (Co-factors).
- مرافق الإنزيم Q10: يساعد في تحسين كفاءة سلسلة نقل الإلكترونات داخل الميتوكوندريا، مما يعزز إنتاج الطاقة الكلي.
- الريبوفلافين (B2): يُعد أساسياً لعمل إنزيمات “الأسيل كو-أ ديهيدروجيناز” المشاركة في عملية أكسدة الأحماض الدهنية.
- البيوتين وفيتامينات B المعقدة: تلعب دوراً ثانوياً في دعم المسارات الاستقلابية الموازية لتقليل العبء على حرق الدهون.
- تجنب الأعشاب المدرة للبول: مثل الهندباء بجرعات عالية، لأنها قد تسبب الجفاف الذي يحفز الأزمات الأيضية.
- الوخز بالإبر: قد يساعد في تخفيف الآلام العضلية الناتجة عن انحلال الربيدات البسيط، لكنه لا يعالج الخلل الإنزيمي.
الاستعداد لموعدك مع الطبيب
نظراً لندرة اضطرابات أكسدة الأحماض الدهنية، فإن التحضير الجيد للموعد مع أخصائي التمثيل الغذائي (Biochemical Geneticist) يضمن الحصول على أفضل خطة رعاية.
ماذا تفعل قبل الموعد؟
يجب الاحتفاظ بـ “سجل غذائي” دقيق لمدة 3 أيام، يوضح فترات الصيام ونوعية الوجبات، مع تدوين أي نوبات إرهاق أو تغيير في لون البول. كما يُنصح بإحضار نتائج “فحص حديثي الولادة” الأصلي وأي سجلات وراثية للعائلة.
ماذا تتوقع من أخصائي التمثيل الغذائي؟
سيقوم الطبيب بطلب تحاليل “الأسيل كارنيتين” المتقدمة وقد يقترح إجراء اختبار جيني (Whole Exome Sequencing) إذا كانت الأعراض غير نمطية. سيفحص أيضاً حجم الكبد وقوة العضلات الهيكلية للتأكد من عدم وجود ضرر صامت ناتج عن خلل أكسدة الأحماض الدهنية.
قائمة الأسئلة الحرجة حول “الحمل وإمكانية توريث المرض”
- ما هي احتمالية إصابة أطفالي المستقبليين بخلل في أكسدة الأحماض الدهنية إذا كان شريك حياتي حاملاً للجين؟
- هل توجد تقنيات تشخيص وراثي قبل الانغراس (PGD) لمنع انتقال الطفرة؟
- كيف تؤثر التغيرات الهرمونية أثناء الحمل على استقراري الأيضي؟
مراحل الشفاء من أكسدة الأحماض الدهنية
بما أن هذه الحالات مزمنة وجينية، فإن مفهوم “الشفاء” يشير إلى “الاستقرار الاستقلابي الطويل” والقدرة على ممارسة حياة طبيعية دون نوبات دخول مستشفى.
- مرحلة التثبيت (الصفر): تبدأ فور التشخيص، وتهدف لإيقاف أي هدم عضلي وتعويض نقص السكر الوريدي.
- مرحلة التكيف الغذائي: تستغرق من 3-6 أشهر، حيث يتعلم المريض أو الأهل حساب حصص الدهون والنشويات بدقة لمنع تحفيز أكسدة الأحماض الدهنية.
- مرحلة الاستقرار المستدام: وصول المريض لسنوات دون أزمات حادة، مع نمو طبيعي للطول والوزن وتطور حركي سليم.
- مرحلة المراقبة الدورية: إجراء فحوصات وظائف الكبد والقلب كل 6-12 شهراً للتأكد من عدم وجود مضاعفات تراكمية.
الأنواع الشائعة لأكسدة الأحماض الدهنية
تختلف الاضطرابات بناءً على “طول السلسلة” الدهنية التي يعجز الجسم عن معالجتها، ولكل نوع بروتوكوله الخاص.
- نقص MCAD: العجز عن أكسدة الدهون متوسطة السلسلة؛ هو الأكثر انتشاراً والأسهل في الإدارة عبر تجنب الصيام فقط.
- نقص VLCAD: يؤثر على الدهون طويلة السلسلة جداً، ويتطلب حمية صارمة منخفضة الدهون مع استخدام زيوت خاصة (MCT oil).
- نقص LCHAD: نوع معقد يرتبط بمشاكل في شبكية العين والكبد، ويتطلب مراقبة دقيقة لمستويات الدهون الثلاثية.
- نقص CPT II: يؤثر على دخول الدهون للميتوكوندريا؛ يظهر غالباً كآلام عضلية شديدة وبول داكن لدى المراهقين والبالغين.
التأثير النفسي والاجتماعي للأمراض الاستقلابية النادرة
يعيش مرضى اضطراب أكسدة الأحماض الدهنية وعائلاتهم تحت ضغط نفسي مستمر يُعرف بـ “قلق الصيام”. فالخوف الدائم من تأخر وجبة أو إصابة الطفل بالقيء يخلق حالة من التأهب العصبي. اجتماعياً، يواجه الأطفال صعوبات في المشاركة في الأنشطة المدرسية أو الرحلات التي تتطلب مجهوداً بدنياً طويلاً، مما يتطلب دعماً نفسياً تخصصياً لتعزيز الثقة بالنفس وتجنب الشعور بـ “الاختلاف المرضي”.
التغذية العلاجية: جدول حصص الماكروز لمرضى خلل الأكسدة
يتطلب تحسين عملية التمثيل الغذائي توزيعاً دقيقاً للمغذيات الكبيرة (Macros) لتقليل العبء على مسار أكسدة الأحماض الدهنية:
| العنصر الغذائي | النسبة المئوية الموصى بها | ملاحظات هامة |
| الكربوهيدرات | 60% – 70% | التركيز على الكربوهيدرات المعقدة (الشوفان، الأرز البني). |
| البروتينات | 10% – 15% | ضرورية لترميم العضلات ومنع الهدم البروتيني. |
| الدهون الكلية | 15% – 20% | يجب أن تكون من مصادر محددة (تجنب الدهون المشبعة). |
| زيت MCT | حسب الجرعة الطبية | يُحسب كجزء من حصة الدهون اليومية في أنواع معينة. |
الإحصائيات العالمية ومعدلات الانتشار
تُشير البيانات المستقاة من (CDC) و (The Lancet) إلى أن معدل الإصابة الإجمالي باضطرابات أكسدة الأحماض الدهنية يبلغ حوالي 1 من كل 5,000 إلى 10,000 مولود حي عالمياً. يُعد نقص (MCAD) هو الأكثر انتشاراً، خاصة في المجتمعات الغربية، بينما تزداد نسب الأنواع الأخرى في مناطق زواج الأقارب. وبفضل الفحص الشامل لحديثي الولادة، انخفضت معدلات الوفيات المفاجئة بنسبة تزيد عن 70% في العقدين الأخيرين.
النظرة المستقبلية: العلاج الجيني ومستقبل مرضى FAODs
يتجه العلم الآن نحو “العلاج بالرنا المرسال” (mRNA therapy) و “تحرير الجينات” (CRISPR) لتصحيح الخلل الإنزيمي في الكبد بشكل دائم. الأبحاث الجارية في (Mass General) تهدف إلى زرع خلايا كبدية معدلة تستطيع القيام بـ أكسدة الأحماض الدهنية بشكل طبيعي، مما قد يعني مستقبلاً عدم الحاجة للالتزام الصارم بالحمية الغذائية أو تجنب الصيام.
خرافات شائعة حول أكسدة الأحماض الدهنية
- الخرافة: “نقص السكر يعني تناول السكر فقط”.
- الحقيقة: تناول السكر البسيط يرفع السكر بسرعة ثم يخفضه؛ الحل هو الكربوهيدرات المعقدة التي تضمن استقرار الطاقة.
- الخرافة: “الرياضة ممنوعة تماماً لهؤلاء المرضى”.
- الحقيقة: الرياضة مسموحة بل ومفيدة، بشرط التخطيط الدقيق للوجبات وتجنب الوصول لمرحلة الإجهاد الشديد.
- الخرافة: “هذا المرض يختفي مع الكبر”.
- الحقيقة: الخلل الجيني في أكسدة الأحماض الدهنية يبقى مدى الحياة، لكن البالغين يتعلمون إدارة أجسامهم بشكل أفضل.
نصائح ذهبية من “مدونة حياة الطبية” 💡
- قاعدة “وجبة الطوارئ”: يجب أن يحمل المريض دائماً (في حقيبته أو سيارته) مصدراً سريعاً للجلوكوز مثل أقراص الجلوكوز أو عصير مركز.
- سوار التعريف الطبي: ارتدِ دائماً سواراً يوضح نوع اضطراب أكسدة الأحماض الدهنية الذي تعاني منه وفصيلة دمك وتنبيه “الجلوكوز الوريدي عند الطوارئ”.
- التواصل مع المدرسة: تأكد من أن المعلمين والممرضة المدرسية يعرفون خطورة تأخير وجبة الغداء أو إجهاد الطفل في حصة التربية البدنية.
- تجنب “الصيام المتقطع”: مهما كانت صيحات النظام الغذائي منتشرة، فإن الصيام المتقطع أو الكيتو قد يكون “قاتلاً” لمن لديه خلل في الأكسدة.
أسئلة شائعة (PAA)
هل يمكن لمريض اضطراب أكسدة الأحماض الدهنية السفر لمسافات طويلة؟
نعم، لكن يتطلب الأمر تخطيطاً دقيقاً. يجب توفير وجبات خفيفة كل ساعتين، والحصول على خطاب طبي باللغة الإنجليزية يوضح الحالة للسماح بحمل السوائل الطبية والوجبات الخاصة عبر أمن المطارات.
هل تؤثر أكسدة الأحماض الدهنية على الذكاء؟
إذا تم التشخيص مبكراً وتجنب الأزمات الاستقلابية (التي تسبب نقص الأكسجين والوقود عن الدماغ)، فإن الأطفال المصابين ينمون بمستويات ذكاء طبيعية تماماً ويتفوقون دراسياً.
ما هي الفواكه المسموحة في هذه الحمية؟
جميع الفواكه مسموحة لأنها غنية بالكربوهيدرات الطبيعية (الفركتوز) وقليلة الدهون، وهي مصدر ممتاز للطاقة السريعة لمنع تنشيط مسار أكسدة الأحماض الدهنية.
الخاتمة
تظل أكسدة الأحماض الدهنية واحدة من أكثر العمليات الحيوية تعقيداً وأهمية في جسم الإنسان. ورغم أن الاضطرابات المرتبطة بها تمثل تحدياً كبيراً، إلا أن العلم الحديث وفر أدوات تشخيصية وعلاجية جعلت من التعايش معها أمراً ممكناً وبجودة حياة عالية. إن الالتزام بالحمية الغذائية والفهم العميق لمحفزات الأزمات هما السلاح الأقوى لحماية الجسم من مخاطر نقص الطاقة.