يُعد ضمور النخاع الشوكي أحد أكثر الأمراض الوراثية تعقيداً التي تؤثر على الجهاز العصبي العضلي، مما يسبب تراجعاً تدريجياً في القدرات الحركية الأساسية لدى المصابين.
نحن في “مدونة حياة الطبية” ندرك حجم القلق الذي يحيط بهذا التشخيص، لذا نقدم هذا الدليل التحليلي الشامل المبني على أحدث الأبحاث السريرية العالمية لعام 2026.
تعتمد قوة هذا الدليل على دمج المعرفة الطبية العميقة بالحلول العملية، لمساعدة العائلات والمرضى على فهم طبيعة هذا الاضطراب الجيني وكيفية مواجهته بأحدث الوسائل التقنية.
ما هو ضمور النخاع الشوكي؟
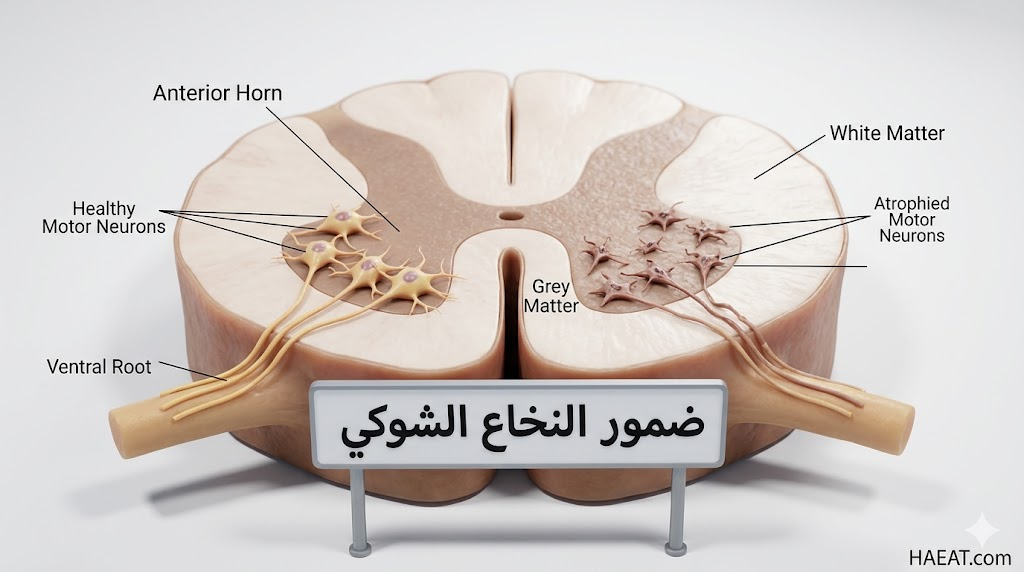
يُعرف ضمور النخاع الشوكي (Spinal Muscular Atrophy) بأنه اضطراب وراثي نادر ناتج عن فقدان الخلايا العصبية الحركية في الحبل الشوكي وجذع الدماغ، مما يؤدي إلى وهن عضلي شديد.
يشير “موقع حياة الطبي” إلى أن هذا المرض يمنع وصول الإشارات العصبية من الدماغ إلى العضلات، مما يتسبب في ضمورها وفقدان القدرة على التحكم في الحركة أو التنفس.
وفقاً للمعهد الوطني للاضطرابات العصبية والسكتة الدماغية (NINDS)، فإن الخلل الجيني الأساسي يكمن في نقص بروتين معين ضروري لبقاء هذه الخلايا العصبية الحركية على قيد الحياة.
أعراض ضمور النخاع الشوكي
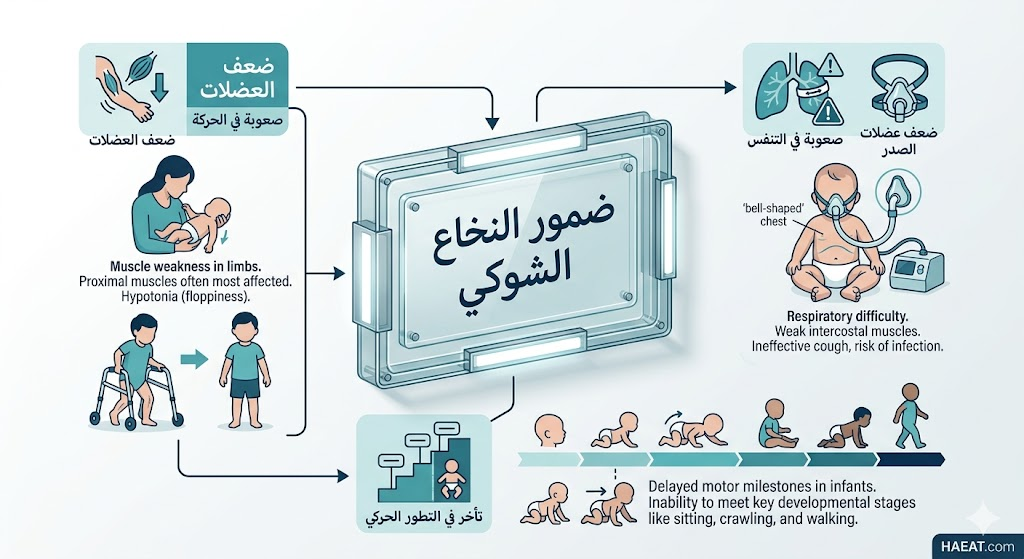
تتفاوت أعراض ضمور النخاع الشوكي بشكل كبير بناءً على نوع المرض والعمر الذي بدأت فيه الخلايا العصبية بالتدهور، وتتلخص أهم العلامات السريرية في القائمة التالية:
- الضعف العضلي المتماثل: يبدأ الضعف عادة في العضلات القريبة من جذع الجسم، مثل الوركين والكتفين، ويكون أكثر حدة من ضعف الأطراف البعيدة.
- مشكلات التنفس الحادة: ضعف العضلات الوربية (بين الأضلاع) يؤدي إلى ضيق التنفس، والتهابات الرئة المتكررة، وصعوبة في السعال الفعال.
- صعوبات البلع والتغذية: يواجه المرضى، خاصة الرضع، تحديات في المص والبلع، مما قد يؤدي إلى سوء التغذية أو استنشاق الطعام إلى الرئتين.
- تأخر التطور الحركي: عدم القدرة على رفع الرأس، أو الجلوس دون دعم، أو الوقوف والمشي في المواعيد الطبيعية للنمو.
- ارتعاش اللسان: تلاحظ “بوابة HAEAT الطبية” أن تموجات أو ارتعاشات دقيقة في اللسان (Fasciculations) هي علامة مميزة جداً لهذا الاضطراب.
- العمود الفقري المشوه: غالباً ما يصاب المرضى بالجفن أو الانحناء الجانبي للعمود الفقري (Scoliosis) نتيجة ضعف العضلات الداعمة للظهر.
- غياب المنعكسات الوترية: ضعف أو اختفاء ردود الفعل العصبية عند النقر على الأوتار (مثل الركبة).
أسباب ضمور النخاع الشوكي
ينشأ ضمور النخاع الشوكي نتيجة طفرات جينية محددة تورث من الأبوين، حيث يلعب التركيب الوراثي الدور المحوري الوحيد في الإصابة بهذا المرض وفق التقسيم التالي:
- طفرة الجين SMN1: السبب الرئيسي في أكثر من 95% من الحالات هو غياب أو خلل في جين (Survival Motor Neuron 1) المسؤول عن إنتاج بروتين SMN.
- نقص بروتين SMN: هذا البروتين حيوي للحفاظ على صحة الخلايا العصبية الحركية؛ وبدونه، تبدأ هذه الخلايا في الموت المبرمج، مما يقطع الاتصال بالعضلات.
- دور الجين الاحتياطي SMN2: يمتلك البشر عدداً متغيراً من نسخ جين SMN2، وكلما زاد عدد هذه النسخ، كانت الأعراض أقل حدة، لأنها تنتج كمية ضئيلة من البروتين الوظيفي.
- الوراثة المتنحية: يُورث المرض بنمط “وراثي متنحي”، مما يعني أن الطفل يجب أن يتلقى نسخة من الجين المعيب من كلا الأبوين ليصاب بالمرض.
- ناقلو الجينات الصامتون: قد يحمل الأبوان الجين دون ظهور أعراض عليهما، وتصل نسبة احتمال إصابة الطفل بـ ضمور النخاع الشوكي إلى 25% في كل حمل إذا كان كلاهما حاملاً للجين.
متى تزور الطبيب؟
يعد التدخل المبكر حاسماً في إدارة ضمور النخاع الشوكي، حيث تساهم العلاجات الحديثة في وقف تدهور الخلايا العصبية قبل فقدانها نهائياً، لذا يجب الانتباه للمؤشرات التالية:
العلامات التحذيرية لدى الأطفال والرضع
- ملاحظة “رخاوة” غير طبيعية في جسم الرضيع (Floppy Baby Syndrome).
- ضعف حركة الأطراف أو عدم القدرة على الركل بقوة.
- صعوبات واضحة في الرضاعة أو البلع المتكرر.
- فشل الطفل في تحقيق المهارات الحركية الكبرى مثل التقلب أو الجلوس بمفرده.
العلامات التحذيرية لدى البالغين
- الشعور بضعف تدريجي في عضلات الفخذين أو الكتفين يصعب صعود الدرج.
- ملاحظة ارتجاف دقيق في عضلات اليدين عند محاولة استخدامها.
- حدوث سقطات متكررة أو فقدان التوازن بشكل غير مبرر.
دور الذكاء الاصطناعي في الفحص المبكر لضمور النخاع الشوكي
تؤكد الدراسات الحديثة في “مجلة حياة الطبية” أن خوارزميات الذكاء الاصطناعي باتت قادرة الآن على تحليل فيديوهات الحركة للأطفال في مراحلهم الأولى للكشف عن أنماط ضعف دقيقة لا تراها العين البشرية المجردة. يساعد هذا المسح الرقمي في تسريع إحالة الحالات المشتبه بها إلى الفحص الجيني قبل ظهور الأعراض الشاملة، مما يرفع من كفاءة العلاج الجيني بشكل مذهل.
عوامل خطر الإصابة بـ ضمور النخاع الشوكي
على الرغم من أن ضمور النخاع الشوكي هو اضطراب وراثي بحت، إلا أن هناك عوامل تزيد من احتمالية ظهور المرض أو انتقاله عبر الأجيال، وتشمل هذه العوامل ما يلي:
- التاريخ العائلي للإصابة: يُعد وجود قريب من الدرجة الأولى مصاب بالمرض أقوى مؤشر على وجود الجين المعيب في العائلة.
- الوالدان الحاملان للجين: إذا كان كلا الأبوين يحملان طفرة في جين SMN1، فإن خطر ولادة طفل مصاب بـ ضمور النخاع الشوكي يرتفع إلى 25% في كل حمل.
- زواج الأقارب: في المجتمعات التي يكثر فيها زواج الأقارب، تزداد احتمالية التقاء الجينات المتنحية المعيبة، مما يرفع معدلات انتشار المرض بشكل ملحوظ.
- العرق والأصل الإثني: تشير إحصائيات “موقع HAEAT الطبي” إلى أن نسب حاملي الجين تختلف طفيفاً بين الأعراق، لكن المرض يظل عالمياً ويصيب كافة الأجناس دون استثناء.
- غياب الفحص قبل الزواج: عدم إجراء التحاليل الجينية المخصصة للأمراض الوراثية يمنع الأزواج من معرفة وضعهم كحاملين للجين قبل التخطيط للإنجاب.
مضاعفات ضمور النخاع الشوكي
يؤدي التدهور المستمر في قوة العضلات إلى سلسلة من التحديات الصحية التي تؤثر على جودة الحياة وتتطلب تدخلاً طبياً مستمراً، ومن أبرز هذه المضاعفات:
- الفشل التنفسي المزمن: ضعف العضلات المسؤولة عن التنفس يجعل المريض عرضة لنقص الأكسجين وتراكم ثاني أكسيد الكربون.
- التهابات الرئة المتكررة: تؤدي صعوبة السعال وضعف عضلات البلع إلى دخول جزيئات الطعام أو اللعاب إلى الرئتين، مما يسبب “ذات الرئة الاستنشاقية”.
- تشوهات الهيكل العظمي: يعد الجنف (Scoliosis) من أكثر المضاعفات شيوعاً نتيجة عدم توازن القوة العضلية حول العمود الفقري، مما قد يضغط على الرئتين ويزيد صعوبة التنفس.
- تقبضات المفاصل (Contractures): يؤدي نقص الحركة إلى قصر العضلات والأوتار، مما يثبت المفاصل في وضعيات منحنية ومؤلمة.
- سوء التغذية الحاد: نضوب القدرة على المضغ والبلع يمنع المريض من الحصول على السعرات الحرارية الكافية، مما يسرع من عملية الهزال العضلي.
- تأثر جودة الحياة النفسية: يواجه المرضى تحديات في الاستقلالية، مما قد يؤدي إلى العزلة الاجتماعية أو الاكتئاب إذا لم يتوفر الدعم المناسب.
الوقاية من ضمور النخاع الشوكي
بما أن ضمور النخاع الشوكي مرض جيني، فإن الوقاية تركز بشكل أساسي على الجوانب الوراثية والتقنيات الإنجابية الحديثة، وتتمثل في النقاط التالية:
- الفحص الجيني قبل الزواج: إجراء اختبارات الدم للكشف عن طفرات جين SMN1 للأزواج الذين لديهم تاريخ عائلي أو في مناطق الانتشار العالي.
- التشخيص الوراثي قبل الانغراس (PGD): استخدام تقنيات التلقيح الاصطناعي لفحص الأجنة جينياً قبل زرعها في الرحم لضمان اختيار جنين سليم.
- الفحص المبكر لحديثي الولادة: إدراج ضمور النخاع الشوكي ضمن برامج فحص المواليد الإلزامية للكشف عن المرض قبل ظهور الأعراض السريرية.
- الاستشارة الوراثية: مراجعة متخصص في علم الوراثة لفهم نسب المخاطر والخيارات المتاحة لبناء أسرة سليمة.
- التوعية المجتمعية: نشر المعرفة حول نمط التوريث المتنحي لتقليل الوصمة المرتبطة بالأمراض الجينية وتشجيع الفحص الطوعي.
تشخيص ضمور النخاع الشوكي
يعتمد تشخيص ضمور النخاع الشوكي على تضافر التقييم السريري الدقيق مع الفحوصات المخبرية المتقدمة لضمان دقة النتائج، وتشمل الإجراءات ما يلي:
- الاختبار الجيني (المعيار الذهبي): تحليل دم للبحث عن حذف أو طفرة في جين SMN1، وهو الفحص الأكثر دقة وتحديداً للمرض.
- تحديد عدد نسخ جين SMN2: يساعد هذا الفحص في التنبؤ بمدى حدة المرض وتحديد البروتوكول العلاجي الأنسب.
- تخطيط العضلات الكهربائي (EMG): تقييم النشاط الكهربائي للعضلات، حيث يظهر في حالات الإصابة أنماطاً تشير إلى فقدان الأعصاب المحركة.
- دراسة التوصيل العصبي (NCS): قياس سرعة وقوة الإشارات العصبية، وتفيد في استبعاد أمراض الأعصاب الطرفية الأخرى.
- فحص إنزيم الكرياتين كينيز (CK): قد يظهر ارتفاعاً طفيفاً، ويستخدم “مدونة HAEAT الطبية” هذا الفحص للتمييز بين ضمور العضلات الناتج عن الأعصاب والضمور العضلي الأولي.
- خزعة العضلات: نادراً ما يتم اللجوء إليها حالياً، لكنها قد تظهر أنماطاً من الضمور العصبي في الحالات المعقدة تشخيصياً.
علاج ضمور النخاع الشوكي
شهد علاج ضمور النخاع الشوكي ثورة تاريخية في العقد الأخير، حيث انتقل من مجرد الرعاية التلطيفية إلى العلاجات المعدلة للمرض التي تستهدف السبب الجيني مباشرة.
نمط الحياة والرعاية المنزلية
تركز الرعاية المنزلية على الحفاظ على الوظائف الحيوية ومنع التدهور السريع، وتشمل:
- استخدام أجهزة التنفس غير الاختراقي (مثل BiPAP) خاصة أثناء النوم لضمان تهوية كافية للرئتين.
- الالتزام بجلسات العلاج الطبيعي اليومية للحفاظ على مرونة المفاصل ومنع التقلصات.
- توفير كراسي متحركة مخصصة وأدوات مساعدة للتنقل لتعزيز استقلالية المريض.
العلاجات الدوائية الحديثة
توجد حالياً أدوية معتمدة من FDA تعمل على زيادة مستويات بروتين SMN في الجسم:
- نيوسينيرسين (Spinraza): يُحقن في السائل الشوكي ويساعد الجين الاحتياطي SMN2 على إنتاج بروتين أكثر فعالية.
- ريسديبلام (Evrysdi): علاج سائل يُؤخذ عن طريق الفم يومياً، ويعمل بآلية مشابهة لزيادة إنتاج البروتين الوظيفي.
بروتوكول علاج الأطفال
يؤكد خبراء “كليفلاند كلينك” أن البدء بالعلاج في الأسابيع الأولى من العمر، خاصة قبل ظهور الأعراض، يمنح الطفل فرصة لتحقيق تطور حركي يقارب الطبيعي.
بروتوكول علاج البالغين
يركز العلاج لدى البالغين على استقرار الحالة ومنع المزيد من فقدان الخلايا العصبية الحركية، مع التركيز المكثف على العلاج الوظيفي والفيزيائي.
العلاج الجيني “زولجينزما” (Zolgensma) وآليات عمله الثورية
يُعتبر هذا العلاج قفزة علمية، حيث يتم حقن ناقل فيروسي (غير ضار) يحمل نسخة سليمة من جين SMN1 إلى داخل الخلايا. هي حقنة واحدة تُعطى وريدياً للأطفال دون سن الثانية، لتقوم بتعويض الجين المفقود بشكل دائم، مما يوقف تقدم ضمور النخاع الشوكي من جذوره.
دور العلاج الوظيفي في تعزيز الاستقلالية
يساعد المعالج الوظيفي مريض ضمور النخاع الشوكي على التكيف مع بيئته، من خلال تعديل أدوات الأكل والكتابة واستخدام التكنولوجيا المساعدة (مثل التحكم في الحاسوب عبر العين)، مما يرفع من جودة الحياة اليومية بشكل كبير.

الطب البديل وضمور النخاع الشوكي
لا يعد الطب البديل بديلاً عن العلاجات الجينية أو الدوائية، ولكنه يعمل كداعم لتحسين جودة الحياة وتخفيف بعض الأعراض الجسدية المرتبطة بـ ضمور النخاع الشوكي، وتشمل الخيارات المتاحة:
- العلاج المائي (Hydrotherapy): تساعد ممارسة التمارين في الماء الدافئ على تقليل الضغط على المفاصل وتسمح بحركات قد تكون مستحيلة على الأرض، مما يعزز القوة العضلية البسيطة.
- تمارين اليوغا والتنفس: تساهم وضعيات اليوغا المعدلة في الحفاظ على مرونة الأوتار، بينما تساعد تمارين التنفس العميق في تقوية الحجاب الحاجز وتوسيع الرئتين.
- التدليك العلاجي: يعمل المساج الطبي على تحسين الدورة الدموية في الأطراف الضعيفة وتقليل التشنجات العضلية المؤلمة الناتجة عن نقص الحركة.
- المكملات الغذائية المدروسة: قد يوصي البعض بالأحماض الأمينية أو الأوميغا 3 لدعم صحة الخلايا، ولكن يجب أن يتم ذلك تحت إشراف طبي كامل لتجنب التفاعلات الدوائية.
- الوخز بالإبر الصينية: تستخدم في بعض الحالات للمساعدة في إدارة الآلام المزمنة المرتبطة بتشوهات الهيكل العظمي، رغم محدودية الأدلة العلمية في هذا السياق تحديداً.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع مرض معقد مثل ضمور النخاع الشوكي تنظيماً دقيقاً للمعلومات الطبية لضمان الاستفادة القصوى من وقت الاستشارة.
ما يمكنك فعله قبل الموعد
- تدوين قائمة مفصلة بجميع المهارات الحركية التي فقدها المريض أو التي يجد صعوبة في أدائها مؤخراً.
- إعداد “شجرة عائلة” طبية توضح أي إصابات مشابهة أو وفيات مبكرة في العائلة لم يسبق تشخيصها.
- تسجيل مقاطع فيديو قصيرة للمريض أثناء الحركة أو التنفس لإطلاع الطبيب على الأنماط التي قد لا تظهر بوضوح في غرفة الكشف.
ما تتوقعه من الطبيب المختص
- سيسألك الطبيب عن توقيت ظهور أول علامة للضعف العضلي ومدى سرعة تطورها.
- إجراء فحص بدني شامل يتضمن اختبار المنعكسات الوترية وتقييم قوة العضلات الدانية.
- طلب فحوصات دم جينية عاجلة لتأكيد التشخيص والبدء في بروتوكول العلاج المعدل للمرض.
استخدام المنصات الرقمية لمتابعة تطور الأعراض
نوصي باستخدام تطبيقات تسجيل البيانات الصحية التي تتيح تتبع قوة القبضة، ومعدلات التنفس، وكفاءة البلع بشكل يومي. هذه البيانات الرقمية توفر للطبيب صورة واقعية عن تطور ضمور النخاع الشوكي بعيداً عن لحظة الكشف السريري، مما يساعد في تعديل الجرعات الدوائية بدقة أكبر.
مراحل الشفاء من ضمور النخاع الشوكي
في حالة ضمور النخاع الشوكي، غالباً ما يعني “الشفاء” استقرار الحالة، منع التدهور، واكتساب مهارات حركية جديدة كانت مفقودة، وتمر هذه العملية بعدة مراحل:
- مرحلة التقييم القاعدي: تحديد مستوى الوظائف الحركية الحالية قبل البدء بالعلاجات الحديثة (مثل نيوسينيرسين).
- مرحلة الاستجابة الدوائية: تبدأ الخلايا العصبية المتبقية في العمل بكفاءة أكبر نتيجة زيادة بروتين SMN، وتظهر أولى بوادر التحسن في قوة التنفس والبلع.
- مرحلة التأهيل المكثف: هي المرحلة الأطول، وتتضمن تدريب العضلات على المهارات الجديدة مثل الجلوس أو تحريك الأطراف باستخدام العلاج الفيزيائي.
- مرحلة الاستقرار الطويل: المتابعة الدورية لضمان استمرار مفعول العلاج الجيني ومراقبة أي مضاعفات ثانوية في العمود الفقري أو المفاصل.
الأنواع الشائعة لـ ضمور النخاع الشوكي
يُصنف ضمور النخاع الشوكي إلى عدة أنواع رئيسية تعتمد على عمر الظهور وأقصى وظيفة حركية يمكن تحقيقها:
- النوع الأول (مرض ويردنيج هوفمان): يظهر قبل عمر 6 أشهر، وهو الأخطر حيث لا يستطيع الرضع الجلوس دون دعم، ويعانون من مشكلات تنفسية حادة.
- النوع الثاني (النوع المتوسط): يظهر بين 6 و18 شهراً، يستطيع الأطفال الجلوس ولكن لا يمكنهم الوقوف أو المشي بمفردهم.
- النوع الثالث (مرض كوجيلبرج ويلاندر): يظهر بعد عمر 18 شهراً، ويستطيع المصابون المشي بشكل مستقل ولكن قد يفقدون هذه القدرة لاحقاً في الحياة.
- النوع الرابع (النوع المتأخر): يصيب البالغين عادة في سن الثلاثينات، وتكون أعراضه خفيفة مقارنة بالأنواع الأخرى، وتؤثر غالباً على المشي.
- النوع صفر: نوع نادر جداً وحاد يظهر قبل الولادة، ويتميز بضعف حركة الجنين في الرحم.
التطورات الجينية الحديثة في علاج ضمور النخاع الشوكي
تشهد الساحة الطبية حالياً أبحاثاً واعدة تتجاوز العلاجات الحالية، حيث يتم استكشاف تقنيات “تحرير القواعد الجينية” (Base Editing) لتصحيح طفرة جين SMN1 داخل الجسم بدقة متناهية. كما تهدف الدراسات الحديثة إلى تطوير أدوية تستهدف العضلات مباشرة لزيادة قوتها وحمايتها من الضمور، بالتوازي مع العلاجات العصبية، مما يخلق نهجاً علاجياً مزدوجاً لمرضى ضمور النخاع الشوكي.
تأثير ضمور النخاع الشوكي على الصحة النفسية وجودة الحياة
لا يقتصر تأثير المرض على الجسد، بل يمتد ليشمل الصحة النفسية للمريض وعائلته:
- إرهاق مقدمي الرعاية: العبء البدني والنفسي على الوالدين يتطلب دعماً نفسياً تخصصياً لمنع الاحتراق النفسي.
- الاستقلالية والهوية: يواجه المراهقون المصابون تحديات في بناء هويتهم المستقلة، مما يستدعي توفير أدوات مساعدة تكنولوجية متطورة.
- التنمر والعزلة: يحتاج المصابون إلى بيئة مدرسية واجتماعية واعية تضمن دمجهم الكامل وتمنع تدهور حالتهم النفسية.
الإدارة التغذوية المتخصصة لمرضى ضمور النخاع الشوكي
التغذية السليمة هي حجر الزاوية في إدارة ضمور النخاع الشوكي؛ فالسمنة تزيد العبء على العضلات الضعيفة، بينما سوء التغذية يسرع الضمور. يُنصح بنظام غذائي عالي البروتين لدعم الأنسجة العضلية، مع التركيز على الألياف والسوائل لتجنب الإمساك المزمن الناتج عن ضعف عضلات البطن وقلة الحركة. في حالات صعوبة البلع، يتم اللجوء إلى أنابيب التغذية لضمان حصول الجسم على احتياجاته دون خطر الاستنشاق.
الدعم المجتمعي والحقوق القانونية للمصابين بضمور النخاع الشوكي
يجب على العائلات معرفة حقوقهم القانونية التي تضمنها التشريعات الحديثة، مثل الحق في التعليم الشامل، وتوفير بيئة عمل مهيأة، والحصول على التسهيلات في الأماكن العامة. تساهم مجموعات دعم المرضى في تبادل الخبرات حول أفضل الأجهزة التعويضية وكيفية الحصول على التمويل للعلاجات الباهظة لمرض ضمور النخاع الشوكي.
خرافات شائعة حول ضمور النخاع الشوكي
- الخرافة: ضمور النخاع الشوكي يصيب الأطفال فقط.
- الحقيقة: يمكن أن يبدأ النوع الرابع في الظهور لدى البالغين، كما أن العلاجات الحديثة جعلت المصابين بالأنواع المبكرة يعيشون حتى سن البلوغ.
- الخرافة: العلاج الجيني يشفي المرض تماماً في لحظات.
- الحقيقة: العلاج يوقف تقدم المرض ويعوض الجين المفقود، لكن العضلات التي ضمرت بالفعل تحتاج إلى سنوات من التأهيل لاستعادة جزء من وظيفتها.
- الخرافة: المصابون بـ ضمور النخاع الشوكي يعانون من تراجع ذهني.
- الحقيقة: المرض لا يؤثر إطلاقاً على الذكاء، بل إن العديد من المصابين يتميزون بقدرات ذهنية وإبداعية فائقة.
نصائح ذهبية من “مدونة حياة الطبية” 💡
- السرعة هي الحياة: في مرض ضمور النخاع الشوكي، كل يوم يمر دون علاج يعني فقدان خلايا عصبية لا تعوض؛ لا تنتظر “غداً” للتشخيص.
- التنفس أولاً: اجعل مراقبة كفاءة التنفس أولوية قصوى، واستثمر في أجهزة قياس الأكسجين المنزلية.
- الكرسي المتحرك ليس نهاية: اعتبر الوسائل المساعدة “أجنحة” تمنح المريض حرية الحركة والاستكشاف، وليست قيوداً.
- وثق مسيرتك: احتفظ بسجل طبي رقمي شامل لكل التحاليل الجينية والجرعات الدوائية، فهذا يسهل الانتقال بين الفرق الطبية.
- تواصل مع مجتمعك: الانضمام لجمعيات مرضى ضمور النخاع الشوكي يوفر لك دعماً عاطفياً ومعلوماتياً لا يقدر بثمن.
أسئلة شائعة
هل يمكن علاج ضمور النخاع الشوكي بعد فوات الأوان؟
لا يوجد وقت “متأخر جداً” للبدء بالعلاجات الحديثة؛ فبينما تكون النتائج في أوجها عند البدء المبكر، إلا أن العلاج حتى في المراحل المتقدمة يساعد في استقرار الوظائف الحيوية مثل التنفس والبلع ومنع المزيد من التدهور.
هل ينتقل ضمور النخاع الشوكي للأبناء إذا كان أحد الأبوين مصاباً؟
إذا كان أحد الأبوين مصاباً والآخر لا يحمل الجين، سيكون جميع الأبناء حاملين للجين دون إصابة. أما إذا كان الطرف الآخر حاملاً للجين، فهناك احتمالية 50% لإصابة كل طفل.
ما هو الفرق بين ضمور العضلات وضمور النخاع الشوكي؟
ضمور العضلات (مثل دوشين) ناتج عن خلل في ألياف العضلات نفسها، بينما ضمور النخاع الشوكي ناتج عن خلل في الأعصاب التي تغذي العضلات في الحبل الشوكي.
ما هي تكلفة العلاج الجيني لضمور النخاع الشوكي؟
يُعد “زولجينزما” من أغلى الأدوية عالمياً، حيث تتجاوز تكلفته 2 مليون دولار، ولكن العديد من الدول توفره الآن ضمن برامج الرعاية الحكومية أو التأمين الصحي الشامل نظراً لفعاليته الحاسمة.
الخاتمة
يظل ضمور النخاع الشوكي تحدياً طبياً كبيراً، ولكن العلم في عام 2026 قد قطع شوطاً هائلاً في تحويل هذا المرض من حكم بالموت أو العجز الكلي إلى حالة مزمنة يمكن إدارتها والعيش معها بأمل كبير. إن الفهم العميق للأسباب، والتشخيص المبكر، والوصول إلى العلاجات الجينية المبتكرة، هي الركائز الثلاث التي تضمن لمصابي ضمور النخاع الشوكي مستقبلاً أكثر إشراقاً واستقلالية.