يُعد مستضد نسيجي (Histocompatibility Leucocyte Antigen – HLA) حجر الزاوية في نظام المناعة البشري، حيث يعمل بمثابة “بطاقة هوية” خلوية تسمح للجسم بالتمييز بين خلاياه الذاتية والأجسام الغريبة.
إن فهم هذا النظام المعقد لا يقتصر على المختبرات فحسب، بل هو مفتاح تشخيص وعلاج مجموعة واسعة من الأمراض المناعية والوراثية. في هذا الدليل المعمق من مدونة حياة الطبية، سنكشف أسرار هذه البروتينات وتأثيرها المباشر على صحتك.
ما هو مستضد نسيجي؟
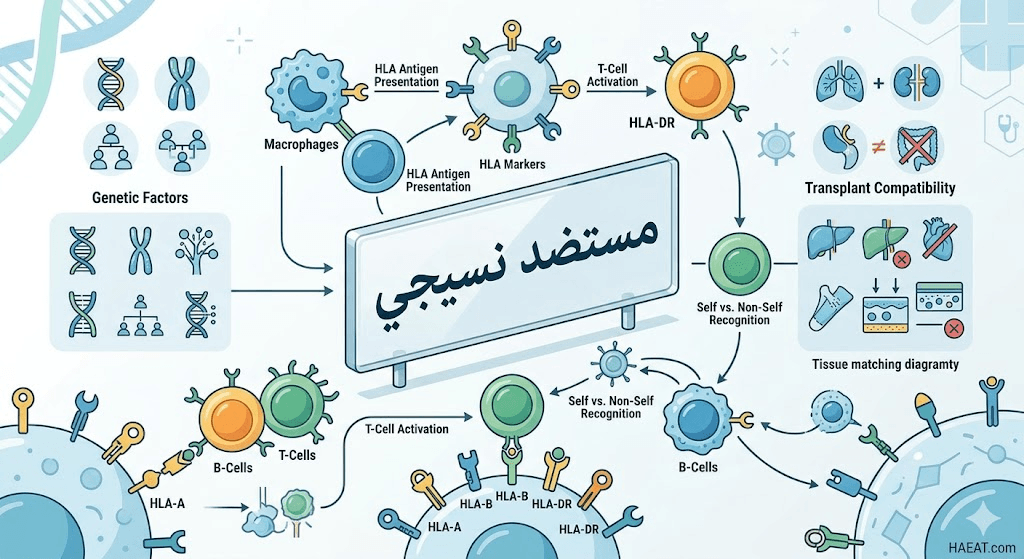
يعرف مستضد نسيجي بأنه مجموعة من البروتينات الموجودة على سطح معظم خلايا الجسم، وتعمل كمنصة لعرض أجزاء من البروتينات (الببتيدات) للجهاز المناعي. يتم تشفير هذه المستضدات بواسطة مجموعة جينات تقع على الكروموسوم رقم 6، وهي المسؤولة عن تحديد مدى توافق الأنسجة بين الأفراد، خاصة في سياق زراعة الأعضاء.
تؤدي هذه الجزيئات دوراً محورياً في استجابة الخلايا التائية؛ فإذا تعرف الجهاز المناعي على بروتين معروض بواسطة مستضد نسيجي على أنه “غريب” (مثل فيروس أو خلية سرطانية)، فإنه يشن هجوماً فورياً. وتعتبر هذه المنظومة الجينية الأكثر تنوعاً وتعدداً في الجنس البشري، مما يجعل لكل فرد بصمة جينية تكاد تكون فريدة من نوعها، باستثناء التوائم المتطابقة.

أعراض اضطرابات مستضد نسيجي
يجب التوضيح أن هذا المستضد في حد ذاته ليس مرضاً، ولكن وجود أنماط جينية معينة يرتبط بظهور أعراض سريرية ناتجة عن خلل في التعرف المناعي، وتتلخص هذه الأعراض وفقاً للحالات المرتبطة بها فيما يلي:
- آلام المفاصل وتيبسها: يرتبط نمط HLA-B27 بآلام مزمنة في أسفل الظهر وتيبس صباحي، وهو ما يشير غالباً إلى التهاب الفقار المقسط.
- الاضطرابات الهضمية الحادة: تظهر أعراض مثل الإسهال المزمن، الانتفاخ، وسوء الامتصاص عند الأفراد الذين يحملون أنماط HLA-DQ2 أو DQ8 عند تناول الجلوتين.
- الطفح الجلدي والتقرحات: تظهر بعض الاضطرابات المناعية المرتبطة بـ مستضد نسيجي على شكل صدفية شديدة أو تقرحات فموية وتناسلية (كما في مرض بهجت).
- العطش الشديد والتبول المتكرر: قد تشير هذه الأعراض إلى بداية السكري من النوع الأول، المرتبط بقوة ببعض جينات HLA التي تهاجم خلايا البنكرياس.
- علامات رفض العضو المزروع: في حالات زراعة الأعضاء، يظهر عدم توافق مستضد نسيجي على شكل حمى، ألم في مكان الزرع، وتدهور سريع في وظائف العضو.
- التهابات العين المتكررة: مثل التهاب القزحية الأمامي الذي يسبب احمراراً، ألماً، وحساسية تجاه الضوء.
- التعب المزمن غير المبرر: الناتج عن النشاط الزائد للجهاز المناعي أو الالتهابات الكامنة المرتبطة بالاستعداد الوراثي.
أسباب تباين مستضد نسيجي بين البشر
يعود التنوع الهائل في أنماط هذا المستضد إلى عوامل تطورية وجينية معقدة تهدف إلى حماية الجنس البشري من الانقراض بسبب الأوبئة، وتتمثل الأسباب في:
- التعددية الشكلية المتطرفة (Polymorphism): يمتلك نظام HLA آلاف الأليلات (النسخ الجينية) المختلفة، مما يضمن وجود أفراد في كل مجتمع قادرين على مقاومة مسببات أمراض معينة.
- الوراثة المندلية والسيادة المشتركة: يرث الفرد مجموعة واحدة من جينات مستضد نسيجي من كل والد، ويتم التعبير عن كلاهما معاً، مما يضاعف احتمالات الاستجابة المناعية.
- الضغط الانتخابي من الميكروبات: عبر العصور، نجت المجموعات البشرية التي امتلكت أنماطاً من مستضد نسيجي قادرة على اكتشاف الفيروسات والبكتيريا المحلية بفعالية.
- إعادة الارتباط الجيني: تحدث عمليات تبادل جيني أثناء تكوين الخلايا التناسلية، مما يؤدي أحياناً إلى ظهور توليفات جديدة من مستضدات الأنسجة.
- التوزيع العرقي والجغرافي: تؤدي الهجرات البشرية والعزلة الجغرافية إلى تركز أنماط معينة من مستضد نسيجي في شعوب دون غيرها، مما يفسر تباين نسب الإصابة بالأمراض المناعية عالمياً.
متى تزور الطبيب؟
إن تحديد الوقت المناسب لاستشارة المختصين حول فحص هذا المستضد يعتمد على التاريخ المرضي والعائلي، وتوضح مجلة حياة الطبية الحالات التي تتطلب تدخلاً طبياً:
عند البالغين
يجب التوجه للطبيب في حال المعاناة من آلام ظهر مزمنة تبدأ قبل سن الأربعين ولا تتحسن بالراحة، أو عند وجود اضطرابات هضمية غير مفسرة رغم اتباع حميات مختلفة. كما يُعد الفحص ضرورياً إذا كان الشخص مرشحاً لعملية زراعة أعضاء أو نخاع عظمي، أو إذا ظهرت تفاعلات جلدية شديدة وتاريخ عائلي من أمراض المناعة الذاتية.
عند الأطفال
تستوجب أعراض مثل تأخر النمو، الإسهال المتكرر المرتبط بإدخال الحبوب (القمح)، أو ظهور علامات السكري المبكر (كثرة التبول والعطش) إجراء تقييم لنمط هذا المستضد. (وفقاً لـ “كليفلاند كلينك“، فإن التشخيص المبكر للأنماط المرتبطة بالسكري قد ينقذ الطفل من مضاعفات حادة مثل الحماض الكيتوني).
دور الخوارزميات التنبؤية في رصد التفاعلات المناعية
في العصر الحديث، يقترح خبراء موقع حياة الطبي اللجوء إلى الفحوصات الجينية التنبؤية عند وجود أقارب من الدرجة الأولى مصابين بأمراض مرتبطة بـ HLA. تستخدم هذه الخوارزميات بيانات مستضد نسيجي لتحليل احتمالية الإصابة المستقبلية، مما يسمح للأطباء بوضع خطط وقائية صارمة قبل ظهور الأعراض السريرية الواضحة، خاصة في حالات التصلب المتعدد أو التهاب المفاصل الروماتويدي.
عوامل خطر الإصابة بـ مستضد نسيجي
على الرغم من أن نظام هذا المستضد هو جزء طبيعي من التكوين البيولوجي، إلا أن هناك عوامل تزيد من احتمالية ارتباط أنماط معينة منه بأمراض خطيرة، وهي:
- التاريخ العائلي الوراثي: يعتبر وجود قريب من الدرجة الأولى مصاب بمرض مناعي مرتبط بـ مستضد نسيجي (مثل الذئبة الحمراء أو التهاب المفاصل) العامل الأقوى في تحديد الخطر الجيني.
- الأصول العرقية والجغرافية: ترتبط بعض الأنماط الجينية لشعوب معينة بأمراض محددة؛ فمثلاً نمط HLA-B27 ينتشر بكثرة في شعوب شمال أوروبا، مما يرفع نسب إصابتهم بالتهابات الفقار.
- الجنس (النوع الاجتماعي): تظهر الدراسات أن النساء أكثر عرضة للإصابة بالأمراض المناعية المرتبطة بـ مستضد نسيجي بنسبة تصل إلى 3 أضعاف مقارنة بالرجال، خاصة في أمراض مثل التهاب المفاصل الروماتويدي.
- التعرض للعدوى الفيروسية: قد تؤدي بعض الفيروسات إلى تحفيز الجهاز المناعي لمهاجمة جزيئات مستضد نسيجي الذاتية عبر آلية “المحاكاة الجزيئية”.
- العوامل البيئية والكيميائية: قد يؤدي التعرض المستمر لبعض السموم أو التدخين إلى تعديل الطريقة التي يعرض بها مستضد نسيجي البروتينات للخلايا المناعية، مما يشرع في الهجوم الذاتي.
مضاعفات مستضد نسيجي
تنشأ المضاعفات عندما يفشل نظام مستضد نسيجي في أداء مهمته بدقة، أو عندما يتعرض الجسم لرد فعل مناعي عنيف، وتشمل هذه المخاطر:
- الفشل العضوي التام: في حالات زراعة الكلى أو الكبد، يؤدي عدم تطابق هذا المستضد إلى رفض حاد قد يدمر العضو الجديد خلال ساعات أو أيام.
- الإعاقة الحركية الدائمة: يؤدي التهاب الفقار المرتبط بنمط HLA-B27 إلى اندماج فقرات العمود الفقري، مما يفقد المريض القدرة على الانحناء أو الحركة الطبيعية.
- فقدان البصر التدريجي: ترتبط بعض أنماط مستضد نسيجي بالتهابات العين المزمنة التي قد تنتهي بتلف العصب البصري إذا لم تُعالج فوراً.
- سوء التغذية الحاد وهشاشة العظام: نتيجة لتدمير أهداب الأمعاء في مرضى السيلياك (المرتبط بـ HLA-DQ2/DQ8)، مما يمنع امتصاص العناصر الحيوية.
- أمراض القلب والأوعية الدموية: تزيد بعض الالتهابات المناعية المرتبطة بـ مستضد نسيجي من فرص الإصابة بتصلب الشرايين المبكر والتهاب عضلة القلب.
الوقاية من مستضد نسيجي
تؤكد مدونة HAEAT الطبية أنه لا يمكن تغيير الجينات، ولكن يمكن الوقاية من تحفيزها الضار وتجنب مضاعفاتها من خلال:
- الفحص الجيني الاستباقي: إجراء تحليل مستضد نسيجي للأفراد الذين لديهم تاريخ عائلي قوي للبدء في إجراءات وقائية مبكرة.
- التدقيق في اختيار المتبرعين: استخدام تقنيات المطابقة عالية الدقة (High-Resolution Typing) لضمان أعلى نسبة توافق في عمليات نقل النخاع والأعضاء.
- الحمية الغذائية الوقائية: تجنب محفزات المناعة مثل الجلوتين للأفراد الذين يحملون استعداداً وراثياً للاضطرابات الهضمية المرتبطة بـ مستضد نسيجي.
- الاستشارة الجينية قبل الزواج: لتقييم احتمالات انتقال الأمراض المناعية الوراثية المرتبطة بأنماط معينة من HLA للأبناء.
- تجنب المحفزات البيئية: مثل الإقلاع عن التدخين وتقليل التوتر، حيث أثبتت الأبحاث أن الضغوط النفسية تحفز التعبير الجيني الضار لـ مستضد نسيجي.
تشخيص مستضد نسيجي
تطور تشخيص أنماط مستضد نسيجي بشكل هائل، وتستخدم المختبرات المتقدمة اليوم وفقاً لـ بوابة HAEAT الطبية التقنيات التالية:
- تقنية PCR-SSO: وهي فحص يعتمد على تفاعل البوليميراز المتسلسل لتحديد تسلسل الأليلات بدقة متوسطة إلى عالية.
- تسلسل الجيل القادم (NGS): يعتبر أدق فحص متاح حالياً لتنميط مستضد نسيجي، حيث يقرأ الشيفرة الجينية بالكامل للكشف عن الطفرات النادرة.
- اختبار المطابقة المتقاطعة (Cross-matching): فحص حيوي يتم قبل الزراعة للتأكد من عدم وجود أجسام مضادة في دم المتلقي تهاجم مستضد نسيجي الخاص بالمتبرع.
- المقايسات المناعية القائمة على اللومينكس (Luminex): تقنية تستخدم جزيئات دقيقة للكشف عن الأجسام المضادة الموجهة ضد مستضدات الأنسجة في المصل.
- الفحص الخلوي التدفيقي (Flow Cytometry): يستخدم لتقييم استجابة الخلايا اللمفاوية تجاه جزيئات مستضد نسيجي المعينة، مما يوفر رؤية ديناميكية للحالة المناعية.

علاج مستضد نسيجي
تعتمد استراتيجية العلاج على إدارة الاستجابة المناعية المفرطة وتسكين الأعراض، وتنقسم إلى عدة مستويات:
نمط الحياة والرعاية المنزلية
يُنصح المرضى الذين يعانون من اضطرابات مرتبطة بـ مستضد نسيجي باتباع نظام غذائي مضاد للالتهابات (مثل حمية البحر المتوسط)، وممارسة التمارين الرياضية منخفضة التأثير للحفاظ على مرونة المفاصل، مع ضرورة الالتزام بفترات راحة كافية لتقليل إجهاد الجهاز المناعي.
العلاجات الدوائية والمناعية
عند البالغين
يتم التركيز على استخدام المثبطات المناعية القوية مثل “الميثوتركسيت”، والعلاجات البيولوجية (مضادات TNF) مثل “إيتانيرسيبت” و”أداليموماب”، التي تستهدف المسارات الالتهابية التي يثيرها خلل مستضد نسيجي.
عند الأطفال
تُستخدم جرعات دقيقة من الكورتيكوستيرويدات، مع التركيز الشديد على العلاجات المناعية التي لا تؤثر على النمو الطبيعي، بالإضافة إلى الأنسولين في حالات السكري المرتبطة بنمط HLA.
هندسة الخلايا التائية الموجهة
يقترح علماء المناعة استخدام تقنيات “CAR-T cell” المعدلة لإعادة تعليم الجهاز المناعي بحيث يتوقف عن مهاجمة جزيئات مستضد نسيجي الذاتية، مما قد يؤدي إلى شفاء تام من بعض الأمراض المناعية بدلاً من مجرد إدارة الأعراض.
بروتوكولات تثبيط المناعة الانتقائية
تطوير أدوية “ذكية” لا تثبط الجهاز المناعي بالكامل، بل تعطل فقط التفاعل بين نوع محدد من مستضد نسيجي والخلية المناعية المهاجمة، مما يقلل بشكل كبير من خطر الإصابة بالعدوى الجانبية.
الطب البديل لمستضد نسيجي
لا يمكن للطب البديل أن يحل محل العلاجات المناعية في حالات اضطراب مستضد نسيجي، لكنه يلعب دوراً “مسانداً” (Complementary) في تقليل مستويات الالتهاب العام في الجسم، ومن أبرز هذه الوسائل المدعومة بحثياً:
- فيتامين د (Vitamin D): أثبتت الدراسات في “المعاهد الوطنية للصحة NIH” أن فيتامين د يلعب دوراً تنظيمياً مباشراً في تعبير جينات مستضد نسيجي من الفئة الثانية، مما يساعد في تهدئة النشاط المناعي المفرط.
- الكركمين (Curcumin): يعتبر مضاد التهاب طبيعي قوي، يساعد في تقليل إشارات السيتوكينات التي يتم تحفيزها عند تعرف الخلايا التائية على جزيئات مستضد نسيجي الغريبة.
- أحماض أوميجا-3 الدهنية: تساهم في تعديل مرونة أغشية الخلايا، مما قد يؤثر بشكل طفيف على كيفية عرض البروتينات عبر مستضدات الأنسجة.
- مكملات الزنك: ضرورية لوظيفة الخلايا التائية السليمة، وتساعد في منع الاستجابات المناعية العشوائية المرتبطة بنقص التوازن المعدني.
- تقنيات تقليل التوتر (اليوجا والتأمل): بما أن الضغط النفسي يرفع مستويات الكورتيزول الذي يؤثر على التعبير الجيني لـ مستضد نسيجي، فإن هذه الممارسات تعد ضرورية للحفاظ على استقرار الحالة المناعية.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع حالات مستضد نسيجي تحضيراً دقيقاً لضمان الحصول على التشخيص الصحيح، وإليك الخطوات العملية:
ماذا تفعل؟
قم بتدوين كافة الأعراض المناعية التي عانيت منها، حتى تلك التي تبدو غير مترابطة مثل جفاف العين مع آلام الظهر. اجمع سجلاً عائلياً دقيقاً لأي أمراض وراثية أو مناعية لدى الأقارب من الدرجة الأولى والثانية، فهذا يساعد الطبيب في تحديد نمط مستضد نسيجي المحتمل للبحث عنه.
ماذا تتوقع من الطبيب؟
سيقوم الطبيب المختص (غالباً استشاري روماتيزم أو أمراض دم وزراعة) بطلب فحوصات دقيقة للدم، وقد يستفسر عن أصولك العرقية لتضييق نطاق الاحتمالات الجينية. سيناقش معك مخاطر وفوائد العلاج البيولوجي إذا ثبت ارتباط حالتك بنمط معين من مستضد نسيجي.
استخدام التطبيقات الصحية لتتبع السجل الجيني
يقترح خبراء التقنية الطبية استخدام تطبيقات تعتمد على الذكاء الاصطناعي لربط بيانات الفحوصات الجينية السابقة مع الأعراض اليومية، مما يخلق خارطة طريق رقمية تسهل على الطبيب فهم التفاعل بين مستضد نسيجي والبيئة المحيطة بك.
مراحل الشفاء من مستضد نسيجي
نظراً لأن مستضد نسيجي جزء ثابت من جيناتك، فإن “الشفاء” هنا يعني الوصول إلى حالة الاستقرار المناعي (Remission) وتجنب المضاعفات، وتمر هذه العملية بمراحل:
- المرحلة الحادة: تركز على كبح الهجوم المناعي الأولي باستخدام جرعات عالية من الأدوية المثبطة.
- مرحلة الاستقرار: تعديل الجرعات للوصول إلى أدنى مستوى من الالتهاب مع أقل آثار جانبية ممكنة.
- المرحلة الوقائية طويلة الأمد: مراقبة دورية لمستويات الأجسام المضادة الموجهة ضد مستضد نسيجي، خاصة بعد عمليات الزراعة.
- مرحلة التكيف النسيجي: في حالات زراعة النخاع، يحتاج الجسم لفترة قد تصل لعام ليتعرف الجهاز المناعي الجديد على خلايا المضيف (المتلقي) كخلايا صديقة.
الأنواع الشائعة لمستضد نسيجي
ينقسم نظام مستضد نسيجي البشري إلى ثلاث فئات رئيسية، لكل منها دور وظيفي محدد:
- الفئة الأولى (Class I): تشمل الأنماط HLA-A، وHLA-B، وHLA-C. توجد على سطح جميع الخلايا ذات النواة، وهي المسؤولة عن عرض البروتينات الفيروسية للخلايا التائية القاتلة.
- الفئة الثانية (Class II): تشمل الأنماط HLA-DR، وHLA-DQ، وHLA-DP. توجد بشكل أساسي على الخلايا المناعية المتخصصة (مثل الخلايا البالعة)، وهي المسؤولة عن بدء الاستجابة المناعية الشاملة.
- الفئة الثالثة (Class III): تحتوي على جينات تشفر بروتينات مكملة (Complement system) تلعب دوراً في الالتهاب، لكنها لا تعرض المستضدات مباشرة.
دور المستضد النسيجي في نجاح زراعة الأعضاء والنخاع العظمي
تعتمد نجاة المريض بعد الزراعة على دقة المطابقة في مستضد نسيجي؛ فكلما زاد عدد الأليلات المتطابقة (مثلاً 10/10)، قلت احتمالية حدوث رفض العضو أو داء المضيف. في زراعة النخاع العظمي، تعتبر مطابقة مستضد نسيجي أكثر صرامة منها في زراعة الأعضاء الصلبة مثل الكلى، لأن الخلايا المنقولة هي بحد ذاتها جهاز مناعي جديد
التوزيع العالمي لأنماط المستضد النسيجي وتنوعها العرقي
تعكس أنماط مستضد نسيجي تاريخ الهجرات البشرية؛ حيث نجد أن بعض الأنماط التي توفر حماية ضد الملاريا تتركز في شعوب أفريقيا وجنوب آسيا. في المقابل، نجد أن “تأثير المؤسس” (Founder Effect) قد جعل بعض الأنماط النادرة في العالم شائعة جداً في مجتمعات مغلقة، مما يزيد من صعوبة العثور على متبرعين متطابقين لهؤلاء الأفراد خارج محيطهم العرقي.
الارتباط الخفي بين مستضد نسيجي والحساسيات الغذائية المعقدة
لا يقتصر دور مستضد نسيجي على محاربة الفيروسات، بل يمتد لتحديد كيفية تفاعل الجسم مع البروتينات الغذائية. إن الأشخاص الذين يحملون استعداداً وراثياً في جينات HLA-DQ يكون جهازهم المناعي مهيأً لاعتبار بروتين الجلوتين “عدواً”، مما يطلق سلسلة من التفاعلات الالتهابية التي تدمر بطانة الأمعاء، وهو ما يفسر لماذا يصاب البعض بالسيلياك بينما يتناول الآخرون نفس الطعام بأمان.
الأبعاد النفسية والاجتماعية للفحوصات الجينية لـ HLA
قد يسبب اكتشاف نمط جيني معين من مستضد نسيجي مرتبط بمرض مزمن قلقاً وجودياً للمريض. كما أن صعوبة العثور على متبرع مطابق في العائلات الصغيرة أو الأقليات العرقية تضع عبئاً نفسياً ثقيلاً على المرضى الذين ينتظرون زراعة الأعضاء، مما يستوجب توفير دعم نفسي متخصص يرافق الفحوصات المختبرية.
مستقبل التعديل الجيني لمستضدات الأنسجة
بفضل تقنيات مثل CRISPR، يعمل الباحثون حالياً على “تعديل” جينات مستضد نسيجي في الأعضاء المتبرع بها لجعلها “غير مرئية” للجهاز المناعي للمتلقي. هذا الاختراق العلمي قد ينهي الحاجة إلى المطابقة التامة بين المتبرع والمريض، ويقضي على مشكلة رفض الأعضاء المزمنة، مما يفتح الباب لعصر “الأعضاء العالمية”.
خرافات شائعة
- الخرافة الأولى: “تطابق فصيلة الدم يعني تطابق الأنسجة”. الحقيقة أن تطابق فصيلة الدم هو الخطوة الأولى فقط، بينما يتطلب هذا المستضد مطابقة جينية أعمق بكثير.
- الخرافة الثانية: “يمكن للأشقاء دائماً التبرع لبعضهم”. الحقيقة أن هناك فرصة بنسبة 25% فقط لتطابق مستضد نسيجي الكامل بين الأشقاء.
- الخرافة الثالثة: “نمط HLA يحدد ذكاء الشخص أو قوته”. الحقيقة أن دوره محصور تماماً في النظام المناعي وتوافق الأنسجة.
نصائح ذهبية من “مدونة حياة الطبية” 💡
- التوثيق الجيني: احتفظ بنسخة ورقية ورقمية من نتائج فحص هذا المستضد الخاص بك؛ فقد تحتاجها بشكل طارئ في المستقبل.
- التوعية العائلية: إذا تم اكتشاف نمط مرتبط بمرض مناعي لديك، شجع أفراد عائلتك على إجراء الفحص الاستباقي.
- التوازن المناعي: لا تسرف في استخدام “محفزات المناعة” العشوائية دون استشارة، لأنها قد تزيد من حدة هجوم مستضد نسيجي الذاتي في حال وجود استعداد وراثي.
- الصبر في المطابقة: العثور على المتبرع المثالي لـهذا المستضد قد يستغرق وقتاً، فلا تفقد الأمل واستعن بقواعد البيانات العالمية.
أسئلة شائعة
هل يمكن أن يتغير نمط هذا المستضد الخاص بي؟
لا، النمط الجيني ثابت منذ الولادة، لكن يمكن أن “يتغير” في حال خضوعك لعملية زراعة نخاع عظمي ناجحة، حيث تكتسب نمط المتبرع.
لماذا يعتبر فحص مستضد نسيجي مكلفاً؟
لأنه يتطلب تقنيات بيولوجيا جزيئية متقدمة ومواد كيميائية دقيقة جداً لتحديد الترتيب الجيني الصحيح بين آلاف الاحتمالات.
كم يستغرق ظهور نتائج فحص HLA؟
يعتمد ذلك على التقنية المستخدمة؛ الفحوصات السريعة تستغرق 24-48 ساعة، بينما التنميط عالي الدقة قد يستغرق أسبوعين.
الخاتمة
في ختام هذا الدليل، يمثل مستضد نسيجي البوابة التي يعبر من خلالها جهازنا المناعي نحو حمايتنا أو مهاجمتنا. إن فهمك لهذه “البصمة الجينية” ليس مجرد ترف علمي، بل هو أداة حيوية للوقاية والتعايش مع الأمراض المعقدة. تذكر دائماً أن جيناتك ترسم المسار، لكن الوعي الطبي والرعاية المتخصصة هما من يحددان الوجهة نحو حياة صحية مستقرة.








