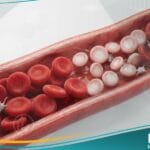
فقر الدم اللاتنسجي الوراثي (Inherited aplastic anemia) هو مجموعة من الاضطرابات الجينية النادرة التي تؤدي إلى فشل النخاع العظمي في إنتاج كميات كافية من خلايا الدم الثلاث: الكريات الحمراء، والكريات البيضاء، والصفائح الدموية. تشير مدونة حياة الطبية إلى أن هذه الحالات تظهر غالباً في سن الطفولة، وتتطلب نهجاً تشخيصياً وعلاجياً يختلف تماماً عن الأنواع المكتسبة من فقر الدم، نظراً لارتباطها المباشر بطفرات جينية موروثة تؤثر على استقرار الحمض النووي داخل الخلايا الجذعية.
ما هو فقر الدم اللاتنسجي الوراثي؟
يُعرف فقر الدم اللاتنسجي الوراثي طبياً بأنه متلازمة فشل نخاع عظمي بنيوية تنتج عن خلل في الجينات المسؤولة عن إصلاح الحمض النووي أو صيانة التيلوميرات. يؤكد موقع حياة الطبي أن هذا المرض لا يؤثر فقط على إنتاج الدم، بل قد يصاحبه تشوهات خلقية وزيادة في مخاطر الإصابة بالأورام السرطانية مستقبلاً. يعاني المرضى في هذه الحالة من نقص الكريات الشامل (Pancytopenia)، وهو ما يجعل الجسم عرضة للعدوى والنزيف المزمن وفقر الدم الشديد.
تختلف هذه المتلازمات الوراثية في مسبباتها الجينية، حيث تشمل أنواعاً شهيرة مثل فقر دم فانكوني ومتلازمة دياموند-بلاكفان. وبناءً على البيانات الصادرة عن المعاهد الوطنية للصحة (NIH)، فإن التشخيص الدقيق يتطلب فحوصات خلوية متقدمة لتمييزه عن الحالات المناعية. يعد فهم الطبيعة الجينية لهذا الاضطراب حجر الزاوية في تحديد الخيار العلاجي الأمثل، سواء كان ذلك عبر الأدوية المحفزة أو اللجوء إلى زراعة الخلايا الجذعية.
أعراض فقر الدم اللاتنسجي الوراثي
تظهر أعراض فقر الدم اللاتنسجي الوراثي بشكل تدريجي أو مفاجئ، وتتنوع حدتها بناءً على مدى انخفاض مستويات خلايا الدم في الدورة الدموية، وتشمل العلامات السريرية الأكثر شيوعاً ما يلي:
- الإرهاق البدني الحاد: شعور مستمر بالتعب والوهن حتى بدون بذل مجهود، ناتج عن نقص الأكسجين الواصل للأنسجة بسبب انخفاض الكريات الحمراء.
- شحوب البشرة الواضح: فقدان اللون الطبيعي للجلد والملتحمة، وهو علامة كلاسيكية لفقر الدم الشديد المرتبط بفشل النخاع.
- ضيق التنفس (Dyspnea): صعوبة في التنفس عند ممارسة أنشطة بسيطة مثل المشي أو صعود الدرج.
- العدوى المتكررة والخطيرة: نتيجة لنقص الكريات البيضاء (العدلات)، يصبح الجسم غير قادر على مقاومة البكتيريا والفيروسات، مما يؤدي لحمى مستمرة.
- نزيف اللثة والرعاف: سهولة حدوث النزيف من الأنف أو الفم نتيجة انخفاض مستويات الصفائح الدموية (Thrombocytopenia).
- الكدمات مجهولة السبب: ظهور بقع زرقاء أو أرجوانية على الجلد دون تعرض الشخص لارتطام أو إصابة جسدية واضحة.
- الحبرات (Petechiae): بقع حمراء صغيرة تشبه رأس الدبوس تظهر تحت الجلد، وهي ناتجة عن تسرب الدم من الأوعية الدموية الصغيرة.
- خفقان القلب: تسارع ضربات القلب في محاولة من الجسم لتعويض نقص خلايا الدم الحاملة للأكسجين.
- الدوخة والدوار: الشعور بعدم الاتزان والصداع المتكرر نتيجة ضعف التروية الدموية للدماغ.
- التشوهات الجسدية: في بعض أنواع فقر الدم اللاتنسجي الوراثي، قد يلاحظ وجود قصر في القامة، أو صغر حجم الرأس، أو عيوب في الإبهام والجهاز الهيكلي.
- تغيرات في تصبغ الجلد: ظهور بقع بلون “القهوة بالحليب” (Café au lait spots) أو مناطق من فرط التصبغ الجلدي.
- فشل النمو: تأخر ملحوظ في التطور الحركي والجسدي لدى الأطفال المصابين بالحالات الجينية المتقدمة.

أسباب فقر الدم اللاتنسجي الوراثي
ترجع أسباب فقر الدم اللاتنسجي الوراثي بشكل رئيسي إلى عيوب بنيوية في الجينات المسؤولة عن الوظائف الحيوية للخلايا الجذعية المكونة للدم، ويوضح موقع HAEAT الطبي التفاصيل الجينية التالية:
- طفرات إصلاح الحمض النووي: كما في فقر دم فانكوني، حيث تعجز الخلايا عن إصلاح الروابط المتقاطعة في الحمض النووي، مما يؤدي لموت الخلايا الجذعية مبكراً.
- خلل صيانة التيلوميرات: تؤدي الطفرات في جينات مثل (TERT) أو (TERC) إلى تقصير مفرط في نهايات الكروموسومات، مما يسبب شيخوخة مبكرة للنخاع العظمي.
- اضطراب تكوين الريبوسومات: عيوب في الجينات المسؤولة عن بناء البروتينات داخل الخلية، وهو السبب الرئيسي وراء متلازمة دياموند-بلاكفان ومتلازمة شواخمان-دايموند.
- الوراثة المندلية: ينتقل المرض عادة بصفة وراثية متنحية (يتطلب جينين معيبين من الأبوين) أو بصفة سائدة في بعض الحالات النادرة.
- الحساسية المفرطة للعوامل المؤكسدة: تصبح الخلايا في حالات فقر الدم اللاتنسجي الوراثي غير قادرة على تحمل الإجهاد التأكسدي الطبيعي، مما يسرع من فشل النخاع.
- نقص البروتينات الحامية: غياب بعض البروتينات الضرورية التي تحمي الخلايا الجذعية من التحول السرطاني أو التلف الوظيفي.
- التاريخ العائلي: وجود حالات إصابة سابقة بفشل النخاع أو سرطانات الدم المبكرة في العائلة يزيد من احتمالية وجود طفرة جينية كامنة.
متى تزور الطبيب؟
تعتبر المتابعة الطبية المبكرة أمراً حاسماً، حيث تشير مدونة HAEAT الطبية إلى أن التدخل السريع يمكن أن يمنع حدوث مضاعفات خطيرة مثل النزيف الدماغي أو الإنتان الدموي. يجب استشارة أخصائي أمراض الدم فور ظهور أي علامات تدل على ضعف كفاءة النخاع العظمي.
البالغون
بالنسبة للبالغين، يجب التوجه للطبيب إذا ظهرت أعراض إرهاق لا تزول بالراحة، أو عند ملاحظة نزيف غير معتاد أثناء تنظيف الأسنان أو الحلاقة. تؤكد مجلة حياة الطبية أن بعض أنواع فقر الدم اللاتنسجي الوراثي قد تظل كامنة وتظهر في العقد الثاني أو الثالث من العمر، وغالباً ما يتم الخلط بينها وبين الأنواع المكتسبة إذا لم يتم إجراء الفحوصات الجينية المتخصصة.
الأطفال
يجب على الآباء مراقبة أي تأخر في النمو أو شحوب مستمر لدى أطفالهم. إذا كان الطفل يصاب بالعدوى بشكل متكرر وغير طبيعي، أو إذا ظهرت عليه علامات جسدية مثل صغر حجم العينين أو تشوهات الإبهام، فإن الفحص الفوري لـ فقر الدم اللاتنسجي الوراثي يصبح ضرورة قصوى. وفقاً لـ بوابة HAEAT الطبية، فإن الكشف المبكر يمنح الأطباء فرصة أفضل للتخطيط لعملية زراعة النخاع قبل تضرر أعضاء الجسم الأخرى.
دور الذكاء الاصطناعي في تحليل الأنماط الظاهرية للكشف المبكر
تساهم تقنيات الذكاء الاصطناعي حالياً في ثورة تشخيصية؛ حيث يتم استخدام خوارزميات تحليل الصور للتعرف على الأنماط الظاهرية الدقيقة (مثل ملامح الوجه وتشوهات الأطراف البسيطة) المرتبطة بمتلازمات فشل النخاع. يمكن لهذه الأنظمة الربط بين البيانات السريرية ونتائج التسلسل الجيني لتوقع سرعة تدهور الحالة الصحية للمريض، مما يتيح للأطباء اتخاذ قرارات استباقية بشأن العلاج الجيني أو التدخل الجراحي.
عوامل خطر الإصابة بـ فقر الدم اللاتنسجي الوراثي
تتمحور عوامل الخطر المتعلقة بمرض فقر الدم اللاتنسجي الوراثي حول المحددات الجينية والتاريخ العائلي بشكل أساسي، حيث أن المرض ليس نتاجاً لعوامل بيئية مكتسبة بل هو خلل بنيوي أصيل. وتتضمن أبرز هذه العوامل ما يلي:
- التاريخ العائلي الإيجابي: وجود صلة قرابة من الدرجة الأولى لأشخاص عانوا من فشل النخاع العظمي أو ابيضاض الدم (Leukemia) في سن مبكرة.
- زواج الأقارب: تزداد احتمالية انتقال الطفرات الوراثية المتنحية في المجتمعات التي يكثر فيها زواج الأقارب، مما يرفع نسب الإصابة بفقر دم فانكوني.
- الاضطرابات الجينية المعروفة: حمل الأبوين لسمات جينية مرتبطة بخلل التيلوميرات يزيد من خطر ولادة أطفال مصابين بحالات فقر الدم اللاتنسجي الوراثي.
- العيوب الخلقية المصاحبة: وجود تشوهات في الهيكل العظمي أو الكلى أو الجلد منذ الولادة يعد مؤشراً قوياً على وجود استعداد جيني لفشل النخاع اللاحق.
- الجنس والعرق: تشير بعض الإحصائيات الصادرة عن مستشفى “جونز هوبكنز” إلى تباين طفيف في انتشار بعض المتلازمات الوراثية بين مجموعات عرقية محددة، وإن كان المرض يصيب كافة الأعراق.
- التعرض للمواد الكيميائية (عامل محفز): في الأشخاص الذين لديهم استعداد وراثي، قد يؤدي التعرض لبعض السموم البيئية إلى تسريع ظهور أعراض فقر الدم اللاتنسجي الوراثي.
مضاعفات فقر الدم اللاتنسجي الوراثي
تعتبر مضاعفات فقر الدم اللاتنسجي الوراثي مهددة للحياة إذا لم يتم إدارتها طبياً بشكل صارم، نظراً للطبيعة التقدمية للمرض وتأثيره الشامل على الجهاز المناعي والدموي، وتشمل:
- الإنتان الدموي الصاعق: نتيجة النقص الحاد في الكريات البيضاء، يصبح المريض عرضة لعدوى بكتيرية وفطرية لا تستجيب للمضادات الحيوية التقليدية.
- النزيف الداخلي الحاد: انخفاض الصفائح الدموية لمستويات حرجة قد يؤدي لنزيف تلقائي في الدماغ أو الجهاز الهضمي.
- متلازمة خلل التنسج النقوي (MDS): وهي حالة ما قبل سرطانية حيث يبدأ النخاع في إنتاج خلايا مشوهة وغير وظيفية.
- التحول إلى ابيضاض الدم الحاد: يواجه مرضى فقر الدم اللاتنسجي الوراثي مخاطر مرتفعة جداً للإصابة بمرض اللوكيميا النخاعية الحادة (AML).
- فشل القلب الاحتقاني: ناتج عن الإجهاد المزمن لعضلة القلب بسبب فقر الدم الشديد واضطرار القلب للعمل بجهد مضاعف لضخ الأكسجين.
- تضرر الأعضاء بسبب ترسب الحديد: نتيجة لعمليات نقل الدم المتكررة، قد يتراكم الحديد في الكبد والقلب، مما يسبب قصوراً وظيفياً فيها.
- هشاشة العظام وتأخر البلوغ: تداخل المرض مع العمليات الهرمونية والنمو الطبيعي في حالات الأطفال المصابين.
الوقاية من فقر الدم اللاتنسجي الوراثي
نظراً لأن المرض وراثي المنشأ، فإن الوقاية من فقر الدم اللاتنسجي الوراثي تتركز في المقام الأول على الإجراءات الاستباقية الجينية والتخطيط الأسري السليم، وتتمثل في:
- الفحص الوراثي قبل الزواج: إجراء اختبارات التسلسل الجيني للأزواج الذين لديهم تاريخ عائلي مع أمراض الدم للكشف عن الطفرات الكامنة.
- التشخيص الوراثي قبل الانغراس (PGD): في حالات التلقيح الاصطناعي، يمكن فحص الأجنة جينياً لاختيار الأجنة السليمة قبل نقلها للرحم.
- الاستشارة الجينية المتخصصة: توفير معلومات دقيقة للعائلات المصابة حول احتمالات تكرار الإصابة في الأبناء المستقبليين.
- المراقبة الدورية للأشقاء: في حال إصابة طفل، يجب فحص جميع الأشقاء دورياً للكشف عن أي بوادر أولية لفشل النخاع العظمي.
- تجنب المحفزات البيئية: تقليل التعرض للأشعة والمواد الكيميائية التي قد تسرع من تدهور الخلايا الجذعية لدى الحاملين للمرض.
- التوعية المجتمعية: رفع مستوى الوعي حول مخاطر زواج الأقارب في العائلات التي تحمل جينات فقر الدم اللاتنسجي الوراثي.
تشخيص فقر الدم اللاتنسجي الوراثي
يتطلب تشخيص فقر الدم اللاتنسجي الوراثي نهجاً متعدد التخصصات يجمع بين التحاليل المخبرية التقليدية والتقنيات الجينية الجزيئية المتقدمة لضمان الدقة:
- تعداد الدم الكامل (CBC): للكشف عن نقص الكريات الشامل وتحديد شدة فقر الدم ونقص الصفائح.
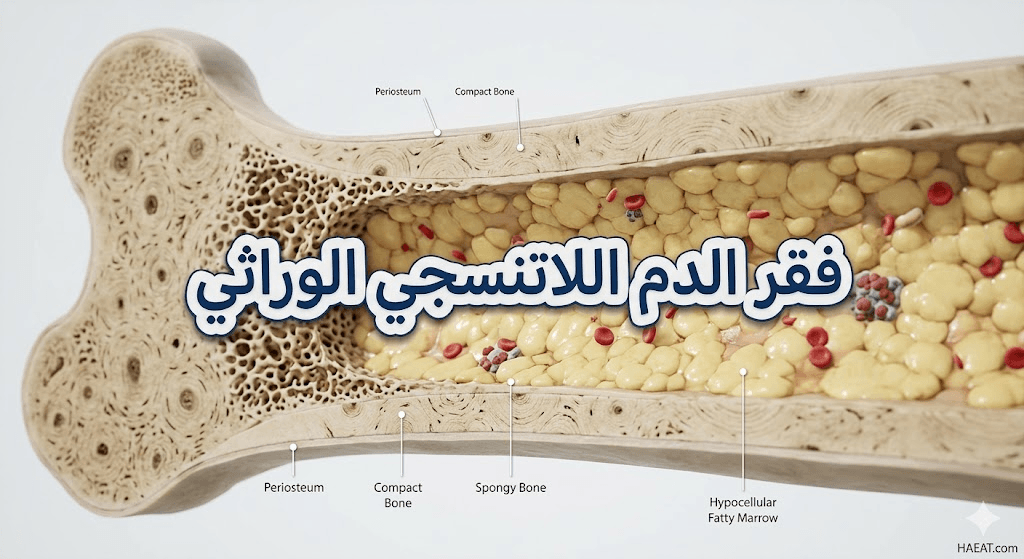
- خزعة وفحص نخاع العظم: فحص عينة من النخاع لتقييم مدى انخفاض الخلايا (Hypocellularity) واستبعاد الأمراض السرطانية الأخرى.
- اختبار تكسر الكروموسومات (Chromosome Breakage Test): وهو المعيار الذهبي لتشخيص فقر دم فانكوني، حيث تُعرض الخلايا لمواد كيميائية لمراقبة قدرتها على إصلاح الحمض النووي.
- قياس طول التيلوميرات: يتم استخدام تقنية (Flow-FISH) لتحديد ما إذا كانت نهايات الكروموسومات أقصر من المعدل الطبيعي للعمر.
- التسلسل الجيني للجيل القادم (NGS): مسح شامل لمئات الجينات المرتبطة بـ فقر الدم اللاتنسجي الوراثي لتحديد الطفرة المسؤولة بدقة.
- فحوصات وظائف الأعضاء: تقييم وظائف الكبد والكلى والقلب لتحديد مدى تأثير المرض ومراقبة المضاعفات المحتملة.
علاج فقر الدم اللاتنسجي الوراثي
يهدف علاج فقر الدم اللاتنسجي الوراثي إلى استعادة إنتاج خلايا الدم ومنع المضاعفات، ويتراوح العلاج بين المراقبة اللصيقة والتدخلات الجذرية مثل زراعة النخاع.
نمط الحياة والعلاجات المنزلية
لا يمكن علاج فقر الدم اللاتنسجي الوراثي عبر تغيير نمط الحياة وحده، ولكن يمكن تحسين جودة الحياة من خلال:
- تجنب الرياضات العنيفة: للوقاية من خطر النزيف الداخلي بسبب نقص الصفائح.
- الحفاظ على نظافة صارمة: لتقليل فرص الإصابة بالعدوى الجرثومية، بما في ذلك غسل اليدين المتكرر وتجنب الزحام.
- التغذية المتوازنة: التركيز على الأطعمة الغنية بالمعادن مع تجنب الأطعمة النيئة التي قد تحمل بكتيريا ضارة.
الأدوية والعلاجات المناعية
تُستخدم الأدوية كحلول مؤقتة أو داعمة، ووفقاً للجمعية الأمريكية لأمراض الدم (ASH)، فإن الاستجابة للعلاجات المناعية في الحالات الوراثية تكون أقل فاعلية مقارنة بالحالات المكتسبة.
بروتوكولات العلاج للبالغين
يعتمد علاج البالغين المصابين بـ فقر الدم اللاتنسجي الوراثي على:
- الأندروجينات (الهرمونات الذكرية): مثل الدانازول، والتي قد تساعد في تحفيز إنتاج الكريات الحمراء وإطالة التيلوميرات في بعض الحالات.
- عوامل تحفيز النمو: مثل (G-CSF) لزيادة عدد الكريات البيضاء وتقليل مخاطر العدوى.
- أدوية خلب الحديد: للتخلص من فائض الحديد الناتج عن نقل الدم المتكرر.
بروتوكولات العلاج للأطفال
بالنسبة للأطفال، يتم التركيز بشكل أكبر على الحلول الجذرية:
- زراعة الخلايا الجذعية المكونة للدم: هي الخيار العلاجي الوحيد الشافي، ويفضل أن يكون المتبرع شقيقاً مطابقاً تماماً.
- العلاج الداعم المكثف: بما في ذلك نقل الصفائح والدم المشع (Leukoreduced) لتجنب التحسس المناعي قبل الزراعة.
تطبيقات تقنية كريسبر (CRISPR) في تصحيح طفرات النخاع
تبرز تقنية تحرير الجينات (CRISPR-Cas9) كأمل ثوري في علاج فقر الدم اللاتنسجي الوراثي. تتيح هذه التقنية للأطباء استخراج الخلايا الجذعية من المريض، وتصحيح الطفرة الجينية المعيبة في المختبر، ثم إعادة زرعها مرة أخرى. هذا النهج يلغي الحاجة إلى متبرع مطابق ويقضي على مخاطر “مرض رفض العائل” (GVHD)، مما يمثل قفزة نوعية في الطب الشخصي.
زراعة النخاع العظمي الموجهة بالبيانات الضخمة
يتم حالياً تطوير أنظمة ذكاء اصطناعي قادرة على تحليل مليارات البيانات من سجلات المتبرعين العالمية لمطابقة المرضى مع أفضل المتبرعين الممكنين، ليس فقط بناءً على تطابق الأنسجة التقليدي (HLA)، بل وأيضاً بناءً على التوافق الجيني الدقيق لتقليل نسب الفشل المناعي بعد العملية. تساهم هذه التقنية في تحسين معدلات البقاء على قيد الحياة لمرضى فقر الدم اللاتنسجي الوراثي بشكل ملحوظ.

الطب البديل وفقر الدم اللاتنسجي الوراثي
يجب التأكيد على أن الطب البديل لا يمكن أن يكون بديلاً للعلاجات الطبية الجذرية لمرض فقر الدم اللاتنسجي الوراثي، بل يُستخدم كنهج تكميلي لتحسين جودة الحياة وتخفيف الآثار الجانبية للأدوية القوية:
- العلاج بالوخز بالإبر: قد يساعد في تخفيف الغثيان والآلام المزمنة المصاحبة لعمليات نقل الدم المتكررة أو العلاج الكيميائي التحضيري للزراعة.
- المكملات المضادة للأكسدة: مثل فيتامين E، مع ضرورة استشارة الطبيب لتجنب تداخلها مع استقرار الحمض النووي في الخلايا.
- تقنيات الاسترخاء والتأمل: تساهم في تقليل مستويات الكورتيزول، مما يحسن من الحالة النفسية العامة للمريض الذي يعاني من ضغوط مزمنة.
- العلاج بالأعشاب المحفزة للشهية: لمواجهة فقدان الوزن الناتج عن المرض، ولكن يجب تجنب الأعشاب التي قد تؤثر على وظائف الكبد.
- اليوجا اللطيفة: تساعد في الحفاظ على مرونة المفاصل دون إجهاد النخاع العظمي أو المخاطرة بالنزيف.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع مرض فقر الدم اللاتنسجي الوراثي تخطيطاً دقيقاً لكل زيارة طبية لضمان الحصول على أقصى فائدة من الوقت المتاح مع الأخصائي.
ما الذي يمكنك فعله؟
- تدوين سجل الأعراض: سجل بدقة مرات حدوث النزيف، نوبات الحمى، أو فترات الإرهاق غير المبرر.
- جمع التاريخ العائلي: ابحث في شجرة العائلة عن أي حالات إجهاض متكرر مجهول السبب أو وفيات مبكرة بسبب أمراض الدم.
- قائمة الأدوية الحالية: أحضر قائمة بكافة الأدوية والمكملات التي يتناولها المصاب بـ فقر الدم اللاتنسجي الوراثي.
ما الذي تتوقعه من الطبيب؟
سوف يقوم الطبيب بطرح أسئلة حول توقيت ظهور الأعراض الأولى، وهل هناك تشوهات جسدية لوحظت عند الولادة. كما سيشرح بالتفصيل مخاطر التحول لسرطان الدم وضرورة المراقبة الجينية الدورية.
استخدام تطبيقات المراقبة الصحية عن بُعد في توثيق الأعراض
تتيح التقنيات الحديثة حالياً استخدام تطبيقات متخصصة مرتبطة بذكاء اصطناعي لتحليل تغيرات لون الجلد (عبر الكاميرا) لاكتشاف الشحوب أو اليرقان المبكر، وإرسال تنبيهات فورية للفريق الطبي قبل تدهور الحالة الصحية لمريض فقر الدم اللاتنسجي الوراثي.
مراحل الشفاء من فقر الدم اللاتنسجي الوراثي
الشفاء التام في حالات فقر الدم اللاتنسجي الوراثي يرتبط غالباً بنجاح زراعة النخاع العظمي، وتمر هذه العملية بمراحل دقيقة:
- المرحلة الأولى (التحضير): تشمل العلاج الكيميائي لتصفية النخاع القديم، وتستغرق من 7 إلى 10 أيام.
- المرحلة الثانية (الانغراس): تبدأ الخلايا الجذعية الجديدة في الوصول للنخاع والبدء في إنتاج الدم، وتستغرق عادة 2-4 أسابيع.
- المرحلة الثالثة (التعافي المناعي): وهي المرحلة الأحرى حيث يكون الجسم عرضة للعدوى، وتستمر لمدة 100 يوم بعد الزراعة.
- المرحلة الرابعة (الاستقرار): العودة التدريجية للحياة الطبيعية مع مراقبة وظائف النخاع شهرياً خلال السنة الأولى.
الأنواع الشائعة لفقر الدم اللاتنسجي الوراثي
يضم فقر الدم اللاتنسجي الوراثي عدة متلازمات تختلف في جيناتها وأعراضها الجسدية، وأبرزها:
- فقر دم فانكوني (Fanconi Anemia): النوع الأكثر شيوعاً، ويتميز بتكسر الكروموسومات وتشوهات في الأطراف.
- متلازمة دياموند-بلاكفان (DBA): تؤثر بشكل رئيسي على إنتاج الكريات الحمراء وتظهر في السنة الأولى من العمر.
- خلل التقرن الخلقي (Dyskeratosis Congenita): يتميز بتغيرات في الأظافر، بقع في الفم، وقصر التيلوميرات.
- متلازمة شواخمان-دايموند: ترتبط بفشل النخاع وقصور في وظائف البنكرياس.
الفروقات الجينية الدقيقة بين الأنواع المختلفة لـ فقر الدم اللاتنسجي الوراثي
تكمن الفروقات في الآلية الجزيئية؛ فبينما يركز فقر دم فانكوني على عيوب إصلاح الروابط المتقاطعة للحمض النووي، نجد أن متلازمة دياموند-بلاكفان تنبع من عيوب في تكوين الريبوسومات (مصانع البروتين). فهم هذه الفروق ضروري جداً لأن بعض المصابين بـ فقر الدم اللاتنسجي الوراثي قد يستجيبون للعلاجات الهرمونية، بينما يحتاج البعض الآخر لزراعة فورية لتجنب الفشل العضوي.
التأثير النفسي والاجتماعي طويل الأمد على العائلات المصابة
يفرض العيش مع فقر الدم اللاتنسجي الوراثي عبئاً نفسياً هائلاً؛ حيث تعاني العائلات من “قلق الانتظار” لنتائج فحوصات الدم الدورية. يحتاج المرضى، وخاصة الأطفال، إلى دعم نفسي لمواجهة الشعور بالاختلاف بسبب التشوهات الجسدية أو العزلة المفروضة لتجنب العدوى. تساهم مجموعات الدعم المتخصصة في تخفيف هذا العبء عبر مشاركة التجارب الناجحة في التعايش.
التغذية العلاجية المتخصصة لمرضى فشل النخاع الوراثي
يجب أن يتبع مريض فقر الدم اللاتنسجي الوراثي نظاماً غذائياً يسمى “نظام قلة العدلات” (Neutropenic Diet) عند انخفاض المناعة، والذي يتضمن:
- تجنب الخضروات والفواكه غير المقشرة: لتقليل مخاطر البكتيريا والتربة.
- الطهي الجيد للحوم: لضمان قتل كافة الميكروبات.
- التركيز على الأطعمة الغنية بالفولات: لدعم إنتاج خلايا الدم الحمراء المتبقية.
- تجنب المكملات العالية بالحديد: إلا تحت إشراف طبي، لتفادي التسمم بالحديد الناتج عن نقل الدم.
التطورات العالمية في أبحاث العلاج الجيني (2024-2026)
تشهد الفترة الحالية (2024-2026) طفرة في التجارب السريرية للعلاجات الجينية الموجهة لمرض فقر الدم اللاتنسجي الوراثي. يتم الآن اختبار نواقل فيروسية “حميدة” قادرة على إدخال نسخ سليمة من جينات (FANCA) أو (TERT) مباشرة إلى الخلايا الجذعية للمريض. وفقاً لنتائج أولية من “كليفلاند كلينك”، أظهرت هذه العلاجات قدرة على استعادة وظيفة النخاع بنسبة تصل إلى 60% في بعض الحالات التجريبية دون الحاجة لمتبرع خارجي.
خرافات شائعة حول فقر الدم اللاتنسجي الوراثي
- الخرافة: المرض معدٍ ويمكن أن ينتقل عبر اللمس.
- الحقيقة: فقر الدم اللاتنسجي الوراثي هو اضطراب جيني داخلي ولا يمكن أن ينتقل من شخص لآخر بأي شكل من أشكال الاتصال الجسدي.
- الخرافة: تناول الكبدة والعسل الأسود يشفي من فشل النخاع الوراثي.
- الحقيقة: هذه الأطعمة تفيد في فقر الدم الناتج عن نقص التغذية، لكنها لا تملك تأثيراً على النخاع العظمي التالف جينياً.
- الخرافة: زراعة النخاع تعني الشفاء الفوري من كل الأعراض.
- الحقيقة: الزراعة هي بداية رحلة تعافٍ طويلة تتطلب سنوات من المتابعة لضمان عدم رفض الجسم للخلايا الجديدة.
نصائح ذهبية من “مدونة حياة الطبية” 💡
بناءً على الخبرات السريرية الطويلة، نقدم للمتعايشين مع فقر الدم اللاتنسجي الوراثي هذه التوصيات:
- الالتزام بجدول التطعيمات: ولكن فقط “اللقاحات غير الحية” بعد استشارة الطبيب.
- العناية الفائقة بالأسنان: استخدم فرشاة ناعمة جداً لتجنب نزيف اللثة الذي قد يتحول لمصدر عدوى.
- التوثيق الجيني الكامل: احتفظ بنسخة من تقرير التسلسل الجيني، فهو “خارطة الطريق” لعلاجك مدى الحياة.
- الدعم التعليمي: تأكد من إبلاغ مدرسة الطفل بحالته لتوفير بيئة آمنة تضمن له التعليم دون التعرض لإصابات جسدية.
أسئلة شائعة (PAA)
هل يمكن لمريض فقر الدم اللاتنسجي الوراثي الزواج والإنجاب؟
نعم، مع وجود تقدم في تقنيات المساعدة على الإنجاب وفحص الأجنة جينياً، يمكن للمرضى تكوين عائلات وإنجاب أطفال أصحاء لا يحملون المرض.
كم تبلغ تكلفة عملية زراعة النخاع العظمي؟
تختلف التكلفة عالمياً وتتراوح ما بين 150,000 إلى 500,000 دولار، ولكن العديد من الدول توفر مراكز وطنية تدعم هذه العمليات المعقدة.
ما هي فرص النجاة طويلة الأمد بعد التشخيص؟
مع العلاجات الحديثة وزراعة النخاع من متبرع مطابق، تتجاوز نسب النجاح والبقاء على قيد الحياة 80% في المراكز المتقدمة.
الخاتمة
يظل فقر الدم اللاتنسجي الوراثي تحدياً طبياً كبيراً يتطلب صبراً ومتابعة دقيقة، إلا أن الأمل يلوح في الأفق مع التطورات المذهلة في الهندسة الجينية والذكاء الاصطناعي. إن التشخيص المبكر والفهم العميق لنوع الطفرة الجينية هما مفتاح الانتقال من مرحلة “إدارة المرض” إلى مرحلة “الشفاء التام”.