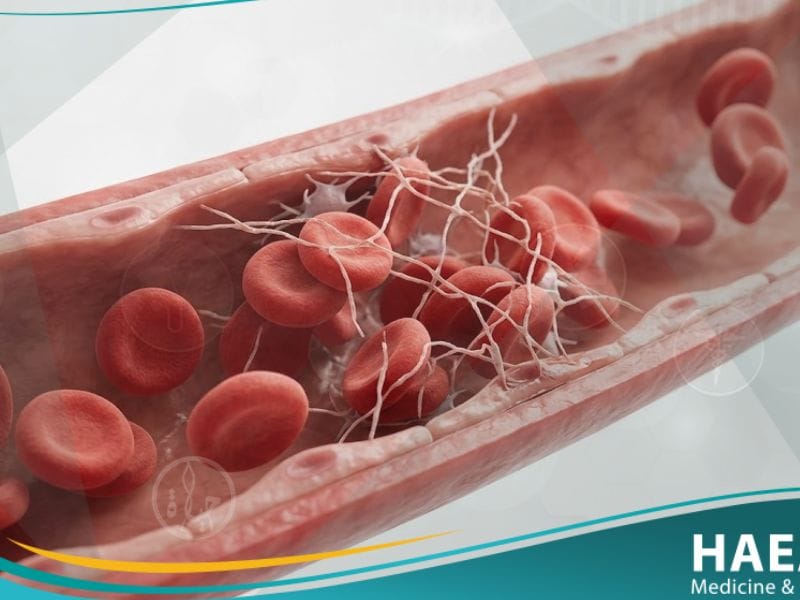
يُعد داء كريسماس (Christmas disease) أحد الاضطرابات النزفية الوراثية النادرة التي تؤثر على قدرة الجسم على تكوين جلطات الدم بشكل صحيح. توضح مدونة حياة الطبية أن هذا المرض، المعروف سريرياً بالهيموفيليا “ب”، ينتج عن نقص في بروتين حيوي يُعرف بعامل التخثر التاسع.
يتسبب هذا النقص في استمرار النزيف لفترات أطول بعد الإصابات أو العمليات الجراحية، وفي الحالات الشديدة، قد يحدث نزيف تلقائي داخل المفاصل والعضلات. يتطلب التعامل مع هذه الحالة فهماً عميقاً للبروتوكولات العلاجية الحديثة لضمان جودة حياة طبيعية للمصابين.
ما هو داء كريسماس؟
داء كريسماس هو اضطراب جيني يؤدي إلى نقص أو غياب عامل التخثر التاسع (Factor IX)، وهو بروتين ضروري لعملية تخثر الدم الطبيعية. يؤكد موقع حياة الطبي أن المرض سُمي بهذا الاسم نسبة إلى “ستيفن كريسماس”، أول مريض تم تشخيص إصابته بنقص هذا العامل النوعي في عام 1952.
تتمثل الوظيفة الأساسية لعامل التخثر التاسع في تنشيط سلسلة من التفاعلات الكيميائية الحيوية التي تؤدي في النهاية إلى تشكيل خيوط الفايبرين، وهي “الشبكة” التي تمسك مكونات الجلطة معاً. في غياب هذا العامل، يفشل الجسم في سد الأوعية الدموية الممزقة بكفاءة، مما يجعل النزيف يشكل خطراً صحياً مستمراً.

أعراض داء كريسماس
تتفاوت حدة الأعراض بناءً على مستويات عامل التخثر التاسع في الدم؛ فكلما انخفضت النسبة، زادت خطورة النزيف التلقائي. تشمل قائمة الأعراض الأكثر شيوعاً وفقاً للتقارير السريرية ما يلي:
- نزيف المفاصل (Hemarthrosis): وهو العرض الأكثر تميزاً، حيث يشعر المريض بتورم، سخونة، وألم شديد في الركبتين، المرفقين، أو الكاحلين.
- الكدمات العميقة والواسعة: ظهور بقع زرقاء أو أرجوانية كبيرة تحت الجلد نتيجة نزيف الأنسجة الرخوة بعد إصابات طفيفة جداً.
- النزيف الأنفي المتكرر: حدوث رعاف مستمر يصعب إيقافه بالطرق التقليدية ويستمر لفترات طويلة.
- نزيف الفم واللثة: يظهر بوضوح عند فقدان الأسنان اللبنية لدى الأطفال أو بعد الخضوع لإجراءات طب الأسنان البسيطة.
- وجود دم في البول أو البراز: ناتج عن نزيف داخلي في الجهاز الهضمي أو المسالك البولية، وهو ما يتطلب تدخلاً طبياً فورياً.
- نزيف ما بعد التحصينات: ظهور تورم كبير أو نزيف مستمر في موقع حقن اللقاحات تحت الجلد أو في العضل.
- النزيف المطول بعد الجروح: استمرار تدفق الدم من الجروح الصغيرة لفترات تتجاوز المعدل الطبيعي بكثير.
- الصداع الشديد والمفاجئ: قد يكون مؤشراً خطيراً على حدوث نزيف داخل الجمجمة، وهو من المضاعفات المهددة للحياة.

أسباب داء كريسماس
ينشأ داء كريسماس نتيجة طفرة جينية في الجين المسؤول عن إنتاج عامل التخثر التاسع، والموجود على الكروموسوم الجنسي (X). يشير موقع HAEAT الطبي إلى أن نمط الوراثة المرتبط بالجنس يفسر سبب إصابة الذكور بالمرض غالباً بينما تكون الإناث حاملات للجين.
- الوراثة المرتبطة بالكروموسوم X: بما أن الذكور لديهم كروموسوم X واحد فقط، فإن وجود طفرة واحدة كفيل بإحداث المرض.
- الإناث الحاملات للجين: تمتلك الأنثى كروموسومين X، لذا إذا كان أحدهما يحمل الطفرة، فإن الكروموسوم الآخر يعوض النقص غالباً، لكنهن ينقلن الجين لأطفالهن.
- الطفرات العفوية: في حوالي 30% من الحالات، لا يوجد تاريخ عائلي للمرض، حيث تحدث الطفرة الجينية بشكل مفاجئ أثناء التطور الجنيني.
- الخلل في ترميز البروتين: تؤدي الطفرة إلى إنتاج بروتين غير فعال أو منع إنتاجه تماماً في الكبد، وهو المصنع الرئيسي لعوامل التخثر.
- التأثير العرقي والجغرافي: لا يرتبط المرض بعرق معين، بل ينتشر عالمياً بمعدل إصابة واحد لكل 25,000 إلى 30,000 مولود ذكر.
متى تزور الطبيب؟
تعتبر مراقبة الحالة الصحية لمرضى داء كريسماس عملية مستمرة، حيث يتداخل النزيف المفاجئ مع الأنشطة اليومية، مما يستدعي تقييماً طبياً فورياً في حالات معينة. تختلف المؤشرات التي تتطلب التدخل السريع بين الفئات العمرية المختلفة لضمان تلافي المضاعفات المستديمة.
العلامات التحذيرية عند البالغين
يجب على البالغين المصابين بنقص العامل التاسع التوجه فوراً للطوارئ في حال ظهور أعراض تدل على نزيف داخلي أو عصبي. تشمل هذه العلامات الصداع الحاد والمستمر، التقيؤ المتكرر، واضطراب الرؤية، والتي قد تشير إلى نزيف دماغي. كما يجب الانتباه لألم الظهر الشديد الذي قد يعكس نزيفاً في العضلات الحرقفية (Iliopsoas) أو ألم المفاصل الذي لا يستجيب للعلاجات المنزلية الأولية.
المؤشرات الحرجة عند الرضع والأطفال
بالنسبة للأطفال، يوصي الخبراء بمراقبة أي تورم غير مبرر في المفاصل أو رفض الطفل لتحريك أحد أطرافه، مما قد يدل على نزيف مفصلي صامت. من الضروري استشارة الطبيب عند تعرض الطفل لضربة في الرأس، حتى لو لم تظهر أعراض فورية، نظراً لاحتمالية النزيف المتأخر. كما يعد ظهور بقع دموية في الحفاظ أو القيء المدمم علامات تستوجب فحصاً عاجلاً في مراكز أمراض الدم المتخصصة.
دور التكنولوجيا والذكاء الاصطناعي في التنبؤ بنوبات النزيف
تقترح الرؤى الحديثة في “بوابة حياة الطبية” استخدام تطبيقات الهواتف الذكية المرتبطة بخوارزميات الذكاء الاصطناعي لمراقبة النشاط البدني للمريض. (وفقاً لـ [National Institutes of Health (NIH)]، فإن تحليل أنماط الحركة ونبضات القلب يمكن أن يتنبأ ببداية التهاب المفاصل الناتج عن النزيف المجهري قبل شعور المريض بالألم السريري). تتيح هذه التقنيات للمرضى أخذ الجرعات الوقائية في الوقت المثالي، مما يقلل من تضرر الأنسجة على المدى الطويل.
عوامل خطر الإصابة بـ داء كريسماس
تعد عوامل الخطر المرتبطة بهذا الاضطراب محدودة وواضحة نظراً لطبيعته الجينية الصرفة، إلا أن فهمها يساعد في التنبؤ باحتمالية ظهور المرض في الأجيال القادمة. تشمل هذه العوامل ما يلي:
- الجنس (الذكور): يمثل الذكور الفئة الأكثر عرضة للإصابة بالأعراض السريرية لـ داء كريسماس بسبب امتلاكهم كروموسوم X واحداً فقط.
- التاريخ العائلي: وجود إصابات سابقة بالهيموفيليا ب في شجرة العائلة يزيد من احتمالية انتقال الجين الطافر من الأم الحاملة إلى أبنائها.
- حالة الأم الوراثية: تعتبر المرأة التي تحمل جين المرض المصدر الرئيسي لانتقاله، حيث تبلغ نسبة احتمالية إنجاب ابن مصاب 50% في كل حمل.
- زواج الأقارب: في المجتمعات التي يكثر فيها زواج الأقارب، قد تزداد احتمالية ظهور الاضطرابات الوراثية النادرة بشكل عام وتجمع الطفرات الجينية.
- الجنس (الإناث في حالات نادرة): قد تظهر أعراض خفيفة لـ داء كريسماس لدى النساء الحاملات للجين إذا كان لديهن انخفاض ملحوظ في مستويات العامل التاسع (أقل من 40%).
مضاعفات داء كريسماس
إذا لم يتم تدبير المرض بشكل استباقي، فقد يؤدي النزيف المتكرر إلى أضرار هيكلية ووظيفية دائمة في الجسم. تبرز مجلة حياة الطبية أهمية الوعي بالمضاعفات التالية:
- تلف المفاصل المزمن (Arthropathy): يؤدي النزيف المتكرر داخل المفصل إلى تآكل الغضاريف، مما يسبب التهاب مفاصل مزمناً وتيبساً قد ينتهي بالإعاقة الحركية.
- تكون الأجسام المضادة (Inhibitors): قد يطور الجهاز المناعي أجساماً مضادة ضد العامل التاسع التعويضي، مما يجعل العلاج التقليدي غير فعال ويتطلب بروتوكولات معقدة.
- النزيف الداخلي العميق: قد يحدث نزيف في العضلات الكبيرة يؤدي إلى ضغط على الأعصاب وفقدان الإحساس أو الوظيفة في الأطراف (متلازمة الحيز).
- العدوى الفيروسية: تاريخياً، كان المرضى عرضة للفيروسات المنقولة عبر الدم (مثل الكبد الوبائي)، لكن التقنيات الحديثة في تصنيع العوامل جعلت هذا الخطر شبه منعدم.
- نزيف الجهاز العصبي المركزي: يمثل النزيف الدماغي أخطر المضاعفات، حيث يؤدي إلى تلف دائم في خلايا الدماغ، فقدان الوعي، أو الوفاة إذا لم يتم إسعافه فوراً.
- التأثيرات النفسية: يعاني بعض المرضى من القلق والاكتئاب نتيجة القيود الجسدية والخوف المستمر من حدوث نوبات نزيف مفاجئة.
الوقاية من داء كريسماس
نظراً لأن داء كريسماس حالة وراثية، فإن الوقاية تركز بشكل أساسي على الجانب الجيني والحد من تكرار النزيف الفعلي للمصابين. تشمل استراتيجيات الوقاية ما يلي:
- الاستشارة الوراثية: خضوع الأزواج الذين لديهم تاريخ عائلي للمرض لفحوصات قبل الزواج لتحديد احتمالات انتقال الطفرة للأبناء.
- الفحص الجنيني (Prenatal Testing): يمكن إجراء فحوصات للمشيمة أو السائل الأمينوسي خلال الحمل لتشخيص إصابة الجنين بـ داء كريسماس مبكراً.
- العلاج الوقائي (Prophylaxis): الالتزام بجدول منتظم لحقن العامل التاسع لمنع حدوث النزيف قبل وقوعه، بدلاً من العلاج عند الحاجة فقط.
- تجنب الأدوية المسيلة للدم: الابتعاد التام عن الأسبرين ومضادات الالتهاب غير الستيرويدية (NSAIDs) التي تزيد من سيولة الدم وتفاقم النزيف.
- تعديل البيئة المحيطة: تأمين منازل الأطفال المصابين لتقليل فرص التعثر والسقوط، واستخدام معدات وقاية (مثل الخوذات) أثناء الأنشطة البدنية.
تشخيص داء كريسماس
يتطلب تشخيص هذا الاضطراب النزفي سلسلة من الاختبارات المعملية الدقيقة التي تجرى في مراكز متخصصة. (وفقاً لـ [Centers for Disease Control and Prevention (CDC)]، فإن التشخيص المبكر هو المفتاح لمنع التلف الدائم للمفاصل). تشمل خطوات التشخيص:
- اختبار زمن الثرومبوبلاستين الجزئي (aPTT): يقيس سرعة تخثر الدم؛ وفي حالات داء كريسماس، يكون هذا الزمن طويلاً بشكل ملحوظ.
- اختبار معايرة العامل التاسع (Factor IX Assay): هو الاختبار الحاسم الذي يحدد النسبة المئوية الدقيقة لنشاط العامل في الدم، مما يحدد شدة المرض.
- اختبارات زمن النزيف الأخرى: مثل زمن البروثرمبين (PT) وعد الصفائح الدموية، والتي تكون طبيعية عادةً في مرضى الهيموفيليا ب، مما يساعد في استبعاد الأمراض الأخرى.
- التنميط الجيني (Genetic Testing): تحديد الطفرة المحددة في جين F9، وهو أمر حيوي لتحديد حاملي الجين من الإناث ولتوجيه العلاج الجيني مستقبلاً.
- فحص الأجسام المضادة: يُجرى بشكل دوري للتأكد من أن جسم المريض لا يرفض العلاج التعويضي ولا يكون مثبطات تعيق عمل الدواء.
علاج داء كريسماس
يهدف علاج داء كريسماس إلى استعادة مستويات كافية من عامل التخثر التاسع لتمكين الدم من التجلط بشكل طبيعي. تطورت الخيارات العلاجية بشكل مذهل في السنوات الأخيرة لتشمل حلولاً طويلة الأمد تقلل من عدد الحقن الأسبوعية.
نمط الحياة والعلاجات المنزلية
يعتبر بروتوكول RICE (الراحة، الثلج، الضغط، والرفع) الخط الأول للتعامل المنزلي فور الشعور ببدء نزيف مفصلي. يساعد استخدام الكمادات الباردة في تضييق الأوعية الدموية، بينما يقلل الرفع من ضغط الدم في المنطقة المصابة. كما يُنصح بممارسة السباحة لتقوية العضلات المحيطة بالمفاصل دون تعريضها لضغط مباشر، مما يقلل من احتمالية الإصابات.
الأدوية والعلاجات التخصصية
يعتمد العلاج الأساسي على “العلاج التعويضي” الذي يتم عن طريق الوريد. ينقسم هذا العلاج إلى نوعين رئيسيين: العوامل المشتقة من بلازما المتبرعين (بعد معالجتها بدقة)، والعوامل “المؤتلفة” (Recombinant) المصنعة في المختبر والتي تعتبر الخيار الأول حالياً لسلامتها العالية.
بروتوكولات الحقن للبالغين
بالنسبة للبالغين المصابين بـ داء كريسماس، يتم التركيز على العلاج الوقائي الشخصي، حيث يتم حقن العامل التاسع مرتين إلى ثلاث مرات أسبوعياً، أو استخدام العوامل ذات “عمر النصف الممتد” (Extended Half-Life) التي قد تتطلب حقنة واحدة كل 10 إلى 14 يوماً. يساعد ذلك في الحفاظ على مستوى ثابت للعامل يمنع النزيف التلقائي أثناء العمل أو ممارسة الرياضة.
رعاية الأطفال وجدول الحقن الوقائي
يبدأ الأطفال غالباً العلاج الوقائي قبل حدوث أول نزيف مفصلي كبير (الوقاية الأولية). يتم تدريب الآباء على كيفية إعطاء الحقن في المنزل أو استخدام “البورت-أ-كاث” (Port-a-cath) وهو جهاز يُزرع تحت الجلد لتسهيل الوصول المتكرر للأوردة، مما يقلل من رهبة الأطفال وتوتر العائلة من عملية الحقن المستمرة.
الابتكارات التقنية في مضخات الحقن الذاتي المبرمجة
تظهر دراسات حديثة فعالية مضخات الحقن الذكي التي يمكن برمجتها لإطلاق جرعات صغيرة من عامل التخثر في أوقات محددة، مما يحاكي الإفراز الطبيعي للجسم. هذه الابتكارات تقلل من التقلبات الحادة في مستويات العامل وتوفر حماية مستقرة على مدار الساعة للمرضى الذين يعانون من أنماط نزيف صعبة.
تطبيقات مراقبة مستويات التخثر اللحظية
تستخدم بعض الأنظمة المتطورة حساسات ذكية مرتبطة بتطبيقات الهاتف لتقدير مستوى عامل التخثر في دم المريض بناءً على آخر جرعة محقونة والنشاط البدني المبذول. توفر هذه التطبيقات تنبيهات للمريض عند وصول مستوى العامل إلى “منطقة الخطر”، مما يدفعه لأخذ جرعة إضافية قبل القيام بأي مجهود بدني شاق.

الطب البديل وداء كريسماس
على الرغم من أن العلاج التعويضي هو الركيزة الأساسية، إلا أن بعض الممارسات التكميلية قد تساعد في تخفيف الأعراض الجانبية وتحسين صحة المفاصل، بشرط استشارة الطبيب لتجنب التفاعلات الدوائية الخطرة. تشمل هذه الممارسات:
- العلاج الطبيعي والفيزيائي: التركيز على تمارين التقوية منخفضة التأثير التي تحمي المفاصل من النزيف التلقائي وتزيد من مرونة الأربطة.
- الوخز بالإبر (بحذر شديد): قد يلجأ البعض له لتخفيف الألم المزمن، ولكن يجب أن يتم بيد خبير مع استخدام إبر دقيقة جداً وتحت حماية جرعة من العامل التاسع لتفادي حدوث كدمات عميقة.
- المكملات العشبية (تجنب المسيلات): يجب الابتعاد تماماً عن الثوم، الزنجبيل، والجنكة بيلوبا لأنها تزيد من سيولة الدم، والتركيز بدلاً من ذلك على المكملات التي تدعم صحة العظام مثل فيتامين د والكالسيوم.
- تقنيات الاسترخاء والتأمل: تساعد في إدارة الألم المزمن وتقليل مستويات التوتر التي قد تؤثر سلباً على إدراك المريض لشدة الأعراض.
- التغذية المضادة للالتهاب: تناول أطعمة غنية بالأوميغا 3 (من مصادر طبيعية) للمساعدة في تقليل التهابات المفاصل الناتجة عن نوبات النزيف المتكررة.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع اضطراب وراثي مثل داء كريسماس تنظيماً دقيقاً للمعلومات الصحية لضمان حصولك على أفضل خطة علاجية ممكنة خلال الزيارة الطبية.
ما الذي يمكنك فعله؟
يُنصح بالاحتفاظ بـ “سجل النزيف” الذي يدون فيه المريض تاريخ كل نوبة، موقع النزيف، وكمية جرعة العامل التي تم أخذها والاستجابة لها. كما يجب تجهيز قائمة بالأدوية والمكملات الحالية، وتدوين أي أسئلة تتعلق بالأنشطة البدنية الجديدة التي يخطط المريض للقيام بها.
ما الذي تتوقعه من الطبيب؟
سيقوم الطبيب المختص بأمراض الدم بإجراء فحص سريري للمفاصل لتقييم مدى الحركة والتأكد من عدم وجود تيبس. كما سيسأل عن عدد المرات التي احتجت فيها لجرعات “عند الطلب” بالإضافة إلى جرعاتك الوقائية، وسيناقش معك نتائج آخر فحص للأجسام المضادة (Inhibitors).
استخدام السجلات الطبية الرقمية الموحدة لتسريع الاستجابة الطارئة
تؤكد الدراسات أن استخدام السجلات الرقمية المشتركة يتيح لأطباء الطوارئ الوصول الفوري لنوع الطفرة والجرعة المناسبة لمريض داء كريسماس. (وفقاً لـ [American Society of Hematology]، فإن التوثيق الرقمي يقلل من زمن الاستجابة في حالات النزيف الحاد بنسبة تصل إلى 40%، مما يحمي المريض من المضاعفات العصبية الدائمة).
مراحل الشفاء من داء كريسماس
الشفاء في سياق الهيموفيليا “ب” لا يعني التخلص من المرض، بل التعافي من نوبات النزيف الحادة والعودة إلى الوظيفة الطبيعية. تمر هذه العملية بالمراحل التالية:
- المرحلة الحادة (0-48 ساعة): التركيز على وقف النزيف فوراً برفع مستويات العامل التاسع واستخدام بروتوكول RICE لتقليل التورم.
- مرحلة الامتصاص (2-7 أيام): يبدأ الجسم في إعادة امتصاص الدم من داخل المفصل أو العضلة؛ في هذه المرحلة، يتم الحفاظ على مستويات وقائية من العامل لمنع “إعادة النزيف”.
- مرحلة إعادة التأهيل (أسبوع فأكثر): البدء بتمارين حركية خفيفة لاستعادة مدى حركة المفصل وتجنب حدوث التيبس الدائم.
- مرحلة التقييم الوظيفي: التأكد من عودة المفصل لحالته قبل النزيف، وفي حال تكرار النزيف في نفس الموقع، قد يتم تعديل الخطة الوقائية طويلة الأمد.
الأنواع الشائعة لداء كريسماس
يُصنف داء كريسماس طبياً بناءً على النسبة المئوية لنشاط عامل التخثر في الدم مقارنة بالمعدل الطبيعي (الذي يتراوح بين 50% إلى 150%):
- الشكل الشديد (أقل من 1%): يعاني هؤلاء المرضى من نزيف تلقائي متكرر في المفاصل والعضلات دون إصابات واضحة، ويشكلون النسبة الأكبر من المراجعين للمراكز الطبية.
- الشكل المتوسط (1% إلى 5%): يحدث النزيف عادةً بعد إصابات طفيفة، ولكن قد تحدث نوبات تلقائية نادرة؛ ويتطلب هؤلاء المرضى وقاية مشددة عند الخضوع لجراحات الأسنان.
- الشكل الخفيف (أكثر من 5% إلى أقل من 40%): قد لا يتم اكتشاف المرض إلا في سن متأخرة بعد تعرض الشخص لإصابة كبيرة أو جراحة، حيث يكون النزيف المطول هو العلامة الوحيدة.
الإحصائيات العالمية والانتشار الجغرافي للمرض
يعد داء كريسماس أقل شيوعاً من الهيموفيليا “أ” بخمس مرات تقريباً، حيث يصيب ذكراً واحداً من بين كل 25,000 إلى 30,000 مولود ذكر حول العالم. تشير الإحصائيات إلى عدم وجود فروق عرقية جوهرية في معدلات الإصابة، إلا أن التحدي الأكبر يكمن في الدول النامية حيث لا تزال معدلات التشخيص منخفضة، مما يؤدي إلى وفيات مبكرة بسبب نزيف غير مُسيطر عليه.
التغذية والنشاط البدني الآمن لمرضى داء كريسماس
- الحفاظ على وزن مثالي: تعتبر السمنة عدواً لمرضى داء كريسماس لأن الوزن الزائد يضع ضغطاً هائلاً على المفاصل الضعيفة أصلاً، مما يحفز النزيف التلقائي.
- الرياضات الموصى بها: السباحة (أفضل خيار لتقوية العضلات دون ضغط)، المشي السريع، وركوب الدراجات (مع ارتداء الخوذة والواقيات).
- الرياضات المحظورة: يمنع منعاً باتاً ممارسة رياضات التلاحم مثل الملاكمة، كرة القدم الأمريكية، والمصارعة بسبب خطر النزيف الدماغي والداخلي المميت.
- فيتامين ك: على الرغم من أنه ضروري للتجلط، إلا أن نقصه ليس سبباً لـ داء كريسماس، ولكن الحفاظ على مستويات طبيعية منه يدعم الصحة العامة للتخثر.
التأثير النفسي والاجتماعي للتعايش مع داء كريسماس
التعايش مع اضطراب نزفي مزمن يفرض عبئاً نفسياً كبيراً على المريض وأسرته، خاصة في مراحل الطفولة والمراهقة حيث يشعر المريض بالاختلاف عن أقرانه. من الضروري دمج الدعم النفسي في خطة العلاج لمساعدة المرضى على تجاوز “قلق النزيف” وبناء ثقة كافية لممارسة حياة اجتماعية ومهنية ناجحة دون خوف مفرط.
التوقعات المستقبلية والعلاجات الجينية لداء كريسماس
- ثورة العلاج الجيني: وافقت الهيئات الصحية العالمية (مثل FDA) مؤخراً على أول علاج جيني لـ داء كريسماس، والذي يعتمد على استخدام ناقل فيروسي غير ضار لإدخال جين سليم إلى خلايا الكبد.
- الاستغناء عن الحقن المستمر: يهدف العلاج الجيني إلى جعل الكبد ينتج العامل التاسع بمفرده، مما قد ينهي حاجة المرضى للحقن الوريدي لسنوات طويلة.
- العوامل طويلة المفعول: استمرار تطوير جزيئات يمكنها البقاء في الدورة الدموية لفترات تصل إلى شهر، مما يحسن من جودة حياة المرضى بشكل كبير.
- العلاجات غير القائمة على العوامل: أدوية جديدة تعمل على تعديل توازن التخثر الكلي في الجسم دون الحاجة لتعويض العامل التاسع مباشرة، وهي قيد التجارب السريرية المتقدمة.
خرافات شائعة حول داء كريسماس
- خرافة: مريض داء كريسماس قد ينزف حتى الموت من خدش بسيط.
- الحقيقة: الجروح السطحية ليست الخطر الأكبر؛ الخطر الحقيقي يكمن في النزيف الداخلي (المفاصل، العضلات، الدماغ) الذي لا يمكن رؤيته.
- خرافة: المرض يختفي مع تقدم العمر.
- الحقيقة: هذا اضطراب جيني وراثي يلازم المريض طوال حياته، لكن طرق إدارته تتحسن مع نضوج المريض وتطور العلاجات.
- خرافة: المصابون لا يمكنهم ممارسة الرياضة أبداً.
- الحقيقة: الرياضة ضرورية لتقوية العضلات وحماية المفاصل، بشرط اختيار الأنواع المناسبة والالتزام بالوقاية.
نصائح ذهبية من “مدونة حياة الطبية” 💡
- لا تتجاهل “الوخز”: الشعور بالوخز أو الحرارة في المفصل هو أول علامة للنزيف؛ خذ جرعتك فوراً قبل ظهور التورم.
- بطاقة الهوية الطبية: احرص دائماً على ارتداء سوار أو حمل بطاقة توضح إصابتك بـ داء كريسماس ونوع فصيلة دمك.
- صحة الفم أولاً: حافظ على نظافة أسنانك لتجنب العمليات الجراحية في اللثة التي قد تسبب نزيفاً معقداً.
- التواصل مع المدرسة: تأكد من أن المعلمين والمدربين يعرفون حالة طفلك وكيفية التصرف في الطوارئ.
- كن عضواً في جمعية: الانضمام لجمعيات الهيموفيليا يوفر لك دعماً مجتمعياً ووصولاً لأحدث المعلومات الطبية.
أسئلة شائعة
هل يمكن للمصاب بداء كريسماس الزواج وإنجاب أطفال أصحاء؟
نعم، يمكن للمصاب الزواج. إذا كانت الزوجة غير حاملة للجين، فإن جميع الأبناء الذكور سيكونون أصحاء، بينما ستكون جميع البنات حاملات للجين (لكن غير مصابات عادةً). الاستشارة الوراثية ضرورية لتوضيح هذه الاحتمالات.
ما هي مدة النزيف الطبيعية لمريض داء كريسماس بعد إصابة بسيطة؟
في حال عدم أخذ العلاج التعويضي، قد يستمر النزيف أو يتوقف ثم يعود مجدداً (نزيف ارتدادي) لعدة أيام. الهدف من العلاج هو جعل زمن التخثر يقترب من الطبيعي (دقائق معدودة).
هل تسبب اللقاحات نزيفاً خطيراً للمصابين؟
لا، لكن يُفضل إعطاء اللقاح تحت الجلد (Subcutaneous) بدلاً من العضل لتجنب التورم الدموي، مع الضغط على موقع الحقن لمدة 5-10 دقائق على الأقل.
الخاتمة
يُعد داء كريسماس نموذجاً للاضطرابات الطبية التي تحولت من حالات مهددة للحياة إلى أمراض مزمنة يمكن إدارتها بنجاح كبير. بفضل التطور التقني في إنتاج عوامل التخثر والآفاق الواعدة للعلاج الجيني، أصبح بإمكان المصابين اليوم التطلع لمستقبل مليء بالنشاط والإنتاجية، بعيداً عن قيود النزيف المتكرر.