يُعد ضمور النخاع الشوكي (Spinal Muscular Atrophy) أحد أخطر الاضطرابات الوراثية التي تصيب الجهاز العصبي الحركي للإنسان، وهو السبب الوراثي الأول لوفيات الرضع عالمياً. توضح مدونة حياة الطبية أن هذا المرض ينجم عن فقدان تدريجي للخلايا العصبية الحركية في الحبل الشوكي، مما يسبب ضعفاً عضلياً شديداً وهزالاً يزداد مع مرور الوقت. تؤثر هذه الحالة الجينية النادرة بشكل مباشر على قدرة الفرد على المشي، والتنفس، والبلع، مما يجعلها تحدياً طبياً يتطلب رعاية متعددة التخصصات.
وفقاً للأبحاث الحديثة، فإن التشخيص المبكر لهذا الاعتلال العصبي العضلي يمثل الفارق الجوهري بين تدهور الحالة واستقرارها، خاصة مع ظهور العلاجات الجينية الثورية. تشير الإحصائيات الطبية إلى أن طفلاً واحداً من بين كل 10,000 مولود يصاب بهذا الاضطراب، مما يضع ضمور النخاع الشوكي ضمن قائمة الأمراض التي تتطلب فحصاً جينياً دقيقاً قبل الزواج وفي مراحل الحمل المبكرة.
ما هو ضمور النخاع الشوكي؟
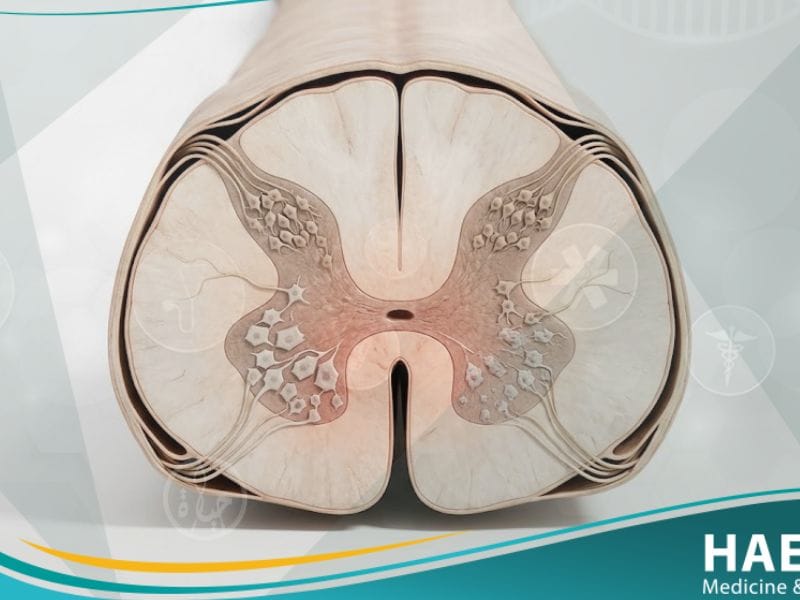
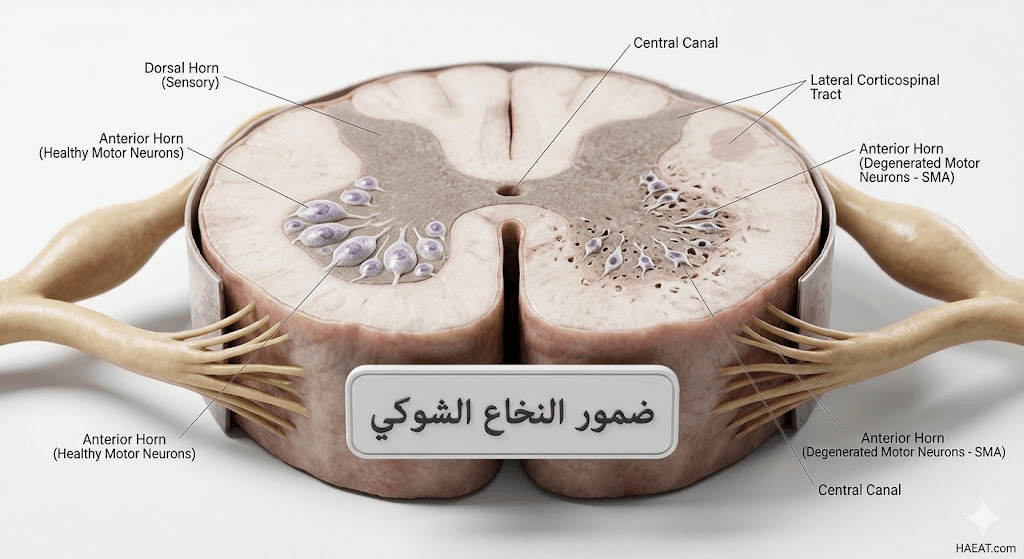
ضمور النخاع الشوكي هو اضطراب وراثي صبغي جسدي متنحٍ يتسم بتنكس الخلايا العصبية الحركية الموجودة في القرن الأمامي للنخاع الشوكي. يؤدي هذا التنكس العصبي إلى انقطاع الإشارات العصبية الواصلة من الدماغ إلى العضلات الهيكلية، مما يتسبب في ضمورها نتيجة عدم الاستخدام الوظيفي. يكمن السبب الرئيسي في نقص بروتين أساسي يسمى (Survival Motor Neuron)، وهو البروتين المسؤول عن بقاء هذه الخلايا حية ونشطة.
وفقاً لـ موقع حياة الطبي، فإن الإصابة لا تؤثر على القدرات الذهنية أو الإدراكية للمريض، بل غالباً ما يتمتع المصابون بذكاء حاد وقدرات عقلية ممتازة. تكمن المشكلة الحقيقية في أن هذا الاضطراب الجيني يهاجم العضلات القريبة من جذع الجسم (Proximal Muscles) بشكل أكثر ضراوة من العضلات البعيدة، مما يجعل التحكم في الجذع والكتفين والفخذين أول المهارات المفقودة لدى المريض.
أعراض ضمور النخاع الشوكي
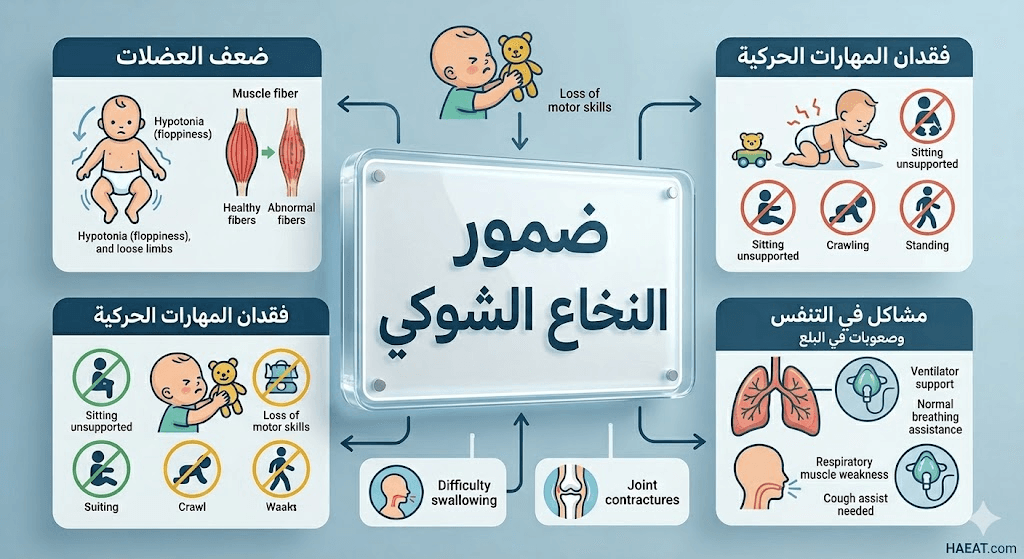
تتنوع العلامات السريرية لهذا المرض بناءً على وقت ظهوره وشدة الطفرة الجينية، وتلخصها مجلة حياة الطبية في النقاط التالية لضمان الوعي الكامل للأسر:
- ضعف عضلي متماثل يبدأ غالباً في الأطراف السفلى ويتطور ليشمل الأطراف العلوية مع تقدم الحالة.
- ارتخاء شديد في العضلات (Hypotonia) يُعرف سريرياً بمتلازمة “الطفل الرخو”، حيث يظهر الرضيع بمرونة غير طبيعية تشبه العجينة.
- صعوبات بالغة في الجهاز التنفسي ناتجة عن ضعف عضلات الصدر، مما يجعل المريض يعتمد كلياً على تنفس الحجاب الحاجز (التنفس البطني).
- مشاكل في البلع (Dysphagia) تزيد من خطر دخول الطعام إلى القصبة الهوائية، مما يسبب التهابات رئوية متكررة تهدد الحياة.
- رعاش دقيق وواضح في لسان الطفل المصاب، وهي علامة سريرية مميزة يبحث عنها أطباء الأعصاب لتأكيد التشخيص الأولي.
- فقدان المنعكسات الوترية العميقة، حيث لا يستجيب المريض عند النقر على الركبة أو المرفق بالمطرقة الطبية.
- تشوهات في الهيكل العظمي، وأبرزها الجنف (Scoliosis)، نتيجة عدم قدرة العضلات الضعيفة على دعم استقامة العمود الفقري.
- تأخر حركي ملحوظ، مثل عدم القدرة على رفع الرأس، أو الجلوس دون استناد، أو التدحرج في السن الطبيعي.
- ظهور الصدر بشكل “الناقوس” أو الجرس، حيث يكون الجزء العلوي ضيقاً والبطن بارزاً بسبب الجهد التنفسي المفرط.
- ضعف في القدرة على السعال، مما يؤدي إلى تراكم الإفرازات في الرئتين وزيادة احتمالية الإصابة بالعدوى البكتيرية.
- تراجع في القوة البدنية بعد فترات من النشاط، حيث تنهك العضلات بسرعة نتيجة نقص التروية العصبية.
- صعوبة في المص والرضاعة لدى المواليد الجدد، مما يؤدي إلى فشل النمو العضوي وبطء زيادة الوزن.
أسباب ضمور النخاع الشوكي
يعود السبب الجذري لهذا المرض إلى خلل بنيوي في المادة الوراثية، وإليك التحليل العلمي الدقيق للمسببات من موقع HAEAT الطبي:
- طفرة أو حذف في جين (SMN1) الموجود على الكروموسوم 5، وهو الجين الأساسي لإنتاج بروتين بقاء الخلايا العصبية الحركية.
- النقص الحاد في هذا البروتين يؤدي إلى موت الخلايا العصبية التي تربط الحبل الشوكي بالعضلات الإرادية في الجسم.
- وجود جين احتياطي يُسمى (SMN2)، لكنه للأسف ينتج نسخة ناقصة وغير مستقرة من البروتين بنسبة 90%، مما لا يعوض النقص.
- وراثة المرض تتم بشكل “متنحٍ”، أي أن الطفل يحتاج لنسختين معيبتين (واحدة من الأب وأخرى من الأم) ليظهر عليه المرض.
- عدد نسخ جين (SMN2) يلعب دوراً حاسماً في تحديد شدة الإصابة؛ فكلما زاد عدد النسخ، كانت الأعراض أخف وطأة وتأخراً.
- في حالات استثنائية (حوالي 2%)، قد تحدث طفرة جينية جديدة في الجنين دون أن يكون الأبوان حاملين للمرض.
- الخلل الكيميائي الحيوي يؤدي إلى تراكم السموم داخل الخلية العصبية، مما يعجل بضمور المحاور العصبية المسؤولة عن نقل النبضات.
متى تزور الطبيب؟
إن التدخل المبكر في حالات ضمور النخاع الشوكي يمثل حارساً حقيقياً لمنع تدهور الوظائف الحيوية، لذا يجب الانتباه لأي علامة غير طبيعية في النمو.
تؤكد مدونة حياة الطبية أن التشخيص في الأيام الأولى بعد الولادة يفتح الباب أمام العلاجات الجينية الحديثة التي قد تغير مسار المرض تماماً.
عند البالغين
على الرغم من ندرة ظهور المرض في سن متأخرة، إلا أن البالغين قد يواجهون أعراضاً تستدعي الاستشارة الفورية، ومنها:
- ملاحظة ضعف مفاجئ أو تدريجي في عضلات الفخذين أو الكتفين يصعب معه صعود الدرج.
- تكرار السقوط أو التعثر دون وجود سبب ميكانيكي واضح في المفاصل.
- تشنجات عضلية مستمرة أو رفرفة غير مفسرة في الألياف العضلية تحت الجلد.
- صعوبة في رفع الأشياء التي كانت تعتبر خفيفة في السابق.
عند الأطفال
يجب على الآباء مراقبة المعالم الحركية بدقة، وزيارة طبيب أعصاب الأطفال في الحالات التالية:
- إذا كان الرضيع لا يستطيع تثبيت رأسه بعد إتمام الشهر الرابع.
- إذا لاحظت الأم أن حركة الجنين في أواخر الحمل كانت ضعيفة بشكل غير معتاد.
- فشل الطفل في الجلوس مستنداً بحلول الشهر الثامن، أو عدم القدرة على الوقوف في نهاية السنة الأولى.
- وجود صوت “قعقعة” أو صفير في الصدر مع كل نفس، مما يشير لضعف العضلات التنفسية.
أسئلة ذكية وحرجة يجب طرحها على أخصائي الأعصاب
عند لقاء المختص، تنصحكم بوابة HAEAT الطبية بتحضير قائمة الأسئلة التالية لضمان الحصول على صورة كاملة:
- ما هو نوع SMA الذي يعاني منه طفلي بناءً على عدد نسخ جين SMN2؟
- هل طفلي مرشح للعلاجات الجينية المعتمدة من FDA مثل (Zolgensma)؟
- كيف يمكننا البدء في بروتوكول الدعم التنفسي الاستباقي قبل حدوث أزمات؟
- ما هي خطة العلاج الطبيعي المناسبة للحفاظ على مرونة المفاصل ومنع التقلصات؟
- هل تتوفر تجارب سريرية حديثة يمكننا الانضمام إليها؟
(وفقاً لـ National Institutes of Health (NIH)، فإن التشخيص المبكر عبر فحص حديثي الولادة الجيني يساهم في تحسين النتائج الحركية بنسبة تصل إلى 80% عند البدء بالعلاج قبل ظهور الأعراض).
عوامل خطر الإصابة بـ ضمور النخاع الشوكي
تعتبر عوامل الخطر المرتبطة بهذا الاعتلال الوراثي محددة بدقة في الأبحاث الجينية، حيث لا يرتبط المرض بعوامل بيئية بقدر ارتباطه بالتركيبة الجينية للأبوين. تشمل أبرز هذه العوامل ما يلي:
- التاريخ العائلي: وجود طفل سابق مصاب بـ ضمور النخاع الشوكي يزيد من احتمالية إصابة المواليد القادمين بنسبة 25% في كل حمل.
- حمل الجينات المعيبة: يُقدر أن شخصاً واحداً من بين كل 40 إلى 50 شخصاً يحمل طفرة في جين (SMN1) دون ظهور أعراض عليه، مما يجعله “حاملاً صامتاً” للمرض.
- زواج الأقارب: ترتفع معدلات الإصابة في المجتمعات التي يكثر فيها زواج الأقارب، حيث تزداد فرص التقاء نسختين معيبتين من الجينات لدى الزوجين.
- العوامل العرقية: على الرغم من أن المرض يصيب كافة الأعراق، إلا أن بعض الدراسات تشير إلى تباين طفيف في وتيرة تواتر الطفرات الجينية بين المجموعات السكانية المختلفة.
- تكرار عدد نسخ جين (SMN2): يُعد نقص عدد نسخ الجين الاحتياطي عامل خطر رئيسي يحدد شدة المرض وسرعة تدهور الحالة الصحية للمريض.
- الفحص الجيني المسبق: غياب الفحص المبكر قبل الزواج يمثل عامل خطر يتسبب في انتقال المرض للأجيال القادمة دون وعي مسبق بالخطر الجيني.
مضاعفات ضمور النخاع الشوكي
يؤدي الإهمال في إدارة حالة ضمور النخاع الشوكي أو تأخر العلاج إلى سلسلة من المضاعفات الجهازية التي تؤثر على جودة الحياة، ومن أهمها:
- الفشل التنفسي المزمن: نتيجة ضعف العضلات الوربية وعضلات الحجاب الحاجز، مما يستدعي الاعتماد الدائم على أجهزة التنفس الاصطناعي.
- الجنف الشديد (Scoliosis): انحراف العمود الفقري الذي قد يضغط على الرئتين والقلب، مما يعيق الوظائف الحيوية ويستدعي تدخلاً جراحياً معقداً.
- التقلصات العضلية (Contractures): قصر دائم في العضلات والأوتار يؤدي إلى تيبس المفاصل وفقدان النطاق الحركي الطبيعي للأطراف.
- سوء التغذية الحاد: صعوبات البلع المزمنة تؤدي إلى نقص السعرات الحرارية والبروتينات، مما يفاقم من هزال العضلات وضعف جهاز المناعة.
- الالتهاب الرئوي الشفطي: ناتج عن تسرب الطعام أو السوائل إلى المجرى التنفسي، وهو أحد الأسباب الرئيسية للوفاة في الحالات المتقدمة.
- هشاشة العظام والكسور: قلة الحركة والحمل الميكانيكي على العظام تؤدي إلى ضعف كثافتها، مما يجعل المريض عرضة للكسور من أبسط الإصابات.
- مشاكل الجهاز الهضمي: مثل الإمساك المزمن والارتجاع المعدي المريئي نتيجة ضعف عضلات جدار البطن والجهاز الهضمي.
- العزلة الاجتماعية والاكتئاب: التأثيرات النفسية الناتجة عن فقدان الاستقلالية الحركية تؤثر بشكل مباشر على الصحة العقلية للمصاب وعائلته.
الوقاية من ضمور النخاع الشوكي
على الرغم من أن ضمور النخاع الشوكي مرض وراثي، إلا أن العلم الحديث وفر سبل الوقاية للحد من انتشاره عبر استراتيجيات استباقية دقيقة:
- الفحص الجيني قبل الزواج: إجراء فحوصات الكشف عن “حامل الجين” للزوجين لتحديد مدى خطورة انتقال المرض للأطفال.
- التشخيص الوراثي قبل الانغراس (PGD): استخدام تقنيات أطفال الأنابيب لفحص الأجنة جينياً قبل غرسها في الرحم، لضمان اختيار جنين سليم.
- الفحص المبكر لحديثي الولادة: إدراج اختبار (SMN1) ضمن فحوصات المولود الجديد الوطنية للبدء بالعلاج قبل ظهور الأعراض السريرية.
- الاستشارة الوراثية المتخصصة: توفير الدعم العلمي للعائلات التي لديها تاريخ مرضي لشرح الأنماط الوراثية وخيارات الإنجاب الآمنة.
- التوعية المجتمعية: نشر الوعي حول أهمية الفحوصات الجينية، خاصة في المناطق التي تشهد معدلات عالية من زواج الأقارب.
- الاختبارات السابقة للولادة: فحص السائل السلوي أو عينة من خملات الكوريون خلال الأسابيع الأولى من الحمل للتأكد من سلامة الجنين.
تشخيص ضمور النخاع الشوكي
يعتمد تشخيص ضمور النخاع الشوكي على تضافر النتائج السريرية مع الاختبارات المخبرية الدقيقة لضمان دقة النتيجة، وتتبع المنهجية التالية:
- الاختبار الجيني الجزيئي: وهو المعيار الذهبي للتشخيص، حيث يبحث عن حذف في جين (SMN1) وتحديد عدد نسخ جين (SMN2).
- اختبار كينيز الكرياتين (CPK): فحص إنزيمات العضلات في الدم؛ ورغم أنها تكون طبيعية أو مرتفعة قليلاً، إلا أنها تساعد في استبعاد أنواع أخرى من ضمور العضلات.
- تخطيط العضلات الكهربائي (EMG): يقيس النشاط الكهربائي للعضلات للكشف عن وجود علامات التنكس العصبي الحركي.
- دراسة توصيل الأعصاب (NCV): تقييم سرعة وقوة الإشارات الكهربائية في الأعصاب الطرفية لاستبعاد اعتلالات الأعصاب الأخرى.
- خزعة العضلات: نادراً ما تُستخدم حالياً، ولكنها قد تكشف عن أنماط معينة من الضمور العضلي المرتبط بمشاكل الأعصاب.
- الفحص السريري العصبي الشامل: تقييم المنعكسات، القوة العضلية، وتطور المعالم الحركية مقارنة بالعمر الزمني للطفل.
علاج ضمور النخاع الشوكي
شهد بروتوكول علاج ضمور النخاع الشوكي ثورة حقيقية في العقد الأخير، حيث انتقل من الرعاية التلطيفية إلى العلاجات الجينية الجذرية التي تستهدف إصلاح الخلل من منبعه.
تغييرات نمط الحياة والرعاية المنزلية
تعتبر الرعاية الداعمة حجر الزاوية للحفاظ على استقرار الحالة الوظيفية للمريض:
- العلاج الطبيعي والمهني: ممارسة تمارين الإطالة اليومية لمنع التقلصات العضلية والحفاظ على مرونة المفاصل واستخدام الجبائر المناسبة.
- الدعم التنفسي المنزلي: استخدام أجهزة التنفس غير الاختراقي (BiPAP) أثناء النوم لتحسين جودة التبادل الغازي وإراحة عضلات التنفس.
- الإدارة التغذوية: استخدام أنابيب التغذية (G-tube) في حالات صعوبة البلع لضمان حصول الجسم على العناصر الضرورية دون خطر الاختناق.
- استخدام التكنولوجيا المساعدة: الكراسي المتحركة الكهربائية، وأجهزة التواصل البديلة التي تعزز استقلالية المريض في حياته اليومية.
العلاجات الدوائية والجينية
تستهدف هذه الأدوية زيادة مستويات بروتين (SMN) في الجهاز العصبي المركزي عبر آليات حيوية معقدة:
بروتوكولات علاج البالغين
في حالات البالغين المصابين بـ ضمور النخاع الشوكي، يتم التركيز على استقرار الوظائف الحركية ومنع التدهور:
- دواء نوسينيرسين (Spinraza): يتم حقنه عن طريق الظهر (داخل القراب) لتحفيز جين (SMN2) لإنتاج بروتين فعال بشكل أكبر، وهو يتطلب جرعات دورية مدى الحياة.
- دواء ريسديبلام (Evrysdi): علاج فموي يومي يعمل على تعديل معالجة جين (SMN2)، ويتميز بسهولة الاستخدام المنزلي وفعاليته في تحسين القوة العضلية لدى الكبار.
- مضادات الأكسدة والمكملات: استخدام بروتوكولات داعمة تشمل فيتامين D والكالسيوم لتعزيز صحة العظام التي تتأثر بقلة الحركة.
بروتوكولات علاج الأطفال والرضع
تعتبر هذه المرحلة هي “النافذة الذهبية” لتحقيق أقصى استفادة من العلاجات المتقدمة:
- العلاج الجيني (Zolgensma): حقنة وريدية لمرة واحدة في العمر، تقوم بإدخال نسخة سليمة ووظيفية من جين (SMN1) إلى الخلايا العصبية عبر ناقل فيروسي غير ضار.
- التدخل المبكر قبل السريري: البدء بالعلاجات المذكورة فور التشخيص الجيني وقبل ظهور ضعف العضلات يضمن تطوراً حركياً يقترب من الطبيعي.
- المراقبة الدقيقة للنمو: برامج مكثفة لمتابعة الوزن، التنفس، والتطور الحركي لضبط جرعات الأدوية والتدخلات المساندة.
الابتكارات المستقبلية: تقنيات تعديل الجينات CRISPR وإعادة بناء الأعصاب
يفتح الذكاء الاصطناعي وهندسة الجينات آفاقاً لم تكن متصورة لعلاج ضمور النخاع الشوكي:
- تقنية CRISPR-Cas9: تجرى أبحاث متقدمة لاستخدام “المقص الجيني” لإصلاح الطفرة في جين (SMN1) نفسه داخل جسم الإنسان بشكل دائم ومستقر.
- الطب التجديدي: استخدام الخلايا الجذعية المستحثة (iPSCs) لإنتاج خلايا عصبية حركية جديدة وزراعتها لتعويض الأنسجة التالفة في النخاع الشوكي.
- المحاكاة الحاسوبية للبروتين: استخدام الذكاء الاصطناعي لتصميم جزيئات دوائية صغيرة ترتبط ببروتين (SMN) وتزيد من استقراره وحيويته داخل الخلية.
العلاج الطبيعي المعتمد على الروبوتات
يمثل الدمج بين الهندسة الميكانيكية والعلوم العصبية طفرة في إعادة تأهيل مرضى ضمور النخاع الشوكي:
- الهياكل العظمية الخارجية (Exoskeletons): بدلات روبوتية ذكية تساعد المرضى الذين فقدوا القدرة على المشي على الوقوف والحركة، مما يحسن الدورة الدموية وكثافة العظام.
- أجهزة التدريب التفاعلية: أنظمة تعتمد على الواقع الافتراضي (VR) لتحفيز المسارات العصبية المتبقية عبر ألعاب حركية مدروسة تزيد من مرونة الدماغ والجهاز العصبي.
- التحفيز الكهربائي الوظيفي (FES): استخدام روبوتات ترسل نبضات كهربائية دقيقة للعضلات الضامرة بالتزامن مع الحركة، مما يساعد في تقوية الألياف العضلية المتبقية.

الطب البديل وضمور النخاع الشوكي
على الرغم من أن العلاجات الجينية هي المسار الأساسي، إلا أن هناك خيارات تكميلية تهدف إلى تحسين الراحة العامة وتقليل التوتر العضلي، ويجب استشارة الطبيب قبل البدء بأي منها:
- العلاج المائي (Hydrotherapy): يساعد الماء في تخفيف الحمل عن المفاصل والعضلات الضعيفة، مما يسمح للمريض بأداء حركات قد لا يتمكن منها على اليابسة، ويزيد من كفاءة الدورة الدموية.
- الوخز بالإبر الصينية: يُستخدم لدى بعض البالغين المصابين بـ ضمور النخاع الشوكي لتقليل الآلام العضلية المزمنة وتحسين تدفق الطاقة الحيوية في المسارات العصبية.
- التدليك العلاجي (Massage Therapy): يعمل على تحفيز الأنسجة الرخوة، ومنع تيبس العضلات، وتحسين جودة النوم عبر تقليل مستويات الكورتيزول في الجسم.
- المكملات الغذائية المدروسة: مثل الإنزيم المساعد Q10، والكيرنيتين، والكرياتين، والتي قد تدعم إنتاج الطاقة داخل الميتوكوندريا في الخلايا العضلية المتبقية.
- اليوجا والتأمل: تمارين التنفس العميق والتركيز الذهني تساعد في تخفيف الضغط النفسي المرتبط بالمرض المزمن وتحسن سعة الرئتين بشكل غير مباشر.
- العلاج بالأعشاب: يُستخدم بحذر شديد لتقليل الالتهابات العامة، مع ضرورة التأكد من عدم تداخلها مع الأدوية الجينية أو المناعية.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع مرض معقد مثل ضمور النخاع الشوكي تنظيماً دقيقاً للمعلومات الطبية لضمان الحصول على أفضل خطة علاجية.
ماذا تفعل قبل الموعد؟
- تدوين قائمة شاملة بكافة الأعراض، حتى تلك التي تبدو غير مرتبطة بالحركة، مثل صعوبات الهضم أو جودة النوم.
- جمع التاريخ العائلي الوراثي الدقيق، خاصة حالات الوفاة المبكرة غير المبررة في العائلة أو حالات ضعف العضلات.
- تصوير مقاطع فيديو قصيرة للطفل أو المريض أثناء الحركة أو التنفس لتوضيح العلامات السريرية التي قد لا تظهر بوضوح في غرفة الفحص.
- إعداد قائمة بالأدوية والمكملات الحالية بجرعاتها الدقيقة لتجنب أي تداخلات دوائية محتملة.
ماذا تتوقع من الطبيب؟
- إجراء فحص بدني دقيق للمنعكسات الوترية والقوة العضلية في الأطراف الأربعة.
- طرح أسئلة حول مراحل التطور الحركي (الجلوس، الوقوف، المشي) والتغيرات التي طرأت عليها مؤخراً.
- طلب فحوصات مخبرية جينية فورية لتأكيد حذف جين (SMN1) وتحديد عدد نسخ جين (SMN2).
- التوصية بزيارة فريق متعدد التخصصات يشمل أخصائي أعصاب، وأخصائي تنفس، وخبير تغذية، وأخصائي علاج طبيعي.
تطبيقات مراقبة الحركة الرقمية لتوثيق الحالة
يمكن للمرضى استخدام تطبيقات متطورة تعمل بالذكاء الاصطناعي لجمع بيانات دقيقة قبل الموعد:
- تطبيقات تتبع المهارات الحركية: تسجيل التطور اليومي وتحويله إلى رسوم بيانية توضح للطبيب سرعة استجابة المريض للعلاج.
- منصات مراقبة التنفس الليلي: تتبع أنماط الشخير أو انقطاع النفس وتسجيلها لمناقشتها مع أخصائي الصدرية.
- المفكرة الجينية الرقمية: حفظ نتائج الفحوصات والخرائط الجينية لمشاركتها مع الأطباء عبر رموز استجابة سريعة (QR Codes).
مراحل الشفاء من ضمور النخاع الشوكي
في ظل العلاجات الحديثة، لم يعد مصطلح “الشفاء” يعني العودة الكاملة للوضع الطبيعي بالضرورة، بل يشمل مراحل من التحسن والاستقرار:
- مرحلة الاستقرار العصبي: وهي المرحلة الأولى بعد تلقي العلاج الجيني، حيث يتوقف تنكس الخلايا العصبية الحركية ويتم الحفاظ على ما تبقى من وحدات وظيفية.
- مرحلة اكتساب المهارات الحركية: يبدأ المريض (خاصة الأطفال) في الوصول إلى معالم حركية جديدة مثل رفع الرأس أو الجلوس، وهي ثمرة التعاون بين الدواء والعلاج الطبيعي.
- مرحلة تحسين الوظائف الحيوية: تشمل استقرار الوزن، وتحسن قدرات البلع، وزيادة كفاءة التنفس التلقائي دون الحاجة لأجهزة مساندة لفترات طويلة.
- مرحلة الإدماج الوظيفي: تمكين المريض من المشاركة في الأنشطة المدرسية أو المهنية باستخدام أدوات تكنولوجية مساعدة تعزز من استقلاليته.
الأنواع الشائعة لضمور النخاع الشوكي
يُصنف المرض إلى أربعة أنواع رئيسية بناءً على عمر ظهور الأعراض وأقصى وظيفة حركية يمكن الوصول إليها:
- النوع الأول (مرض ويردنيج-هوفمان): النوع الأكثر شيوعاً وشدة، تظهر أعراضه قبل سن 6 أشهر، ولا يتمكن الأطفال فيه من الجلوس دون استناد، ويواجهون صعوبات تنفسية حادة.
- النوع الثاني: تبدأ الأعراض بين 6 إلى 18 شهراً، يستطيع هؤلاء الأطفال الجلوس ولكنهم عادة لا يتمكنون من الوقوف أو المشي بشكل مستقل، ويحتاجون لدعم تنفسي لاحقاً.
- النوع الثالث (مرض كوجيلبيرج-ويلاندر): تظهر أعراضه بعد سن 18 شهراً، يستطيع المرضى المشي بشكل مستقل في البداية ولكنهم قد يفقدون هذه القدرة مع تقدم العمر والوزن.
- النوع الرابع: يظهر في مرحلة البلوغ (بعد سن 21 عاماً)، وتكون الأعراض خفيفة نسبياً وتشمل ضعفاً تدريجياً في العضلات القريبة دون التأثير على التنفس أو العمر المتوقع.
التطورات الحديثة في العلاج الجيني لضمور النخاع الشوكي
يشهد العالم ثورة حقيقية في علاجات ضمور النخاع الشوكي، حيث انتقلت الأبحاث من مجرد محاولة تخفيف الأعراض إلى “إعادة برمجة” المادة الوراثية. تقنيات مثل “أولينوكليوتيدات مضادة للاتجاه” (ASOs) أثبتت نجاحاً باهراً في تعديل عملية ربط جين (SMN2) لتحويله إلى جين وظيفي ينتج بروتيناً كاملاً. هذه الابتكارات لا تنقذ الأرواح فحسب، بل تعيد كتابة التاريخ المرضي للعائلات التي كانت تعاني من فقدان أطفالها في سن مبكرة.
التأثير النفسي والاجتماعي على المصابين وعائلاتهم
يتطلب التعايش مع ضمور النخاع الشوكي مرونة نفسية هائلة ودعماً اجتماعياً مكثفاً:
- مواجهة التشخيص: تمر العائلات بمراحل الصدمة والإنكار قبل قبول الحالة، مما يتطلب وجود مستشارين نفسيين متخصصين في الأمراض النادرة.
- عبء الرعاية: الضغط البدني والمادي على مقدمي الرعاية قد يؤدي إلى الاحتراق النفسي، لذا يجب توفير “رعاية استراحة” دورية.
- التنمر والدمج: يحتاج المصابون إلى بيئة مدرسية واجتماعية تحترم قدراتهم وتوفر لهم التسهيلات الحركية دون تمييز أو شفقة.
- مجموعات الدعم: التواصل مع عائلات تمر بنفس التجربة يساعد في تبادل النصائح العملية وتقليل الشعور بالعزلة.
النظام الغذائي والدعم التغذوي لمرضى ضمور النخاع الشوكي
تعد التغذية جزءاً لا يتجزأ من بروتوكول العلاج، حيث أن هزال العضلات يغير من احتياجات الجسم الاستقلابية. يجب التركيز على الوجبات الغنية بالبروتين عالي الجودة لدعم الألياف العضلية المتبقية، مع مراعاة قوام الطعام لتجنب مشاكل البلع. كما ينصح بتوزيع الوجبات إلى حصص صغيرة ومتكررة لتجنب نقص سكر الدم الليلي، وضمان الحصول على كميات كافية من فيتامين د والكالسيوم للحفاظ على قوة العظام الهشة.
ضمور النخاع الشوكي والزواج: الفحوصات الجينية
يفتح التقدم العلمي باب الأمل للمقبلين على الزواج من العائلات التي تحمل تاريخاً مع المرض:
- فحص الناقل الصامت: إجراء اختبارات دقيقة للطرفين للتأكد من عدم حملهما لطفرة (SMN1) في نفس الوقت.
- خيارات الإنجاب: مناقشة تقنيات الفحص الوراثي للأجنة لضمان إنجاب أطفال أصحاء غير حاملين للمرض.
- الحق في المعرفة: توفير معلومات شفافة حول احتمالات انتقال المرض وكيفية الاستعداد لها طبياً ومادياً.
خرافات شائعة حول ضمور النخاع الشوكي
- الخرافة: المرض معدٍ أو ينتج عن سوء التغذية أثناء الحمل.
- الحقيقة: هو اضطراب جيني بحت ينتقل عبر الوراثة ولا علاقة له بالعدوى أو تصرفات الأم أثناء الحمل.
- الخرافة: يؤدي المرض دائماً إلى الوفاة المبكرة ولا يوجد علاج له.
- الحقيقة: مع العلاجات الجينية والدوائية الحديثة، أصبح المرضى يعيشون حياة مديدة ويحققون تقدماً حركياً مذهلاً.
- الخرافة: المصابون بـ ضمور النخاع الشوكي يعانون من تأخر ذهني.
- الحقيقة: المصابون غالباً ما يتمتعون بذكاء حاد وقدرات معرفية تفوق أقرانهم في بعض الأحيان.
نصائح ذهبية من “مدونة حياة الطبية” 💡
- قاعدة الـ 24 ساعة: لا تتجاهل أي عدوى تنفسية بسيطة لأكثر من يوم واحد؛ اطلب الرعاية الطبية فوراً لتجنب المضاعفات الرئوية.
- التكنولوجيا صديقك: استثمر في الأجهزة اللوحية وأدوات التحكم الصوتي لتعزيز استقلالية المريض في بيئته المنزلية.
- العلاج الطبيعي ليس خياراً: الانتظام في التمارين اليومية هو الوقود الذي يجعل الأدوية الجينية تعمل بأقصى كفاءة.
- التغذية الوقائية: استشر أخصائي تغذية لوضع خطة تمنع السمنة، حيث أن الوزن الزائد يمثل عبئاً إضافياً على العضلات الضعيفة.
أسئلة شائعة (PAA)
هل يمكن لمرضى ضمور النخاع الشوكي ممارسة الرياضة؟
نعم، وبشكل ضروري، ولكن تحت إشراف متخصص. الرياضة الموصى بها هي التمارين الهوائية الخفيفة والسباحة التي لا تسبب إجهاداً مفرطاً للألياف العضلية.
ما هو متوسط العمر المتوقع للمصابين؟
تغير هذا المتوسط بشكل جذري مع العلاجات الجديدة؛ فبعد أن كان النوع الأول نادراً ما يتجاوز العامين، أصبح الأطفال الآن ينمون ويصلون لسنوات الدراسة بفضل التدخل المبكر.
هل تتوفر العلاجات الجينية في الدول العربية؟
بدأت العديد من الدول العربية في إدراج العلاجات الجينية (مثل زولجينسما) ضمن برامجها الصحية الوطنية، وتوفيرها للمواطنين عبر مبادرات رئاسية وحكومية.
الخاتمة
ختاماً، يمثل ضمور النخاع الشوكي رحلة تحدٍ تتطلب صبراً، وإيماناً، ومعرفة طبية مستمرة. إن التحول من اليأس إلى الأمل في علاج هذا المرض هو قصة نجاح للعلم البشري. نحن في بوابة HAEAT الطبية نؤمن بأن المعرفة هي أولى خطوات العلاج، وأن التكاتف بين الأسرة والفريق الطبي والتقنيات الحديثة كفيل بصناعة مستقبل أفضل لكل محارب يعاني من هذا المرض.