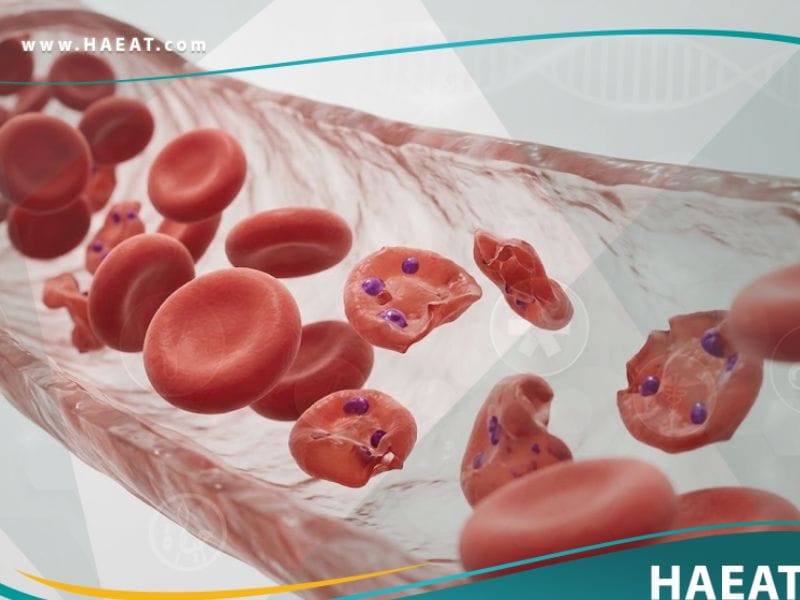
يُعد نقص الإنزيم G6PD (Glucose-6-Phosphate Dehydrogenase Deficiency) أحد أكثر الاضطرابات الوراثية انتشاراً حول العالم، حيث يؤثر بشكل مباشر على استقرار كريات الدم الحمراء.
تشير التقارير الصادرة عن مدونة حياة الطبية إلى أن هذا الخلل الجيني يحرم الجسم من إنزيم حيوي يحمي الخلايا من الإجهاد التأكسدي الناتج عن بعض الأطعمة أو الأدوية.
في هذا الدليل الاستقصائي، نستعرض كافة التفاصيل العلمية والسريرية المتعلقة بهذه الحالة، موفرين حلولاً عملية لإدارة الحياة اليومية وتجنب نوبات انحلال الدم المفاجئة.
ما هو نقص الإنزيم G6PD؟
نقص الإنزيم G6PD هو حالة وراثية جينية تتميز بنقص بروتين “غلوكوز – 6 – فوسفات دي هيدروجيناز” المسؤول عن حماية كريات الدم الحمراء من التلف المبكر.
يوضح موقع حياة الطبي أن هذا الإنزيم يلعب دوراً محورياً في مسار “فوسفات البنتوز”، حيث يساهم في إنتاج جزيئات (NADPH) التي تحافظ على مستويات الغلوتاثيون داخل الخلية.
بدون كميات كافية من هذا الإنزيم، تصبح خلايا الدم عرضة للتكسر عند التعرض لمحفزات معينة، مما يؤدي إلى ما يُعرف طبياً بفقر الدم الانحلالي الحاد.
تتفاوت شدة الإصابة بهذا العوز الجيني بناءً على نوع الطفرة، حيث يعاني الملايين من “أنيميا الفول” التي تتسبب في تحلل الدم فور تناول البقوليات.
تعتبر هذه الحالة أكثر شيوعاً في مناطق حوض البحر الأبيض المتوسط، وأفريقيا، وآسيا، مما يتطلب وعياً مجتمعياً كبيراً بطرق الوقاية والتشخيص المبكر.
وفقاً لمنظمة الصحة العالمية، فإن نقص الإنزيم G6PD لا يسبب أعراضاً دائمة في الغالب، بل تظهر المشكلات الصحية بشكل نوبات مرتبطة بمحفزات بيئية وكيميائية محددة.

أعراض نقص الإنزيم G6PD
تظهر أعراض نقص الإنزيم G6PD بشكل مفاجئ عند التعرض لمواد مؤكسدة، وتتراوح حدتها بين البسيطة التي تزول تلقائياً، والخطيرة التي تتطلب تدخلاً طبياً فورياً:
- اليرقان (Jaundice): اصفرار ملحوظ في الجلد وبياض العينين نتيجة تراكم مادة البيليروبين الناتجة عن تكسر الكريات.
- تغير لون البول: يتحول البول إلى اللون الداكن أو البرتقالي المائل للحمرة (يشبه لون الشاي أو الكوكاكولا).
- الشحوب المفاجئ: فقدان اللون الطبيعي للجلد والشفاه نتيجة الانخفاض السريع في عدد خلايا الدم الحمراء الحاملة للأكسجين.
- التعب والإرهاق الشديد: شعور بالوهن وعدم القدرة على القيام بالأنشطة اليومية البسيطة بسبب نقص التروية الأكسجينية للأنسجة.
- ضيق التنفس (Dyspnea): صعوبة في التقاط الأنفاس، خاصة عند بذل مجهود بدني، نتيجة فقر الدم الحاد.
- تسارع ضربات القلب (Tachycardia): يحاول القلب التعويض عن نقص الأكسجين عبر زيادة سرعة الضخ، مما يسبب خفقاناً ملموساً.
- آلام البطن والظهر: يشعر المريض بآلام حادة في منطقة البطن أو الظهر، وهي علامة شائعة أثناء نوبات انحلال الدم الكبرى.
- تضخم الطحال: في الحالات المزمنة أو النوبات المتكررة، قد يتضخم الطحال نتيجة عمله الشاق في تصفية الخلايا التالفة.
- الحمى الخفيفة: قد ترتفع درجة حرارة الجسم بشكل طفيف كاستجابة مناعية لعملية التحلل الواسعة داخل الأوعية الدموية.
- الدوار والدوخة: الشعور بعدم الاتزان، والذي قد يتطور إلى فقدان الوعي في حالات فقر الدم الانحلالي الشديد.
تعتمد سرعة ظهور هذه الأعراض على كمية المادة المحفزة التي تعرض لها المصاب، ومدى النقص الفعلي في نشاط نقص الإنزيم G6PD لديه.
أسباب نقص الإنزيم G6PD
يعود السبب الرئيسي وراء نقص الإنزيم G6PD إلى طفرة جينية موروثة على الكروموسوم (X)، مما يجعله مرضاً مرتبطاً بالجنس يصيب الذكور غالباً.
يشير موقع HAEAT الطبي إلى أن الخلل يكمن في ترتيب القواعد النيتروجينية لجين G6PD، مما يؤدي لإنتاج إنزيم غير مستقر أو غير فعال وظيفياً.
يمكن تلخيص الميكانيكا الجينية والفسيولوجية للمرض في النقاط التالية:
- الوراثة المرتبطة بالكروموسوم X: ينتقل المرض من الأم (التي قد تكون حاملة للجين) إلى أبنائها الذكور بنسبة 50%.
- إصابة الإناث: نادراً ما تصاب الإناث بالأعراض الكاملة، إلا إذا ورثت الجين المصاب من كلا الوالدين، أو عبر ظاهرة “تعطيل الكروموسوم X”.
- نقص مركب NADPH: يؤدي الخلل في الإنزيم إلى فشل الخلية في إنتاج هذا المركب الضروري لمكافحة الجذور الحرة الضارة.
- أكسدة خضاب الدم (Hemoglobin): عند غياب الحماية الإنزيمية، يتأكسد الهيموجلوبين ويترسب داخل الخلية مكوناً ما يعرف بـ “أجسام هاينز” (Heinz bodies).
- تدمير الغشاء الخلوي: تقوم البلعوميات في الطحال بالتعرف على الأجسام الغريبة داخل الكرية وتدميرها، مما يؤدي لانفجار الخلية وتحللها.
- المحفزات الغذائية: تناول الفول الأخضر أو البقوليات المشابهة يطلق مركبات (Vicine) و(Convicine) التي تسبب إجهاداً تأكسدياً عنيفاً.
- المحفزات الدوائية: بعض المضادات الحيوية (مثل السلفا) وأدوية الملاريا تعمل كمؤكسدات قوية تفشل الخلايا المصابة في التعامل معها.
- العدوى الفيروسية والبكتيرية: تُعد الالتهابات من أكثر الأسباب شيوعاً لتحفيز نوبات انحلال الدم، بسبب إفراز الكريات البيضاء للمواد المؤكسدة.
يصنف العلماء نقص الإنزيم G6PD إلى فئات مختلفة (حسب تصنيف WHO) بناءً على مستوى النشاط الإنزيمي المتبقي، مما يفسر تباين ردود الفعل بين المصابين.

متى تزور الطبيب؟
إن التعامل مع نقص الإنزيم G6PD يتطلب يقظة تامة، فبينما يعيش الكثيرون دون مشاكل، قد تظهر مواقف تستدعي التدخل الطبي العاجل لإنقاذ الحياة.
تؤكد مدونة HAEAT الطبية أن التأخر في طلب الرعاية الصحية أثناء نوبة التحلل الحاد قد يؤدي إلى فشل كلوي نتيحة ترسب الهيموجلوبين في الأنابيب الكلوية.
الحالات الحرجة لدى البالغين
يجب التوجه فوراً إلى قسم الطوارئ إذا لاحظ البالغ المصاب بـ نقص الإنزيم G6PD ظهور اصفرار مفاجئ في العين مصحوباً بآلام شديدة في الظهر.
كما يعد ضيق التنفس الشديد أثناء الراحة أو تحول لون البول إلى البني الغامق مؤشراً على فقدان كميات هائلة من كريات الدم الحمراء تتطلب نقلاً فورياً للدم.
مؤشرات الخطر عند الأطفال وحديثي الولادة
تعتبر مراقبة الأطفال المصابين بـ نقص الإنزيم G6PD مسؤولية مضاعفة؛ فحديث الولادة قد يعاني من يرقان ولادي شديد يهدد سلامة الدماغ (اليرقان النووي).
إذا لاحظت الأم خمولاً غير طبيعي، أو رفضاً للرضاعة، أو شحوباً مفاجئاً بعد إدخال أطعمة جديدة، فيجب إجراء فحص دم شامل فوراً لتقييم مستويات الهيموجلوبين.
التنبؤ المبكر عبر تقنيات الذكاء الاصطناعي لنوبات انحلال الدم الحادة
في عام 2026، بدأت بعض المراكز المتقدمة في استخدام نماذج تنبؤية تعتمد على الذكاء الاصطناعي لتحليل البيانات الحيوية للمصابين بـ نقص الإنزيم G6PD.
تقوم هذه الأنظمة بربط المؤشرات الحيوية (مثل معدل نبضات القلب ودرجة حرارة الجسم من الساعات الذكية) مع التاريخ الغذائي والدوائي المسجل رقمياً.
بناءً على هذا التحليل، يرسل النظام تنبيهاً للمريض أو الطبيب عند رصد أنماط تشير إلى بداية تحلل كيميائي في الدم قبل ظهور الأعراض السريرية الواضحة.
تساعد هذه التقنية في تقليل دخول المستشفيات عبر توجيه المريض لشرب كميات كبيرة من السوائل أو التوقف الفوري عن تناول دواء معين بمجرد رصد الخلل الأولي.

عوامل خطر الإصابة بنقص الإنزيم G6PD
تتداخل العوامل الوراثية والجغرافية لتحديد مدى احتمالية إصابة الفرد بحالة نقص الإنزيم G6PD، وهي عوامل لا يمكن تغييرها ولكن فهمها يساعد في التشخيص المبكر.
تشير الدراسات الموثقة في مجلة حياة الطبية إلى أن العوامل التالية تزيد من فرص ظهور المرض أو شدة نوباته:
- الجنس (الذكور): كما ذكرنا، فإن طبيعة الوراثة المرتبطة بالكروموسوم X تجعل الذكور هم الفئة الأكثر عرضة للإصابة بالأعراض السريرية الكاملة.
- الأصول العرقية: يرتفع معدل انتشار نقص الإنزيم G6PD بشكل ملحوظ بين المنحدرين من أصول أفريقية، أو من منطقة حوض البحر المتوسط، أو جنوب شرق آسيا.
- التاريخ العائلي: وجود إصابات سابقة في العائلة، خاصة من جهة الأم، يرفع احتمالية انتقال الطفرة الجينية للأجيال الجديدة بشكل كبير.
- الطفرات الجينية النوعية: بعض الطفرات (مثل طفرة النوع الأول) تكون مرتبطة بنقص إنزيمي مزمن وشديد حتى دون التعرض لمحفزات خارجية.
- العيش في مناطق الملاريا: تاريخياً، تطور هذا الخلل الجيني كنوع من الحماية الطبيعية ضد الملاريا، لذا يكثر تواجده في المناطق الموبوءة سابقاً بهذا المرض.
- الحمل: قد تظهر أعراض خفيفة على النساء الحوامل اللواتي يحملن الجين نتيجة التغيرات الفسيولوجية والإجهاد التأكسدي المتزايد خلال هذه الفترة.
مضاعفات نقص الإنزيم G6PD
إذا لم يتم التعامل مع نوبات التحلل الناتجة عن نقص الإنزيم G6PD بحذر، فقد تترتب عليها عواقب صحية وخيمة تؤثر على وظائف الأعضاء الحيوية:
- فشل كلوي حاد (AKI): يؤدي التحلل الواسع للكريات إلى تحرر الهيموجلوبين في الدم، والذي قد يسد أنابيب الكلى ويسبب توقفها عن العمل.
- فقر الدم الانحلالي الشديد: انخفاض الهيموجلوبين لمستويات خطيرة قد يؤدي إلى صدمة نقص التروية وفشل في وظائف القلب.
- اليرقان النووي (Kernicterus): عند حديثي الولادة، قد يعبر البيليروبين المرتفع حاجز الدم الدماغي مسبباً تلفاً عصبياً دائماً أو فقدان السمع.
- تكون حصوات المرارة: التحلل المستمر والمزمن للكريات الحمراء يؤدي إلى زيادة إفراز البيليروبين، مما يسرع من تشكل حصوات صبغية في المرارة.
- الإجهاد القلبي المزمن: في حالات نقص الإنزيم G6PD المرتبطة بفقر دم مزمن، يضطر القلب للعمل بجهد مضاعف، مما قد يؤدي لتضخم عضلة القلب.
- العدوى المتكررة: أحياناً يؤثر نقص الإنزيم على قدرة الخلايا البيضاء على قتل بعض أنواع البكتيريا، مما يجعل المصاب أكثر عرضة لبعض الالتهابات.
الوقاية من نقص الإنزيم G6PD
تعتمد الوقاية من نوبات نقص الإنزيم G6PD بشكل كلي على “الوعي الانتقائي”، أي معرفة ما يجب تجنبه بدقة متناهية لمنع تحفيز الإجهاد التأكسدي:
- تجنب البقوليات: الامتناع التام عن تناول الفول بكافة أشكاله (أخضر، مجفف، معلب) والابتعاد عن استنشاق حبوب لقاح نبات الفول.
- مراجعة الأدوية: يجب إبلاغ أي طبيب أو صيدلي بالإصابة بـ نقص الإنزيم G6PD قبل تناول أي مضادات حيوية أو مسكنات أو خافضات حرارة.
- تجنب النفتالين: الابتعاد عن كرات العثة (النفتالين) المستخدمة في تخزين الملابس، حيث إن استنشاق أبخرتها كفيل بإحداث نوبة انحلال حادة.
- الحذر من الحناء: بعض أنواع الحناء والصبغات قد تحتوي على مواد كيميائية تسبب تكسر الدم عند امتصاصها عبر الجلد لدى المصابين.
- شرب السوائل بكثرة: الحفاظ على ترطيب الجسم يساعد الكلى على التخلص من نواتج تحلل الخلايا ويحميها من الانسداد.
- الفحص المبكر للمواليد: إجراء فحص G6PD فور الولادة يضمن اتخاذ الاحتياطات اللازمة قبل ظهور أي مضاعفات يرقانية.
- الاستشارة الوراثية: يفضل للمقبلين على الزواج في العائلات التي ينتشر بها المرض إجراء فحوصات جينية لتحديد احتمالات إصابة الأبناء.
تشخيص نقص الإنزيم G6PD
يتطلب تشخيص نقص الإنزيم G6PD دقة مخبرية عالية، خاصة وأن نتائج بعض الفحوصات قد تكون مضللة إذا أجريت أثناء نوبة تحلل نشطة:
- فحص البقعة الفلورية (Beutler Test): اختبار سريع وشائع يستخدم للكشف النوعي عن وجود نشاط الإنزيم من عدمه تحت الأشعة فوق البنفسجية.
- القياس الكمي للإنزيم (Quantitative Assay): أدق الفحوصات ويحدد النسبة المئوية لنشاط نقص الإنزيم G6PD في الخلايا، ويصنف الحالة لدرجات (بسيطة، متوسطة، شديدة).
- فحص صورة الدم الكاملة (CBC): يظهر انخفاض الهيموجلوبين وارتفاع عدد الخلايا الشبكية (الكريات الشابة) كدليل على محاولة النخاع التعويض.
- لطخة الدم الطرفية: فحص عينة دم تحت المجهر لرصد “أجسام هاينز” أو الخلايا “المعضوضة” (Bite cells) المميزة لهذه الحالة.
- فحص البيليروبين: قياس مستويات البيليروبين المباشر وغير المباشر لتقييم حدة اليرقان وتأثيره على الجسم.
- الاختبارات الجينية (DNA Testing): تستخدم لتحديد نوع الطفرة الجينية بدقة، وهي مفيدة جداً في الدراسات الوراثية وتخطيط العائلة.
نقطة هامة: أثناء النوبة الحادة، تتحلل الخلايا الأكبر سناً (التي تفتقر للإنزيم)، وتبقى الخلايا الشابة ذات النشاط الإنزيمي العالي، مما قد يعطي نتيجة “طبيعية كاذبة”، لذا يجب إعادة الفحص بعد أسابيع من النوبة.
علاج نقص الإنزيم G6PD
لا يوجد علاج جذري لـ نقص الإنزيم G6PD كونه خللاً جينياً، ولكن الإدارة الطبية تهدف إلى وقف التحلل ودعم وظائف الجسم الحيوية أثناء الأزمات.
توضح بوابة HAEAT الطبية أن الخطوة الأولى والأهم هي الإيقاف الفوري للمحفز (سواء كان دواءً أو طعاماً) لمنع استمرار تدمير الخلايا.
الإدارة المنزلية ونمط الحياة
في الحالات البسيطة، يكتفي المريض بالراحة التامة وزيادة مأخوذ السوائل لتسهيل عمل الكلى، مع مراقبة دقيقة للون البول وبياض العين. يجب على المصاب بـ نقص الإنزيم G6PD الاحتفاظ بـ “بطاقة تنبيه طبية” في محفظته توضح حالته والأدوية المحظورة عليه لاستخدامها في حالات الطوارئ.
العلاجات الدوائية والتدخلات الطبية
تختلف بروتوكولات العلاج بناءً على الفئة العمرية وشدة فقر الدم الناتج عن الانحلال:
بروتوكول البالغين
- نقل الدم: يتم اللجوء إليه إذا انخفض مستوى الهيموجلوبين عن حدود معينة (عادة أقل من 7-8 جم/ديسيلتر) أو عند ظهور علامات فشل قلبي.
- السوائل الوريدية: تعطى بتركيزات محددة لضمان استمرار تدفق البول وحماية الأنابيب الكلوية من الانسداد بالهيموجلوبين.
- حمض الفوليك: يوصف لدعم النخاع العظمي في إنتاج كريات دم حمراء جديدة بشكل أسرع.
بروتوكول الأطفال
- العلاج الضوئي (Phototherapy): يستخدم لحديثي الولادة المصابين باليرقان الناتج عن نقص الإنزيم G6PD لتكسير البيليروبين ومنع وصوله للمخ.
- تبديل الدم (Exchange Transfusion): في الحالات الشديدة جداً لدى المواليد، يتم استبدال دم الطفل بدم متبرع سليم لخفض مستويات السموم بسرعة.
البروتوكولات الذكية لإدارة الأزمات الانحلالية
في وحدات العناية المركزة الحديثة لعام 2026، يتم استخدام بروتوكولات ذكية تعتمد على المراقبة اللحظية لدرجة حموضة البول (pH). يتم حقن بيكربونات الصوديوم وريدياً تحت إشراف أنظمة آلية للحفاظ على البول قلوياً، مما يمنع ترسب الهيموجلوبين ويحمي المريض من الفشل الكلوي.
تقنيات نقل الدم الحديثة وفلترة الكريات
عند الحاجة لنقل الدم لمريض نقص الإنزيم G6PD، يتم استخدام تقنيات فلترة دقيقة لإزالة الكريات البيضاء والمواد السيتوكينية التي قد تزيد من الالتهاب. كما يتم اختيار دم المتبرعين بدقة للتأكد من خلوه هو الآخر من نقص الإنزيم، لضمان أطول فترة حياة ممكنة للكريات المنقولة داخل جسم المصاب.
الطب البديل ونقص الإنزيم G6PD
يجب الحذر الشديد عند التفكير في “الطب البديل” لعلاج نقص الإنزيم G6PD، حيث إن بعض الأعشاب قد تعمل كمؤكسدات قوية تزيد من حدة انحلال الدم بشكل غير متوقع.
- الحذر من الأعشاب الصينية: بعض التركيبات العشبية الصينية تحتوي على مواد قد تسبب تكسر الدم لدى المصابين، لذا يمنع تناولها دون تحليل كيميائي دقيق.
- مكملات فيتامين C و K: الجرعات العالية جداً من فيتامين C (أكثر من 1 جرام) قد تحفز الإجهاد التأكسدي، وكذلك بعض مشتقات فيتامين K الاصطناعية.
- الكركم والزنجبيل: رغم فوائدهما، إلا أن تناول مستخلصاتهما بتركيزات عالية جداً قد يتداخل مع توازن الأكسدة في الخلايا المصابة بـ نقص الإنزيم G6PD.
- مضادات الأكسدة الطبيعية: يفضل التركيز على الأغذية الغنية بمضادات الأكسدة الخفيفة (مثل التوت والخضروات الورقية) بدلاً من المكملات المركزة.
- التوعية ضد “الخلطات المجهولة”: يمنع تماماً استخدام خلطات العطارين لعلاج فقر الدم دون التأكد من خلوها من مستخلصات البقوليات أو المواد المؤكسدة.
الاستعداد لموعدك مع الطبيب
لتحقيق أقصى استفادة من الزيارة الطبية ومساعدة الطبيب في إدارة نقص الإنزيم G6PD بشكل فعال، يفضل اتباع الخطوات التالية:
ماذا تفعل قبل الموعد؟
- تسجيل الأعراض: دون تاريخ بدء الشحوب، أو تغير لون البول، وأي أعراض مرافقة مثل آلام البطن أو الظهر.
- قائمة الطعام والدواء: سجل كل ما تناوله المريض (أو الأم إذا كانت ترضع طفلاً مصاباً) خلال الـ 48 ساعة التي سبقت ظهور الأعراض.
- تجهيز التاريخ العائلي: ابحث عن أي إصابات بفقر دم أو يرقان ولادي لدى الأقارب من جهة الأم.
ما الذي تتوقعه من الطبيب؟
- طرح أسئلة حول التعرض لمواد كيميائية (مثل النفتالين) أو تناول أطعمة تحتوي على الفول.
- طلب فحص دم شامل (CBC) وقياس نشاط نقص الإنزيم G6PD (بعد استقرار الحالة).
- تقديم قائمة بالأدوية الآمنة والأدوية المحظورة التي يجب تجنبها مدى الحياة.
أدوات المتابعة الرقمية وتطبيقات الهواتف
يمكن استخدام تطبيقات مخصصة لمرضى الحساسية والاضطرابات الجينية لمسح الباركود الخاص بالمنتجات الغذائية للتأكد من خلوها من مشتقات البقوليات أو الصبغات المحظورة.
مراحل الشفاء من نقص الإنزيم G6PD
التعافي من نوبة انحلال الدم الناتجة عن نقص الإنزيم G6PD يمر بمراحل فسيولوجية محددة تتطلب مراقبة مستمرة:
- مرحلة الاستقرار (24-48 ساعة): تبدأ عند إيقاف المحفز وتلقي السوائل الوريدية، حيث يتوقف تدهور مستوى الهيموجلوبين.
- مرحلة الاستجابة النخاعية (3-7 أيام): يبدأ النخاع العظمي بإطلاق كميات كبيرة من الخلايا الشبكية (الكريات الشابة) لتعويض المفقود.
- مرحلة اختفاء اليرقان (1-2 أسبوع): يبدأ الكبد بمعالجة البيليروبين الفائض وتعود العين والجلد للونهما الطبيعي تدريجياً.
- مرحلة استعادة مخزون الحديد: قد يحتاج المريض لفترة أطول لاستعادة مستويات الطاقة الكاملة ومخازن الحديد التي استهلكت أثناء عملية البناء السريع للدم.
الأنواع الشائعة والطفرات الجينية لنقص الإنزيم G6PD
تصنف منظمة الصحة العالمية (WHO) حالات نقص الإنزيم G6PD إلى خمس فئات أساسية بناءً على شدة النقص الكيميائي الحيوي:
- الفئة الأولى (Class I): نقص شديد جداً مع فقر دم انحلالي مزمن (غير مرتبط بمحفزات)، وهي حالات نادرة جداً.
- الفئة الثانية (Class II): نقص شديد (أقل من 10% من النشاط الطبيعي)، ويتميز بنوبات حادة عند التعرض للمحفزات (مثل طفرة البحر المتوسط).
- الفئة الثالثة (Class III): نقص متوسط (10% إلى 60% من النشاط)، وتكون النوبات أقل حدة (مثل الطفرة الأفريقية A-).
- الفئة الرابعة (Class IV): نشاط طبيعي أو قريب من الطبيعي (60% إلى 100%)، ولا يعاني هؤلاء الأشخاص من أعراض سريرية.
- الفئة الخامسة (Class V): زيادة في نشاط الإنزيم، وهي حالة نادرة ليس لها دلالة مرضية معروفة.
التغذية والمحفزات الممنوعة لمرضى نقص الإنزيم G6PD
تعتبر الثقافة الغذائية هي خط الدفاع الأول ضد مضاعفات نقص الإنزيم G6PD. إليك القائمة التفصيلية للممنوعات:
- البقوليات الصريحة: الفول الأخضر، الفول المدمس، البصارة، الطعمية (الفلافل)، وفول الصويا.
- المحفزات البيئية: كرات النفتالين، صبغات الحناء المعالجة كيميائياً، وبعض المنظفات القوية.
- المشروبات: “المياه التونية” (Tonic Water) لاحتوائها على الكينين، وبعض مشروبات الطاقة التي تحتوي على أصباغ صناعية معينة.
- المواد المضافة: السلفيت (Sulfites) المستخدم كحافظ للأغذية، والجرعات العالية من المنثول (في بعض أنواع الحلوى).
- الأدوية المحظورة: السلفوناميدات، الأسبرين بجرعات عالية، أدوية الملاريا (بريموكين)، وبعض أدوية المسالك البولية (نيتروفورانتوين).
التأثيرات النفسية والاجتماعية للعيش مع “التفول”
لا تقتصر معاناة المصاب بـ نقص الإنزيم G6PD على الجانب الجسدي، بل تمتد لتشمل جوانب نفسية واجتماعية تتطلب دعماً من المحيطين.
يعاني الأطفال المصابون أحياناً من “قلق الطعام” في المدرسة أو الحفلات، حيث يشعرون بالخوف من تناول أي شيء قد يسبب لهم المرض، مما قد يؤدي للعزلة الاجتماعية.
من الضروري تثقيف المعلمين والأصدقاء حول طبيعة نقص الإنزيم G6PD لتجنب التنمر أو تقديم أطعمة خطرة للطفل عن غير قصد، مع التأكيد على أن المصاب يمكنه ممارسة حياته بشكل طبيعي تماماً مع الالتزام بالحمية.
نقص الإنزيم G6PD والزواج: الفحوصات الوراثية ونسب الانتقال
يعد فهم آلية الوراثة أمراً حيوياً للمقبلين على الزواج لتقدير احتمالية إصابة الأبناء بـ نقص الإنزيم G6PD.
- إذا كان الأب مصاباً والأم سليمة تماماً: جميع الأبناء الذكور سيكونون سليمين، بينما ستكون جميع البنات “حاملات” للجين المصاب.
- إذا كانت الأم حاملة للجين والأب سليم: هناك احتمالية 50% لإصابة كل ابن ذكر، واحتمالية 50% لكل ابنة لتكون حاملة للجين.
- إذا كان الأب مصاباً والأم حاملة للجين: هنا تظهر احتمالية إصابة البنات بنسبة 50% (نقص كامل)، بالإضافة لاحتمالية 50% لإصابة الذكور.
تساعد الاستشارة الجينية في تبديد المخاوف وشرح كيفية إدارة الحالة في حال قرر الزوجان الإنجاب، مع التأكيد على أن التشخيص المبكر يضمن حياة آمنة للطفل.
التطورات العلمية والعلاجات الجينية المستقبلية لنقص G6PD
يشهد عام 2026 طفرة في الأبحاث المتعلقة بعلاج نقص الإنزيم G6PD جذرياً عبر تقنيات تعديل الجينات (CRISPR-Cas9).
تجرى حالياً تجارب سريرية تهدف إلى تصحيح الطفرة في الخلايا الجذعية المكونة للدم، مما يسمح للجسم لإنتاج كريات دم حمراء تحتوي على مستويات طبيعية من الإنزيم مدى الحياة.
كما يتم تطوير علاجات تعتمد على “الحويصلات النانوية” لإيصال إنزيم G6PD مباشرة إلى مجرى الدم أثناء النوبات الحادة، مما قد يغني مستقبلاً عن عمليات نقل الدم المعقدة.
خرافات شائعة حول نقص الإنزيم G6PD
تنتشر الكثير من المغالطات حول نقص الإنزيم G6PD والتي قد تسبب قلقاً غير مبرر أو إهمالاً خطيراً:
- خرافة: “المرض يختفي مع التقدم في السن”.
- الحقيقة: الخلل الجيني دائم، لكن البالغين قد يتعلمون تجنب المحفزات بشكل أفضل من الأطفال.
- خرافة: “المصاب بـ نقص الإنزيم G6PD لا يمكنه ممارسة الرياضة”.
- الحقيقة: الرياضة آمنة تماماً طالما لم يكن هناك انحلال دم نشط، مع ضرورة الحفاظ على الترطيب.
- خرافة: “المرض يصيب الذكور فقط”.
- الحقيقة: الإناث يمكن أن يصبن بنقص كامل إذا ورثن الجين من كلا الوالدين، أو بنقص جزئي قد يسبب أعراضاً أحياناً.
نصائح ذهبية من “مدونة حياة الطبية” 💡
بصفتنا خبراء في الرعاية السريرية، نقدم لك هذه النصائح التي قد لا تجدها في المراجع التقليدية لإدارة نقص الإنزيم G6PD:
- قاعدة الـ 48 ساعة: عند الشك في تناول مادة محفزة، راقب لون البول بدقة لمدة يومين كاملين، فالانحلال لا يظهر دائماً في نفس اللحظة.
- كن سفيراً لحالتك: في المطاعم، لا تقل “لدي حساسية من البقوليات” فقط، بل اشرح صراحة أنك لا تستطيع تناول أي شيء يحتوي على الفول أو مشتقاته.
- ترطيب الكلى: أثناء أي عدوى فيروسية (حتى الزكام)، ضاعف كمية شرب الماء، فالجفاف يزيد من خطر ترسب الهيموجلوبين في الكلى إذا حدث تحلل خفيف.
- التوعية المدرسية: ضع ملصقاً صغيراً على حقيبة طعام طفلك يوضح حالته والأطعمة الممنوعة، مع رقم هاتف للطوارئ.
أسئلة شائعة حول نقص الإنزيم G6PD
هل يمكن للمصاب بـ نقص الإنزيم G6PD التبرع بالدم؟
طبياً، يفضل عدم تبرع المصاب بالدم، لأن كرياته لن تعيش طويلاً في جسم المتلقي وقد تسبب له مضاعفات إذا تعرض المتلقي لأي مواد مؤكسدة.
هل يؤثر نقص الإنزيم G6PD على الذكاء؟
لا يوجد أي تأثير للمرض على القدرات العقلية أو الذكاء، طالما تم تجنب النوبات الشديدة التي قد تسبب نقص أكسجين أو يرقان نووي في مرحلة الرضاعة.
هل اللقاحات آمنة لمرضى نقص الإنزيم G6PD؟
نعم، معظم اللقاحات (بما فيها لقاحات الإنفلونزا وكورونا) آمنة تماماً وموصى بها، لأن الإصابة بالمرض الفيروسي نفسه أخطر بكثير وقد تحفز نوبة انحلال حادة.
الخاتمة
يظل نقص الإنزيم G6PD حالة تتطلب الاحترام والوعي أكثر من الخوف. من خلال الالتزام بالحمية الغذائية، وتجنب المحفزات الدوائية، والمتابعة الطبية المنتظمة، يمكن للمصابين أن يعيشوا حياة مديدة ونشطة دون أي قيود تذكر على طموحاتهم. إن المعرفة هي المفتاح الحقيقي للسيطرة على هذا الاضطراب الجيني وتحويله من تحدٍ صحي إلى نمط حياة آمن.