يُعد فقد البروتين الشحمي بيتا من الدم (Abetalipoproteinemia)، المعروف أيضاً بمتلازمة باسن-كورنزويج، اضطراباً وراثياً نادراً للغاية يعيق قدرة الجسم على امتصاص الدهون الغذائية والفيتامينات الذائبة في الدهون بشكل طبيعي. توضح مدونة حياة الطبية أن هذا الخلل الكيميائي الحيوي يؤدي إلى نقص حاد في مستويات الكوليسترول والدهون الثلاثية، مما يسبب مضاعفات جهازية تشمل الجهاز الهضمي والعصبي والبصري.
ما هو فقد البروتين الشحمي بيتا من الدم؟
يعتبر فقد البروتين الشحمي بيتا من الدم حالة مرضية جينية تتميز بغياب شبه تام للبروتينات الدهنية المحتوية على “أبوليبروتين ب” (Apolipoprotein B) من البلازما، وهو الناقل الأساسي للدهون. (وفقاً للمعهد الوطني للصحة NIH، فإن هذا المرض يمنع تكوين الكيلوميكرونات والبروتينات الدهنية منخفضة الكثافة جداً VLDL). يؤدي هذا الفشل الوظيفي إلى تراكم الدهون داخل خلايا الأمعاء والكبد بدلاً من إطلاقها في الدورة الدموية، مما يحرم الجسم من الأحماض الدهنية الأساسية والفيتامينات الحيوية مثل A وE وK وD.

أعراض فقد البروتين الشحمي بيتا من الدم
تظهر أعراض فقد البروتين الشحمي بيتا من الدم عادةً في الأشهر الأولى من الحياة، وتتطور تدريجياً لتشمل أجهزة متعددة نتيجة النقص المزمن في العناصر الغذائية، وتتمثل في الآتي:
- الأعراض الهضمية المبكرة:
- الإسهال الدهني المزمن (براز شاحب، كريه الرائحة، وطافٍ).
- انتفاخ البطن الملحوظ وبروزه بشكل غير طبيعي.
- فشل النمو (Failure to thrive) وتأخر زيادة الوزن عند الرضع.
- نوبات من القيء المتكرر وصعوبة الرضاعة.
- الأعراض العصبية والعضلية:
- الترنح (Ataxia) وهو فقدان التنسيق الحركي أثناء المشي.
- ضعف العضلات التدريجي الذي قد يبدأ في الأطراف السفلية.
- فقدان ردود الفعل الوترية العميقة في الركبتين والكاحلين.
- صعوبات في النطق والبلع في المراحل المتقدمة.
- فقدان الحس الاهتزازي وحس الموضع في الأطراف.
- الأعراض البصرية (المرتبطة بنقص فيتامين A وE):
- التهاب الشبكية الصباغي (Retinitis Pigmentosa) الذي يؤدي لتدهور الرؤية.
- العشى الليلي أو صعوبة التكيف مع الإضاءة الخافتة.
- فقدان الرؤية المحيطية (الرؤية النفقية).
- أعراض الدم والمختبر:
- ظهور الخلايا المهمازية (Acanthocytosis) وهي كريات دم حمراء مشوهة الأطراف.
- فقر الدم الناجم عن خلل في جدار الخلية الحمراء.
- الميل للنزف التلقائي نتيجة نقص فيتامين K الضروري للتجلط.
أسباب فقد البروتين الشحمي بيتا من الدم
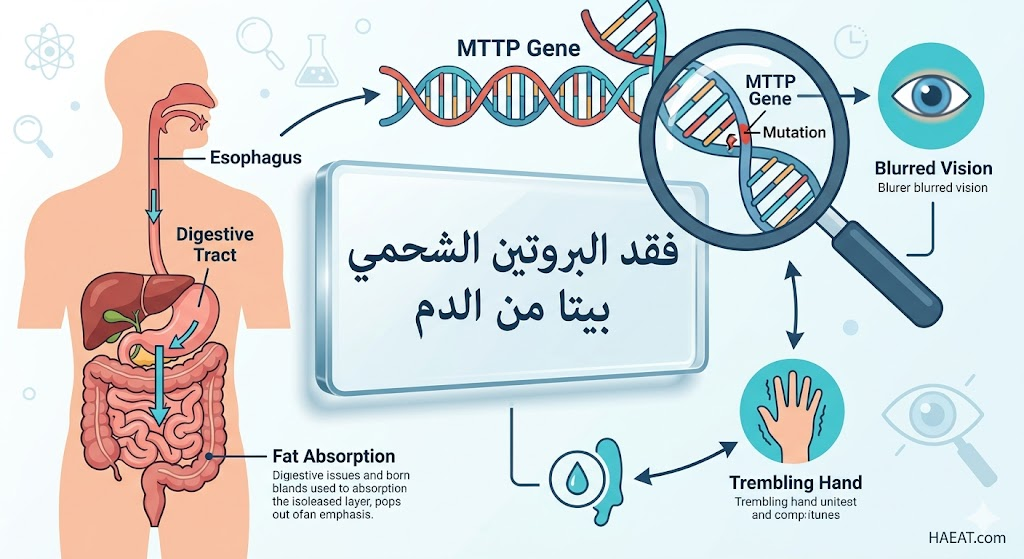
تتمحور أسباب الإصابة بمرض فقد البروتين الشحمي بيتا من الدم حول طفرات جينية محددة تؤثر على استقلاب الدهون، وتبرز النقاط التالية الآلية البيولوجية للمرض:
- طفرة جين MTTP: المسبب الرئيسي هو وجود طفرة في جين البروتين الناقل للدهون الثلاثية الميكروسومي (Microsomal Triglyceride Transfer Protein).
- فشل تجميع البروتينات الدهنية: يعمل بروتين MTTP كـ “مهندس” يقوم بتركيب الدهون مع البروتين (ApoB)؛ وبغيابه، لا يمكن للأمعاء والكبد بناء ناقلات الدهون.
- الوراثة المندلية المتنحية: يتطلب الإصابة بمرض فقد البروتين الشحمي بيتا من الدم وراثة نسختين من الجين المعيب (واحدة من كل والد)، مما يجعل زواج الأقارب عاملاً مؤثراً.
- تراكم الدهون الخلوي: نظراً لعدم القدرة على تصدير الدهون، تتراكم قطرات الدهون (Vacuoles) داخل خلايا الأمعاء (Enterocytes) مما يسبب سوء الامتصاص.
- نقص الفيتامينات الذائبة في الدهون: يعد تعطل امتصاص فيتامين E هو الأخطر، حيث يعمل كمضاد أكسدة لحماية الأعصاب والشبكية، وبدونه يبدأ التحلل العصبي.
متى تزور الطبيب؟
يتطلب اضطراب فقد البروتين الشحمي بيتا من الدم تدخلاً طبياً عاجلاً فور ملاحظة علامات سوء الامتصاص الحاد، لضمان تقليل الضرر العصبي المستقبلي.
العلامات التحذيرية لدى البالغين
يجب على البالغين الذين لديهم تاريخ عائلي من اضطرابات الدهون أو الذين يعانون من مشاكل مفاجئة في التوازن المشي، أو تدهور غير مبرر في الرؤية الليلية، التوجه فوراً لإجراء فحص دم شامل. إن ظهور تنميل مستمر في الأطراف أو ضعف عضلي غير مبرر قد يشير إلى بدء تآكل الغمد المياليني للأعصاب نتيجة نقص المغذيات المرتبط بمرض فقد البروتين الشحمي بيتا من الدم.
المؤشرات الحرجة لدى الأطفال والرضع
تعتبر الشهور الأولى من العمر حاسمة؛ فإذا لاحظ الوالدان أن الرضيع لا يكتسب وزناً رغم التغذية الجيدة، أو إذا كان البراز ذا طبيعة دهنية واضحة ورائحة نفاذة جداً، فإن استشارة أخصائي أمراض هضمية للأطفال تصبح ضرورة. التشخيص المبكر لمرض فقد البروتين الشحمي بيتا من الدم عند الأطفال ينقذهم من الإعاقة الحركية الدائمة وفقدان البصر الكلي.
التنبؤ بالتشخيص المبكر عبر الخوارزميات الجينية
في العصر الحديث، يقترح الباحثون استخدام الخوارزميات الجينية المتقدمة لتحليل تسلسل الإكسوم الكامل للأطفال الذين يظهرون أعراضاً غامضة لسوء الامتصاص. تساعد هذه التقنيات في تحديد طفرات MTTP حتى قبل ظهور الأعراض العصبية الواضحة لمرض فقد البروتين الشحمي بيتا من الدم، مما يسمح ببدء بروتوكول المكملات الغذائية بجرعات عالية مبكراً جداً، وهو ما يحسن التوقعات المستقبلية للحالة بشكل كبير.
عوامل خطر الإصابة بـ فقد البروتين الشحمي بيتا من الدم
تعتبر عوامل الخطر المرتبطة بمرض فقد البروتين الشحمي بيتا من الدم محصورة بشكل أساسي في النطاق الوراثي، نظراً لطبيعته كاضطراب جيني متنحٍ، وتشمل العوامل التالية:
- التاريخ العائلي والجيني: وجود طفرات في جين MTTP لدى كلا الوالدين، حتى وإن كانا لا يعانيان من أعراض ظاهرة (حاملين للمرض).
- زواج الأقارب: ترتفع احتمالية الإصابة بمرض فقد البروتين الشحمي بيتا من الدم بشكل ملحوظ في المجتمعات التي يشيع فيها زواج الأقارب، حيث تزداد فرص التقاء الجينات المتنحية المعيبة.
- الأصول العرقية: على الرغم من ندرته العالمية، إلا أن بعض الدراسات رصدت تركزاً طفيفاً للحالات في مناطق حوض البحر الأبيض المتوسط وبعض مناطق الشرق الأوسط نتيجة العوامل الجينية المشتركة.
- وجود أشقاء مصابين: إذا كان هناك طفل مصاب في العائلة، فإن احتمالية إصابة الأشقاء اللاحقين بمرض فقد البروتين الشحمي بيتا من الدم تصل إلى 25% لكل حمل.
مضاعفات فقد البروتين الشحمي بيتا من الدم
في حال إهمال العلاج أو التأخر في التشخيص، يؤدي فقد البروتين الشحمي بيتا من الدم إلى تدهور جسيم في الوظائف الحيوية نتيجة التحلل التأكسدي للأنسجة، وتتمثل المضاعفات في:
- التحلل العصبي التدريجي: تآكل المسارات العصبية في الحبل الشوكي (Spinocerebellar degeneration)، مما يؤدي لفقدان القدرة على المشي بشكل مستقل.
- العمى الكلي: تطور التهاب الشبكية الصباغي لدرجة تجعل المريض يفقد القدرة على الإبصار تماماً، وهو مضاعف ناتج مباشرة عن نقص فيتامين A وE المزمن.
- تليف الكبد والتهابه: نتيجة تراكم الدهون الثلاثية داخل خلايا الكبد وعدم قدرتها على الخروج، يتطور الأمر إلى “الكبد الدهني” (Steatohepatitis) الذي قد ينتهي بالتليف.
- قصور القلب: في حالات نادرة، يمكن أن يؤثر نقص فيتامين E الشديد على عضلة القلب، مما يسبب اعتلالاً قد يهدد الحياة.
- تشوهات العمود الفقري: مثل الجنف (Scoliosis)، نتيجة ضعف العضلات الهيكلية وعدم قدرتها على دعم الهيكل العظمي بشكل صحيح.
الوقاية من فقد البروتين الشحمي بيتا من الدم
نظراً لكون فقد البروتين الشحمي بيتا من الدم اضطراباً جينياً، فإن الوقاية تركز بشكل أساسي على الاستشارة الوراثية والتدابير الاستباقية:
- الفحص الجيني ما قبل الزواج: خاصة في العائلات التي لديها تاريخ مع اضطرابات الدهون أو سوء الامتصاص الغامض.
- التشخيص الوراثي قبل الانغراس (PGD): للأزواج المعروفين بحملهم لطفرات جين MTTP، لضمان اختيار أجنة سليمة.
- الفحص المبكر لحديثي الولادة: عند وجود أخ مصاب، يجب إجراء تحليل دم فوري للمولود الجديد لقياس مستويات الكوليسترول.
- التوعية المجتمعية: تثقيف الأسر حول مخاطر زواج الأقارب في حال وجود أمراض وراثية متنحية معروفة في شجرة العائلة.
تشخيص فقد البروتين الشحمي بيتا من الدم
يعتمد موقع حياة الطبي في توضيح مسار التشخيص على تسلسل يبدأ من الملاحظة السريرية وينتهي بالتدقيق الجزيئي:
- الملف الدهني الكامل (Lipid Profile): يظهر نتائج صادمة تتمثل في مستويات منخفضة للغاية من الكوليسترول الكلي (غالباً أقل من 50 مجم/ديسيلتر) وغياب شبه تام لـ LDL وVLDL.
- فحص لطخة الدم (Blood Smear): البحث عن “الخلايا المهمازية” (Acanthocytes)، وهي كريات دم حمراء ذات نتوءات غير منتظمة تشبه النجوم، وتظهر في 50-90% من الحالات.
- اختبار امتصاص الدهون: قياس كمية الدهون في البراز على مدار 72 ساعة، حيث يظهر فقدان كميات هائلة من الدهون غير الممتصة.
- خزعة الأمعاء الدقيقة: تظهر خلايا الأمعاء ممتلئة بقطرات الدهون (Lipid-laden enterocytes) رغم الصيام، وهو مؤشر قاطع على فشل تصدير الدهون.
- التصوير بالرنين المغناطيسي (MRI): لتقييم مدى تضرر الحبل الشوكي والأعصاب المحيطية في المراحل المتقدمة.
- الاختبار الجيني الجزيئي: هو المعيار الذهبي، حيث يتم تحديد الطفرات في جين MTTP لتأكيد الإصابة بمرض فقد البروتين الشحمي بيتا من الدم بشكل نهائي.
علاج فقد البروتين الشحمي بيتا من الدم
يتطلب علاج فقد البروتين الشحمي بيتا من الدم استراتيجية متعددة الأوجه تهدف إلى تعويض النقص ومنع التدهور العصبي.
التعديلات الغذائية ونمط الحياة كخط أول للعلاج
يكمن مفتاح السيطرة على أعراض الجهاز الهضمي في اتباع نظام غذائي صارم للغاية منخفض الدهون (أقل من 15-20 جراماً يومياً). يجب تجنب الدهون طويلة السلسلة (LCT) لأنها تتطلب الكيلوميكرونات للامتصاص، وهو ما يفتقده مريض فقد البروتين الشحمي بيتا من الدم. بدلاً من ذلك، يتم الاعتماد على الدهون متوسطة السلسلة (MCT) التي يمكن امتصاصها مباشرة في الدورة الدموية البابية دون الحاجة لبروتينات ناقلة.
العلاجات الدوائية والمكملات الغذائية بجرعات عالية
العلاج الأساسي ليس دواءً تقليدياً، بل هو مكملات فيتامينية بجرعات “ضخمة” تتجاوز الاحتياج اليومي العادي بمئات المرات لضمان وصول قدر بسيط منها للأنسجة عبر الانتشار السلبي.
بروتول علاج البالغين
يتضمن تعاطي فيتامين E (ألفا-توكوفيرول) بجرعات تتراوح بين 100-200 وحدة دولية لكل كيلوجرام من وزن الجسم يومياً. كما يركز البرنامج على مكملات فيتامين A لمنع العشى الليلي، وفيتامين K (حوالي 5 مجم يومياً أو أسبوعياً حسب الحالة) للحفاظ على عوامل التجلط، وفيتامين D للوقاية من هشاشة العظام المرتبطة بمرض فقد البروتين الشحمي بيتا من الدم.
بروتوكول علاج الأطفال
يحتاج الأطفال لرقابة لصيقة لضمان النمو البدني. يتم إعطاء المكملات السائلة أو المسحوقة بجرعات دقيقة، مع التركيز على تدعيم النظام الغذائي بالأحماض الدهنية الأساسية (مثل حمض اللينوليك) الضرورية لتطور الدماغ والجهاز العصبي. يجب إجراء فحوصات دورية للكبد والعين لضبط الجرعات ومنع السمية الناتجة عن تراكم فيتامين A.
البروتوكولات المستقبلية والعلاجات الجينية الواعدة
وفقاً لأحدث الأبحاث المنشورة في دورية (The Lancet)، هناك تجارب مخبرية واعدة لاستخدام تقنية CRISPR لتعديل جين MTTP المعيب. كما يتم دراسة إمكانية استخدام نواقل فيروسية لتوصيل نسخة سليمة من الجين إلى خلايا الأمعاء والكبد، مما قد يسمح للمرضى المصابين بـ فقد البروتين الشحمي بيتا من الدم بإنتاج البروتينات الدهنية بشكل طبيعي لأول مرة في حياتهم، وهو ما ينهي عصر الاعتماد الكلي على المكملات.

الطب البديل وفقد البروتين الشحمي بيتا من الدم
لا يمكن للطب البديل أن يكون بديلاً عن البروتوكول الدوائي والغذائي الصارم لمرض فقد البروتين الشحمي بيتا من الدم، ولكنه يلعب دوراً “تدعيمياً” لتقليل الالتهاب وتحسين جودة الحياة:
- زيوت MCT النقية: تعتبر الزيوت متوسطة السلسلة المستخلصة من جوز الهند والتمور هي الركيزة الأساسية في “الطب التكميلي” لهذه الحالة، حيث توفر مصدراً آمناً للطاقة لا يعتمد على المسارات المعطلة.
- مضادات الأكسدة الطبيعية: استخدام الكركمين (الموجود في الكركم) بجرعات مدروسة قد يساعد في تقليل الإجهاد التأكسدي في الأمعاء والكبد الناتج عن تراكم الدهون.
- الوخز بالإبر: قد يلجأ البعض لاستخدامه كعلاج تكميلي لتخفيف آلام الأعصاب الطرفية الناتجة عن تدهور الجهاز العصبي المرتبط بمرض فقد البروتين الشحمي بيتا من الدم.
- العلاج بالأعشاب الملينة: استخدام الألياف القابلة للذوبان بحذر للمساعدة في تحسين قوام البراز الدهني وتقليل الانتفاخات المزعجة.
الاستعداد لموعدك مع الطبيب
يتطلب التعامل مع اضطراب نادر مثل فقد البروتين الشحمي بيتا من الدم تنظيماً دقيقاً للمعلومات الطبية لضمان الحصول على أفضل استشارة ممكنة.
ما يجب عليك فعله قبل الموعد
يجب توثيق كافة الأعراض الهضمية بدقة، بما في ذلك عدد مرات الإسهال وطبيعته. تنصح مدونة HAEAT الطبية بضرورة إحضار شجرة العائلة الكاملة لتحديد أي حالات مشابهة، بالإضافة إلى نتائج فحوصات النظر السابقة وصور الدم التي قد تشير إلى وجود الخلايا المهمازية.
ما الذي تتوقعه من الطبيب
سيقوم الطبيب غالباً بإجراء فحص عصبي دقيق لتقييم المنعكسات والتوازن. من المتوقع أن يطلب الطبيب تحاليل مخبرية صائمة لقياس مستويات البروتين الدهني الوضيع الكثافة (VLDL) والكوليسترول، وقد يحيلك إلى أخصائي وراثة لتأكيد طفرة جين MTTP المسببة لمرض فقد البروتين الشحمي بيتا من الدم.
استخدام تطبيقات التتبع الرقمي لتوثيق الحالة
في عصر الطب الرقمي، يمكن استخدام تطبيقات تتبع التغذية والأعراض لإنشاء “سجل حي” يتم تقديمه للطبيب. يساعد هذا السجل في رصد مدى استجابة الجسم لجرعات فيتامين E العالية، وتحديد ما إذا كان هناك تحسن في مستويات الطاقة أو تقليل في نوبات الإسهال المرتبطة بمرض فقد البروتين الشحمي بيتا من الدم.
مراحل الشفاء من فقد البروتين الشحمي بيتا من الدم
يجب توضيح أن “الشفاء” في حالة فقد البروتين الشحمي بيتا من الدم يعني “الإدارة الناجحة والسيطرة” وليس اختفاء المرض، وتمر العملية بالمراحل التالية:
- المرحلة الأولى (الاستقرار الهضمي): تبدأ فور اتباع الحمية منخفضة الدهون، حيث يتوقف الإسهال الدهني ويبدأ الوزن في التحسن.
- المرحلة الثانية (التعويض الفيتاميني): تهدف للوصول إلى مستويات فيتامين E في الدم تمنع التدهور العصبي الإضافي.
- المرحلة الثالثة (المراقبة المستمرة): تشمل فحوصات دورية للشبكية ووظائف الكبد كل 6-12 شهراً لضمان عدم حدوث مضاعفات صامتة.
- المرحلة الرابعة (التعايش طويل الأمد): الوصول إلى حالة من الاستقرار حيث يمارس المريض حياته الطبيعية مع التزام صارم بالمكملات الغذائية.
الأنواع الشائعة لفقد البروتين الشحمي بيتا من الدم
على الرغم من كونه مرضاً محدداً، إلا أن هناك اضطرابات تشترك معه في الخصائص ويجب التمييز بينها:
- فقد البروتين الشحمي بيتا التقليدي: الناتج عن طفرات جين MTTP (موضوعنا الأساسي).
- نقص البيتا ليبوبروتين الوراثي (Hypobetalipoproteinemia): حالة أقل شدة تنتج عن طفرات في جين APOB، وتكون مستويات الدهون فيها منخفضة ولكنها ليست غائبة تماماً.
- مرض اندخار الكيلوميكرونات (Chylomicron Retention Disease): حيث تفشل الأمعاء فقط في إفراز الكيلوميكرونات، بينما يظل الكبد قادراً على إفراز VLDL.
التأثيرات العصبية والفسيولوجية طويلة الأمد لمرض فقد البروتين الشحمي بيتا من الدم
يمتد تأثير فقد البروتين الشحمي بيتا من الدم إلى أبعد من سوء الامتصاص؛ حيث يؤدي غياب فيتامين E إلى فقدان حماية الخلايا العصبية من التدمير التأكسدي. مع مرور السنين، قد تظهر صعوبات في التنسيق الحركي الدقيق (مثل الكتابة) وتدهور في الوظائف الحسية للأطراف. تشير الدراسات إلى أن الالتزام بالجرعات العالية من مضادات الأكسدة هو العامل الوحيد القادر على إبطاء هذا التدهور الفسيولوجي وحماية النخاع الشوكي من التآكل المزمن.
الدليل الغذائي الصارم: قائمة المسموح والممنوع لمرضى فقد البروتين الشحمي بيتا من الدم
يعد هذا القسم حجر الزاوية في إدارة فقد البروتين الشحمي بيتا من الدم، حيث يجب أن تكون الدهون أقل من 5% من إجمالي السعرات:
| التصنيف | المسموح (صديق للمريض) | الممنوع (خطر) |
| البروتينات | صدر دجاج بدون جلد، بياض بيض، سمك أبيض مشوي. | اللحوم الحمراء، صفار البيض، السجق، البط. |
| الألبان | حليب خالي الدسم تماماً، زبادي 0% دسم. | الزبدة، القشطة، الأجبان الصفراء والدسمة. |
| الزيوت | زيت MCT فقط (بكميات محددة). | زيت الزيتون، الزيوت النباتية، السمن، المايونيز. |
| الخضروات | جميع الأنواع (مسلوقة أو مشوية بدون زيت). | الخضروات المقلية أو المطبوخة بمرق دسم. |
| الفواكه | جميع الفواكه الطازجة. | الأفوكادو (نظراً لمحتواه العالي من الدهون). |
التطورات الجينية الحديثة في فهم طفرات جين MTTP وتأثيرها على النمط الظاهري
لقد كشفت الأبحاث الجينية الحديثة أن هناك أكثر من 50 طفرة مختلفة في جين MTTP يمكن أن تؤدي إلى فقد البروتين الشحمي بيتا من الدم. تختلف شدة المرض بناءً على نوع الطفرة؛ فبعضها يؤدي إلى غياب كامل للبروتين، بينما يترك البعض الآخر نشاطاً ضئيلاً جداً قد يؤخر ظهور الأعراض العصبية حتى سن المراهقة. يساعد فهم “النمط الظاهري” (Phenotype) للأطباء في تخصيص العلاج وتوقع سرعة تدهور حالة الشبكية.
الجوانب النفسية والاجتماعية للمصابين بمرض فقد البروتين الشحمي بيتا من الدم
العيش مع اضطراب نادر يتطلب قيوداً غذائية صارمة يمكن أن يؤدي إلى “عزلة اجتماعية”. يعاني المرضى المصابون بـ فقد البروتين الشحمي بيتا من الدم غالباً من قلق متعلق بالوجبات الخارجية والتجمعات الاجتماعية. يوصي الخبراء بضرورة دمج الدعم النفسي كجزء من الخطة العلاجية، ومحاولة التواصل مع مجموعات دعم المصابين بالأمراض النادرة لتقليل الشعور بالاغتراب المرضي.
خرافات شائعة حول فقد البروتين الشحمي بيتا من الدم
- خرافة: الكوليسترول المنخفض جداً هو علامة على الصحة المثالية دائماً.
- الحقيقة: في حالة فقد البروتين الشحمي بيتا من الدم، يكون الكوليسترول المنخفض جداً مؤشراً خطيراً على فشل نقل الفيتامينات الحيوية.
- خرافة: المرض معدٍ ويمكن أن ينتقل بين الأشقاء بالاختلاط.
- الحقيقة: هو اضطراب وراثي جيني بحت ولا ينتقل إلا عبر التوريث من الأبوين.
- خرافة: يمكن الشفاء منه عبر تناول جرعة واحدة من الفيتامينات.
- الحقيقة: العلاج يحتاج لمتابعة مدى الحياة بجرعات ضخمة يومية.
نصائح ذهبية من “مدونة حياة الطبية” 💡
يقدم لك خبراء موقع حياة الطبي هذه النصائح الجوهرية للتعايش مع فقد البروتين الشحمي بيتا من الدم:
- قاعدة الـ 15 جراماً: لا تتجاوز أبداً 15 جراماً من الدهون التقليدية يومياً لتجنب نوبات الإسهال المؤلمة.
- الفحص البصري الدوري: التزم بفحص قاع العين كل 6 أشهر؛ فالشبكية هي مرآة كفاية مستويات فيتامين E في جسمك.
- الطهي بذكاء: استخدم تقنيات الطهي بالبخار أو القلايات الهوائية بدون نقطة زيت واحدة للحفاظ على مذاق الطعام.
- التوعية المدرسية: إذا كان طفلك مصاباً، تأكد من إبلاغ المدرسة بوضوح عن قيوده الغذائية الصارمة لمنع تناول وجبات غير مناسبة.
أسئلة شائعة
هل يؤثر فقد البروتين الشحمي بيتا من الدم على العمر المتوقع؟
مع التشخيص المبكر والالتزام الصارم بتعويض الفيتامينات، يمكن للمرضى أن يعيشوا حياة طبيعية وطويلة. تكمن الخطورة فقط في إهمال المكملات مما يؤدي لمضاعفات قلبية وعصبية.
هل يمكن للمرأة المصابة بمرض فقد البروتين الشحمي بيتا من الدم أن تحمل وتلد؟
نعم، ولكن تحت إشراف طبي دقيق جداً لضمان وصول مستويات كافية من الفيتامينات والدهون الأساسية للجنين، حيث أن نقصها قد يؤثر على نمو دماغ الجنين.
لماذا تظهر الخلايا المهمازية في الدم؟
تظهر نتيجة خلل في توزيع الدهون في جدار الخلية الحمراء بسبب نقص الكوليسترول والفسفوليبيدات، مما يجعل غشاء الخلية غير مستقر ويتخذ شكلاً مشوكاً.
الخاتمة
يمثل فقد البروتين الشحمي بيتا من الدم تحدياً طبياً يتطلب تضافر الجهود بين المريض والأطباء وأخصائيي التغذية. على الرغم من ندرة الحالة، إلا أن الالتزام بالعلاجات الحديثة والوعي الجيني يفتح آفاقاً واسعة لحياة مستقرة بعيدة عن العجز. تأمل مدونة حياة الطبية أن يكون هذا الدليل منارة لكل من يبحث عن فهم أعمق لهذا المرض النادر.